
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Строение реальных веществ
|
|
|
|
Законы идеальных газов (ИГ) – приближенные законы. При описании реальных газов, в отличие от ИГ, для получения действительных значений параметров состояния необходимо учитывать собственный объем молекул и межмолекулярное взаимодействие. Особенно заметно различие измеряемых значений параметров реальных газов и получаемых из уравнения Менделеева–Клапейрона при низких температурах и высоких давлениях (высокой концентрации, а следовательно, собственном объеме молекул газа, сравнимом с объемом занимаемого сосуда).
Способность твердых тел (ТТ) сопротивляться растяжению и газов сопротивляться сжатию приводит к выводу о существовании сил взаимного притяжения и отталкивания между молекулами вещества, причем на малых расстояниях преобладают силы отталкивания, а с увеличением расстояния – силы притяжения. Данные силы являются короткодействующими. Радиус их действия ориентировочно ~10-9 м, т.к. нельзя говорить о равенстве сил взаимодействия нулю вне сферы молекулярного действия, а лишь об их сравнительно малом значении (быстро, ~r -7, убывают с увеличением расстояния, см. рис. 13.1, а). Так как изменение потенциальной энергии
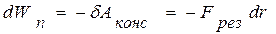 ,
,
то
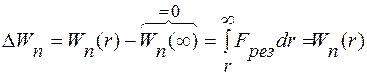 .
.
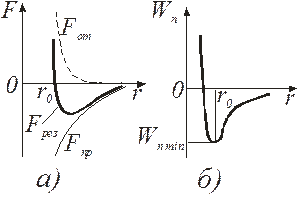
Рис. 13.1
Графически зависимость Wn(r) представлена на рис. 13.1, б. При условии
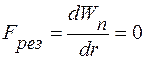 (13.1)
(13.1)
осуществляется состояние равновесия, которое характеризуется минимумом потенциальной энергии. В общем случае в природе система всегда стремится перейти в состояние, характеризуемое минимальной энергией.
Как известно, на одну степень свободы приходится энергия kT /2. Величина kT служит своеобразным критерием определения агрегатного состояния вещества: для газов Wn<<kT (интенсивное тепловое движение молекул), для ТТ Wn>>kT (атомы достаточно жестко фиксированы, лишь колеблются в узлах кристаллической решетки), для жидкостей Wn»kT (молекулы колеблются у одного положения равновесия в течение так называемого времени оседлой жизни и перескакивают из него в другое, что подтверждается броуновским движением).
|
|
|
|
|
Дата добавления: 2015-06-04; Просмотров: 358; Нарушение авторских прав?; Мы поможем в написании вашей работы!