
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Лабораторна робота № 10 Йодометричне визначення міді
|
|
|
|
Контрольні питання.
1. Чому неможливо приготувати титрований розчин Na2S2O3 розчиненням точної наважки Na2S2O3?
2. Якими домішками може бути забруднений Na2S2O3?
3. Які стандартні речовини можна використовувати для стандартизації Na2S2O3?
4. Обчисліть масу наважки калій біхромату яку необхідно взяти для стандартизації 0,1н розчину Na2S2O3, якщо об'єм колби 200 см3, а об’єм піпетки дорювнює10 см3. Місткість бюретки 50 см3.
Мета: Визначити масу міді.
Обладнання та посуд:.
1.Бюретка, 50,0 мл;
2.Колба для титрування;
3.Мірний циліндр, 25мл;
4. Титрований розчин Na2S2O3;
5.Сірчана кислота H2SO4 (1:4);
6.Калію йодид КІ;
7. 1% розчин крохмалю.
Завдання:
1. Обчислити масу міді.
В слабко кислому розчині йони міді Cu2+ окислюють йодистий калій з утворенням вільного йоду, який титрують стандартним розчином тіосульфату натрію
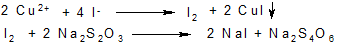
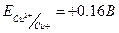 а для йоду
а для йоду 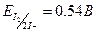 , тобто йодид є більш сильним окисником, ніж Сu2+. Здвиг рівноваги вправо пояснюється тим, що концентрація одновалентної міді в результаті утворення малорозчинного осаду різко зменшується, при цьому реальний потенціал системи зростає до +0,75 В.
, тобто йодид є більш сильним окисником, ніж Сu2+. Здвиг рівноваги вправо пояснюється тим, що концентрація одновалентної міді в результаті утворення малорозчинного осаду різко зменшується, при цьому реальний потенціал системи зростає до +0,75 В.
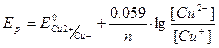
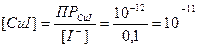 моль/л
моль/л
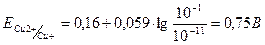
При цьому виявлення міді проводять в слабко кислому середовищі, для припинення гідролізу.
Хід аналіза. До досліджуваного розчину додають 5 см3 сірчаної кислоти (1:4) та 1 г йодистого калію. Суміш стоїть 2-3 хвилини, а йод, що виділився титрують тіосульфатом натрію до появи жовтого забарвлення, а потім 1 см3 крохмалю (20 крапель), проводять титрування до зникнення синього забарвлення. Розраховують масу міді за формулою:
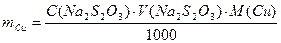
|
|
|
|
|
Дата добавления: 2015-06-28; Просмотров: 477; Нарушение авторских прав?; Мы поможем в написании вашей работы!