
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Лекция 5. Производство и производственная структура
|
|
|
|
Ртуть
Ртуть сравнительно легко извлекается из руд и, несмотря на относительно ограниченное практическое применение, широко известна в течение многих веков. Ртуть - своеобразный металл, в нормальных условиях это жидкость. Именно из-за этого ртуть была названа «жидким серебром».
& В эпоху Ренессанса ртуть в основном ценилась своими медицинскими свойствами, а также использовалась в смеси с другими металлами как средство серебрения зеркал. Для средневековых алхимиков ртуть имела особую ценность и играла важную роль в поисках философского камня - таинственного вещества, которое превращает простые металлы в золото. Только в последнее столетие доказано, что ртуть участвует во многих химических реакциях как катализатор.
Благодаря своим свойствам она находит широкое применение в промышленности. Ежегодно в мире получают более 10 тыс. т ртути. Из них примерно 25% используют для производства электродов при получении хлора и щелочей, 20% - в электрическом оборудовании, 15% - при производстве красок, 10% - для производства ртутных приборов, таких, как термометры, 5% - в производстве зеркал, в агрохимии и 3% в качестве ртутной амальгамы при лечении зубов. Еще около 25% производимой ртути используется в других отраслях промышленности: при получении детонаторов, катализаторов (например, для производства ацетальдегида и поливинилхлорида), в производстве бумажной пульпы, фармацевтике и косметике, а также военных целях. Промышленное значение имеют высокотоксичные неорганические соединения ртути, в частности сулема, из которой получают другие ртутные соединения, и которая применяется при травлении стали. Сулема вызывает смертельные отравления при приеме внутрь в количестве 0,2...0,3 г. Органические соединения ртути применяли в качестве фунгицидов при обработке зерна. Однако с тех пор, как стало известно об опасности подобных соединений, во многих странах их использование было запрещено.
Подсчитано, что кроме 10 тыс. т ртути, добываемых в мире при горнорудных разработках, еще 10 тыс. т металла выделяется в окружающую среду при сгорании угля, нефти и газа, добыче пустой породы и других индустриальных разработках. Естественным образом ежегодно от 30 тыс. до 150 тыс. т ртути выделяется при дегазации земной коры и океанов.
Ртуть относится к числу рассеянных в природе микроэлементов. По распространению в земной коре она занимает 62-е место, средняя концентрация составляет 0,5 мг/кг. В природе ртуть находится в 3-х окисленных состояниях: металлическая или атомарная (Hgо), окисленная со степенью окисления +1 (Hg+) и окисленная со степенью окисления +2 (Hg2+). Свойства ртути в различных степенях окисления (+1, +2) определяются окислительно-восстановительным потенциалом раствора и присутствием комплексных соединений. Ион Hg2+ может образовывать стабильные комплексы с биологическими соединениями, особенно через сульфгидрильные группы. В водном растворе образуются 4 соединения с хлором HgCl+, HgCl2, HgCl3- и HgCl42-.
i В пищевых продуктах ртуть может присутствовать в 3-х видах: атомарная ртуть, окисленная ртуть Hg2+ и алкилртуть - соединения ртути с алкилирующими соединениями.
Случаи загрязнения пищевых продуктов металлической ртутью являются очень редкими. Известно несколько случаев преднамеренного отравления потребителя, например, когда апельсины из Израиля были обработаны металлической ртутью палестинскими активистами в 1978 г. Ртуть плохо адсорбируется на продуктах и легко удаляется с поверхности пищи.
☞ С токсикологической точки зрения ртуть наиболее опасна, когда она присоединена к углеродному атому метиловой, этиловой или пропиловой группы - это алкильные соединения с короткой цепью.
Металлическая ртуть может метилироваться в две стадии:

 Hg CH3Hg+ (CH3)2Hg
Hg CH3Hg+ (CH3)2Hg
Процесс метилирования ртути является ключевым звеном в ее биокумуляции по пищевым цепям водных экосистем. Метил- ии диметилртуть сорбируются организмом. Если в основных пищевых продуктах содержание ртути менее 60 мкг на кг продукта, то в пресноводной рыбе из незагрязненных рек и водохранилищ, это содержание составляет от 100 до 200 мкг/кг массы тела, а из загрязненных - 500...700 мкг/кг. Среднее количество ртути в морских рыбах составляет 150 мкг на кг их массы.
 Ртуть аккумулируют планктонные организмы (например, водоросли), которыми питаются ракообразные. Ракообразных поедают рыбы, а рыб птицы. Концевыми звеньями пищевых цепей нередко бывают чайки и орланы. Человек может включаться на любом этапе и, в свою очередь, тоже становиться
Ртуть аккумулируют планктонные организмы (например, водоросли), которыми питаются ракообразные. Ракообразных поедают рыбы, а рыб птицы. Концевыми звеньями пищевых цепей нередко бывают чайки и орланы. Человек может включаться на любом этапе и, в свою очередь, тоже становиться
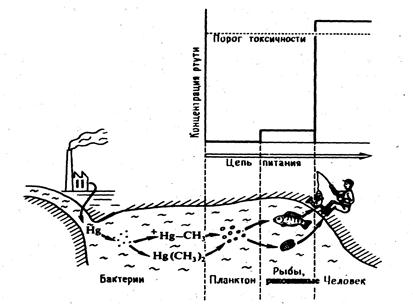 |
концевым звеном; большей частью это происходит в результате потребления рыбы (рисунок 6).
Рисунок 6 - Микробиологический метаболизм ртути в воде и ее накопление в цепи
питания (Fellenberg C., 1997)
За естественное содержание ртути в рыбах принимают величину 0,1...0,2 мг/кг. ВОЗ предложила считать предельно допустимой концентрацией 0,5 мг/кг; эта величина, вероятно, завышена.
& Поэтому в Финляндии рекомендуется есть рыбу только 1...2 раза в неделю, а беременным женщинам - вовсе ее не употреблять в пищу. Шведские специалисты по гигиене продовольствия требовали снизить допустимую концентрацию ртути в рыбе из Балтийского моря до 0,5 или даже 0,2 мг/кг, так как предел, равный 1 мг/кг, ограждает человека только от симптомов острого отравления, но не предохраняет от других тяжелых последствий поражения ртутью (например, генетических повреждений).
В водной пищевой цепи концентрация метилртути от звена к звену увеличивается, так как метилртуть растворима в жирах, она легко переходит из воды в живые организмы.
В таблице 10 приведены данные о содержании ртути в крови матерей. Уровни ртути наиболее высоки среди людей, которые едят много морепродуктов, особенно на востоке Арктики и в Гренландии. Содержание ртути в крови некоторых женщин соответствует суточным дозам поступления, близким к тем, которые могут быть причиной возможных неврологических нарушений у детей.
Таблица 10 - Уровень ртути в крови матерей
| Регион | Ртуть, мкг/л цельной крови |
| Запад Северо-западных Территорий, Канада Северная и центральная части Северо-западных Территорий, Канада Нунавик (север провинции Квебек), Канада Северо-запад Гренландии Север Швеции Север Норвегии Исландия г. Никель, Россия | 1,7 3,5 13,7 19,8 1,6 2,3 2,9 2,3 |
L Токсическая опасность ртути выражается во взаимодействии с SН-группами белков. Блокируя их, ртуть изменяет биологические свойства тканевых белков и инактивирует ряд гидролитических и окислительных ферментов. Ртуть, проникнув в клетку, может включиться в структуру ДНК, что сказывается на наследственности человека.
L Мозг проявляет особое сродство к метилртути и способен аккумулировать почти в 6 раз больше ртути, чем остальные органы. Было показано, что более 95% ртути в тканях мозга находится в органической форме. В других тканях органические соединения деметилируются и превращаются в неорганическую ртуть. В эмбрионах ртуть накапливается так же, как и в организме матери, но содержание ртути в мозге плода может быть выше.
& Так в 50-х годах в заливе Минамата в Японии районы рыбного промысла из-за промышленных выбросов были загрязнены метилртутью. Концентрация ртути в рыбе и моллюсках в этом заливе составила свыше 29 мг/кг. При употреблении такой рыбы в организм ежедневно поступало 30 мг и более. Трагедия Минаматы заключается в том, что, несмотря на загрязнение залива, меры по предотвращению дальнейшего загрязнения не были приняты и загрязнение продолжалось вплоть до 70-х годов. К февралю 1971 г. общее число случаев отравления составило 121, причем 46 - со смертельным исходом. Наблюдалось 22 случая врожденного отравления, когда у матерей, потреблявших загрязненную рыбу, рождались младенцы с мозговыми отклонениями: паралич, отставание в развитии, нарушение координации движений (больные напоминали «дышащих деревянных кукол»). Подобная эпидемия, происшедшая также в Японии на реке Агано (префектура Ниигата), привела к 49 случаям отравления, из них 6 - со смертельным исходом.
Метилртуть выводится из организма частично через почки, а в основном - через печень и желчь, а далее с фекалиями. Продолжительность выведения соединений ртути из организма - полупериод биологического их распада, по-видимому, составляет около 70 дней, однако при массовых отравлениях населения в Ираке потреблявшего семенное зерно обработанное фенилртутью оказалось, что процесс выведения ртути зависит от особенностей организма каждого человека. У 10% населения период полураспада в организме был свыше 190 дней.
Однако, отказ от питания рыбой тоже не служит надежной защитой от поступления в организм ртути, если вырабатывают рыбную муку и используют ее в качестве корма для домашних животных. Даже растительные продукты могут быть источником ртути, если к компосту добавить средство для улучшения структуры почвы, содержащее ртуть.
Таким образом, определение ртути в пищевых продуктах и других биологических объектах требует особого внимания и точности для исключения ртутного отравления организма.
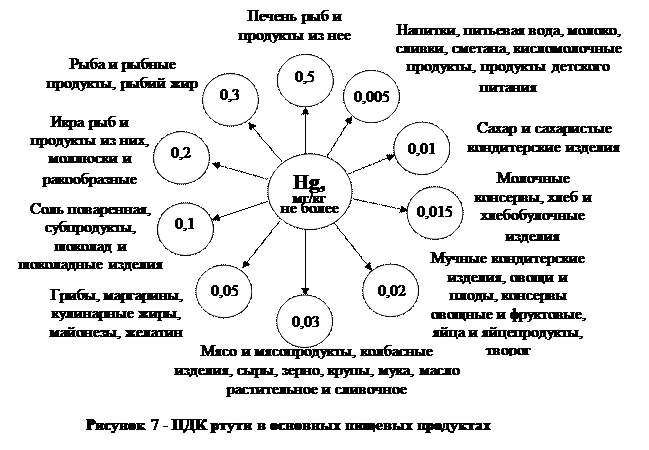
☞ Допустимое недельное поступление ртути не должно превышать 0,3 мг на человека, в том числе метилртути не более 0,2 мг, что эквивалентно 0,005 мг/кг и 0,0033 мг/кг массы тела за неделю. Более дифференцированные нормы ПДК ртути в соответствии с СанПиН 2.3.2. 1078-01 приведены на рисунке 7.
 |
|
|
|
|
|
Дата добавления: 2014-01-03; Просмотров: 511; Нарушение авторских прав?; Мы поможем в написании вашей работы!