
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Люминесцентный анализ
|
|
|
|
Явление люминесценции относится к оптической спектроскопии.
По определению С.И.Вавилова “ люминесценцией тела» в данной спектральной области называют избыток излучения над температурным при условии, что это избыточное излучение обладает конечной длительностью, превышающей период световых колебаний”.
Такое предельно сжатое и точное определение позволяет отличать люминесценцию от других видов излучения: температурного, рассеяния света (Рэлеевского и комбинационного), отражение света, излучения Вавилова-Черенкова и др., которые прекращаются непосредственно вместе с прекращением возбуждения.
Люминесцировать могут вещества, находящиеся в газообразном, жидком и твердом состоянии.
Люминесценцию классифицируют по различным признакам: a) по методу возбуждения и его характеру; б) по длительности послесвечения; в) по внутриатомным процессам при возбуждении.
Классификация люминесценции по методу возбуждения имеет большое практическое значение в реализации методик анализа. Различают фотолюминесценцию – свечение возбуждаемое ультрафиолетовым или видимым излучением; катодолюминесценцию – свечение, возникающее под действием ускоренных электронов; хемилюинесценцию – свечение, сопровождающее ряд химических реакций; рентгено- и радиолюминесценцию – свечение, возбуждаемое рентгеновскими лучами, или быстрыми частицами, такими как продукты радиоактивного распада, космические лучи.
По длительности послесвечения люминесценцию классифицируют на флуоресценцию, т.е. свечение, затухающее после прекращения возбуждения, и фосфоресценцию, свечение, продолжающееся в течение более или менее длительного промежутка времени после прекращения возбуждения.
Квант флуоресценции всегда меньше кванта возбуждения, поглощенного ратомом или молекулой на величину энергии, израсходованной на колебания, а длина волны флуоресценции больше длины волны вызывающего ее ультрафиолетового излучения (правило Стокса). Расстояние на графике между максимумами спектра поглощения и спектра люминисценсии (флуоресценции) называется Стоксовым смещением, причем спектры могут располагаться изолированно или частично перекрываться.
Светопоглощение (445 нм) и флуоресценция (535 нм) раствора рибофлавина (витамина В2).
По характеру внутриатомных процессов при возбуждении люминисценцию классифицируют на спонтанную, вынужденную и рекомбинационную.
При спонтанной люминисценции излучение возникает при возращении предварительно возбужденной молекулы (или атома) в невозбужденное состояние. Излучаемая энергия может быть равна или меньше энергии поглощенного кванта света.


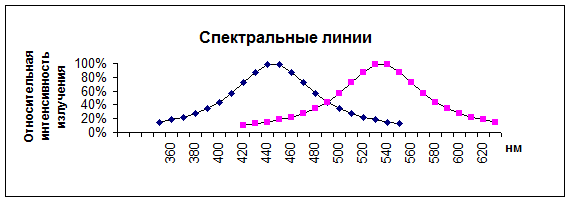
Рис. 11. Стоксово смещение
В процессе вынужденного излучения происходит переход молекулы из возбужденного состояния на промежуточный метастабильный уровень, непосредственный переход с которого на основной (невозбужденный) уровень является запрещенным (маловероятным). На метастабильном уровне молекула находится до тех пор, пока она не будет переведена вынужденным путем на энергетический уровень, переход с которого разрешен.
Длительность этих процессов свечения в значительный мере зависит от температуры. Эти явления, называемые длительным послесвечением или фосфоресценцией, характерны для органических соединений в твердых средах, замороженных и вязких растворах.
Спонтанное и вынужденное излучения, которые наиболее характерны для молекулярных систем, называют молекулярной люминесценсией.
Рекомбинационное свечение характерно тем, что при возбуждении люминесцирующего вещества не происходит перехода молекулы в возбужденное состояние (как при молекулярной люминесценсии), а происходит отрыв электронов от люминесцирующего центра с последующей рекомбинацией электронов и ионизированных центров свечения. Наблюдается рекомбинационное свечение в сложных неорганических веществах, называемых кристаллофосфорами, а также в газах.
Важнейшими характеристиками люминесцирующего вещества являются интенсивность люминесценции, спектры люминесценсии и возбуждения люминесценсии, выход люминесценции, длительность возбужденного состояния, степень поляризации, поляризационный спектр.
Интенсивность люминесценции (J) определяется как суммарное число квантов люминесценции, испускаемое единицей поверхности люминесцирующего вещества в единицу времени.
Для количественного анализа используют зависимость интенсивности люминесценции от концентрации вещества, имеющую линейный диапазон (10-4-10-7 моль/л).
При дальнейшем повышении концентрации выше пороговой сближение молекул вещества приводит к дополнительному расходу энергии на колебательное резонансное взаимодействие, вследствие чего интенсивность люминесценции падает и наступает концентрационное гашение люминесценции. Оно заметно выражено у органических окислителей. Убывание выхода люминесценции описывается соотношением:
η = ηоехр [-K(С-Сo)],
где К – постоянная;
Со – пороговая концентрация, по достижении которой начинается концентрационное гашение.
Различают и другие виды гашения. Гашение электролитами (введение посторонних веществ).
Гашение кислородом особенно сильно проявляется при свечении таких веществ, как нафталин, антрацен и др. полициклические углеводороды.
Повышение температуры люминесцирующих веществ обычно сопровождается уменьшением выхода свечения. Температурное гашение в той или иной степени проявляется у всех люминесцирующих веществ и лимитируется величиной константы скорости (β) безизлучательного перехода, определяемой формулой Больцмана:
β = βоехр (-ЕА/КТ),
где βо – постоянная, не зависящая от температуры;
К – постоянная Больцмана;
ЕА – энергия активации.
Определение концентрации вещества проводится методом построения граидуировочного графика, методом добавок.
Спектр люминесценции определяется как спектральная плотность излучения люминесцирующего вещества.
Φλ = dΦ/dλ; Φhν = dΦ/d(hυ), nhυ= dn/d(hυ),
где Φ – мощность излучения;
n ‑ число квантов, испускаемых в единицу времени,
hυ ‑ энергия испускаемых квантов,
λ ‑ длина волны.
Спектром возбуждения люминесценции называют зависимость интенсивности люминесценции от энергии квантов (или длины волны) возбуждающего света.
Эффективность процессов преобразования поглощенной в молекулах энергии в излучаемую характеризуется выходом люминесценции, под которым понимают отношение энергии (т.е. мощности или интенсивности излучения Φλ), к энергии поглощаемой веществом за то же время (т.е. к мощности поглощения ΦА):
η = Φλ/ΦА
Энергия возбуждающего света и света люминесценции может измеряться либо в энергетических единицах, например, в джоулях, либо в числах квантов.
Понятие квантового выхода используют только в случае оптического возбуждения.
Квантовый выход люминесценции определяется как отношение числа квантов люминесценции, используемых веществом за единицу времени (nл), к числу квантов возбуждающего света, поглощаемых им за то же время (nп):
η кв = nл/ nп
Квантовый выход люминесценции, как правило, меньше единицы вследствии наличия тушения люминесценции (наличия безизлучательных переходов).
При наличии N возбужденных молекул число квантов люминесценции, испускаемых веществом за единицу времени равно αN (α – константа скорости излучательного перехода – вероятность излучательного перехода молекулы).
Число квантов возбуждающего света, поглощаемых веществом за то же время равно (α + β)N (β – вероятность безизлучательного перехода).
Поэтому квантовый выход люминесценции определяется соотношением:
ηкв. = λN/(α+β)N = α(α + β)
В случае отсутствия безизлучательных переходов β =0 и ηкв.=1
Однако, чаще всего часть энергии возбуждающего света тратится на развитие безизлучательных переходов, что приводит к тушению люминесценции.
Вещества, обладающие молекулярным свечением, подчиняются экспоненциальному закону затухания (изменение интенсивности свечения J со временем t после прекращения возбуждения):
J = Joexp [-(t/τ)],
где Jo – интенсивность свечения в начальной период затухания;
τ – естественная длительность возбужденного состояния.
Длительность свечения является одним из основных признаков люминесценции, а законы затухания имеют важное значение для исследования кинетики свечения.
Поляризованной люминесценцией, называется свечение, у которого амплитуды колебаний светового вектора по двум направлениям, взаимно перпендикулярным направлению распространения лучей, неодинаковы. Степень поляризации люминесценции зависит от природы элементарных излучателей, способа возбуждения, а также от различных деполяризующих факторов.
Зависимость степени поляризации люминесценции от длины волны называется поляризационными спектром.
Поляризационный спектр каждого соединения является индивидуальным, что позволяет использовать его для качественного анализа.
Люминесцентный анализ используется для определения в пищевых продуктах целого ряда люминесцирующих компонентов: ароматических аминокислот, полиненасыщенных жирных кислот, и продуктов их окисления, витаминов и т.п.
Вопросы
1. В чем заключается понятие оптической спектроскопии, ее классификация.
2. Основные положения квантовой, корпускулярной теории поглощения, излучения атомами электромагнитных волн.
3. Как определяется полная энергия молекулы?
4. Приведите примеры батохромного, гипсохромного сдвига спектра поглощения.
5. В чем заключается сущность спектрофотометрического метода анализа?
6. Что такое оптическая плотность раствора?
7. Какие факторы влияют на величину оптической плотности раствора?
8. Что такое спектр поглощения?
9. Какие явления вызывают отклонения от закона Бугера-Ламберта-Бера?
10. В чем заключается сущность метода атомно-абсорбционной спектрометрии; его отличия от спектрофотометрического метода?
11. Каковы преимущества атомно-абсорбционного метода анализа?
12. В чем заключается сущность и классификация люминесцентного метода анализа?
Практические задания
1. Выберите выражение общей скорости распространения электромагнитных волн.
а) V = c/εμ;
б) V = c 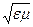
2. По какой формуле можно рассчитать энергию излучения или поглощения атомами электромагнитных волн.
а) h·υmn =  ;
;
б) h·υmn = Em- En
3. По какой формуле определяется частота излучения молекулами света
а) υ = (Еm - En)/h = (Em(эл) – En(эл))/h + (Em(кол) – Еn(кол))/h + (Em(вр) – Еn(вр))/h;
б) υ = (Em + En)·h = (Em(эл) – En(эл))·h – (Em(кол) – En(кол))·h – (Em(вр) – En(вр))·h
4. Какое математическое выражение соответствует объединенному закону Бугера–Ламберта–Бера.
а) Фλ = Φоλ exp(-xoλ cl);
б) Фλ = Φоλ/exp(xoλ cl)
5. Зависимость между какими величинами выражает спектр поглощения?
а) С от λ;
б) D от λ
6. При спектрофотометрическом исследовании аммиачного раствора меди величина оптической плотности оказалась равной 1,20 при толщине исследуемого слоя раствора 30 мм. Молярный коэффициент поглощения 423. Вычислить концентрацию меди в растворе в мкг/мл.
а) 6,048;
б) 60,48
7. Вычислить молярный коэффициент поглощения раствора комплексного соединения железа с роданидом аммония. Величина оптической плотности раствора равна 1,13; при толщине исследуемого слоя раствора 20 мм. Масса железа, используемого для получения раствора, равна 3,136 мг.
а) 5;
б) 500
8. Как рассчитать в спектрофотометрическом методе анализа концентрацию исследуемого раствора (Сх) по методу добавок.
а) Сх = Са∙Dх/(Dх+а-Dх);
б) Сх = Са∙Dх∙(Dх+а-Dх)
9. Что используют в методе атомно-абсорбционного анализа для получения характеристического резонансного излучения?
а) лампы с полым катодом;
б) стабилизаторы
10. В чем заключается правило Стокса?
а) длина волны флуоресценции больше длины волны вызывающего ее ультрафиолетового излучения;
б) длина волны флуоресценции меньше длины волны вызывающего ее ультрафиолетового излучения
11. Каков линейный диапазон концентрации вещества в люминесцентном методе анализа?
а) 10-4-10-2 моль/л;
б) 10-7-10-4 моль/л
12. По какой формуле рассчитывается квантовый выход люминесценсии?
а) ηкв = λN/(α + β)N;
б) ηкв = λ/N(α + β).
Примеры решения задач
1. При определении биогенного микроэлемента в пищевом объекте фотоэлектроколориметрическим методом величина оптической плотности раствора, полученного после соответствующей обработки исследуемого объекта, оказалась равной 1,25. Объем полученного раствора составил 500 см3. Толщина исследуемого слоя раствора равна 20 мм. Молярный коэффициент поглощения равен 928. Определить содержание микроэлемента в полученном растворе в моль/л.
а) 6,73∙10-4
б) 6,73∙10-5
|
|
|
|
|
Дата добавления: 2017-01-14; Просмотров: 1257; Нарушение авторских прав?; Мы поможем в написании вашей работы!