
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Площадь занимаемая одной молекулой азота в адсорбционном слое 0,16 нм2
|
|
|
|
11. По изотерме адсорбции азота определить удельную поверхность адсорбента
(Т=77 К, S0=16,2·10-20 м2). (Варианты 1-5).
1. Р/Рs ………. 0,04 0,09 0,16 0,20 0,30
А, моль/кг….2,20 2,62 2,94 3,11 3,58
2. Р/Рs …………0,029 0,05 0,11 0,14 0,20
А, моль/кг………..2,16 2,39 2,86 3,02 3,33
3. Р/Рs ………….0,02 0,04 0,08 0,14 0,16 0,18
А, моль/кг………..1,86 2,31 2,72 3,07 3,12 3,23
Для следующих двух вариантов объем адсорбированного газа приведен к нормальным условиям:
4. Р/Рs …………….…0,05 0,10 0,15 0,20 0,25 0,30
А ·102 м3/кг……………..0,70 1,10 1,17 1,32 1,45 1,55
5. Р/Рs……………….0,029 0,05 0,11 0,14 0,18 0,20
А ·102 м3/кг……..……..0,48 0,54 0,64 0,68 0,72 0,75
12. По изотерме адсорбции бензола определить удельную поверхность
адсорбента. Т=293 К, S0=49•10-20 м2. Объем адсорбированного газа приведен к нормальным условиям (варианты 1-4):
1. Р/Рs…………………….0,05 0,10 0,15 0,20 0,25 0,30
А·102, м3/кг………………..0,86 1,20 1,40 1,60 1,80 1,90
2. Р/Рs…………………….0,10 0,15 0,20 0,25 0,30 0,35
А·102, м3/кг……….………..1,15 1,37 1,55 1,71 1,86 1,99
3. Р/Рs…………………….0,10 0,15 0,20 0,25 0,30 0,35
А·102, м3/кг………………..0,89 1,09 1,27 1,45 1,60 1,78
4. Р/Рs…………………….0,08 0,16 0,25 0,35 0,45 0,52
А·102, м3/кг………..… ……1,03 1,37 1,70 1,99 2,44 2,82
13. По изотерме адсорбции бензола определить удельную поверхность
адсорбента. Т=293 К, S0=49·10-20 м2(варианты 1-3).
1. Р/Рs ……………..0,05 0,10 0,15 0,20 0,30 0,40
А, моль/кг…...………0,36 0,51 0,60 0,68 0,82 0,98
2. Р/Рs …………...….0,06 0,12 0,20 0,30 0,40 0,50
А, моль/кг…...………..0,08 0,16 0,25 0,35 0,45 0,52
3. Р/Рs …………...….0,46 0,61 0,76 0,89 1,09 1,26
14. Построить изотерму адсорбции нитролигнина на глине и определить константы уравнения Фрейндлиха по следующим экспериментальным данным:
Концентрация водного раствора нитролигнина
С, %………………………….0,12 0,24 0,44 0,65 0,98 1,2
Величина адсорбции
Г· 103, кг/кг……………………5,0 12,0 21,0 26,0 35,0 38,0.
15. Пользуясь экспериментальными данными ионного обмена ионов кальция (Г1с1) и натрия (Г2с2) на синтетическом катионите, определить графически константу уравнения Никольского К:

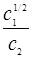 в растворе…………….0,2 0,3 0,4 0,5 0,6 0,8
в растворе…………….0,2 0,3 0,4 0,5 0,6 0,8
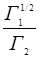 на сорбенте…………..0,75 1,0 1,5 1,8 2,4 3,1.
на сорбенте…………..0,75 1,0 1,5 1,8 2,4 3,1.
16. Пользуясь константами уравнения Фрейндлиха k=4,17·10-3, 1/n=0,4, рассчитать и построить изотерму адсорбции углекислого газа на угле для следующих интервалов давления: 100·102, 200·102, 400·102, 500·102 Н/м2.
17. Пользуясь константами уравнения Фрейндлиха k=3,2·10-3, 1/n=0,6 построить кривую адсорбции углекислого газа на угле в интервале давлений от 5·102 до 25·102 Н/м2.
18. По данным сорбции углекислого газа на угле построить изотерму адсорбции и определить константы изотермы адсорбции Фрейндлиха:
Равновесное давление
Р ·10-2, Н/м2……………..5,0 10,0 30,0 50,0 75,0 100,0
Величина сорбции
Г ·103, кг/кг……………..30, 5,5 16,0 23,0 31,0 35,0.
19. При изучении реакций обмена Mg-ионов из чернозема с ионами Ca из внесенных минеральных удобрений получены следующие результаты:
Концентрация ионов в растворе Количество сорбированных катионов
С ·103, кмоль/м3 Г ·105,кмоль/кг
Mg Ca Mg Ca
2,41 4,75 8,12 42,88
2,25 5,00 7,70 43,30
2,00 5,10 6,90 44,10
1,84 5,50 6,10 44,90
1,53 5,87 4,54 46,46
1,37 5,99 4,12 46,88
Графическим методом определить константу уравнения Никольского.
20. Оределить константу уравнения Никольского К, используя экспериментальные данные реакций обмена ионов Ca из почвы на ионы Na из раствора натриевой соли.
Концентрация ионов в растворе Na…3,26 6,60 13,80 21,25 38,41 65,19
С ·103, кмоль/м3 Ca.…37,84 36,72 34,62 31,87 26,16 17,10
Количество сорбированных Na….0,28 0,60 1,20 1,89 3,18 7,62
ионов Г ·105, кмоль/кг Ca…39,72 39,56 39,40 38,93 38,68 37,40
21. Пользуясь экспериментальными данными реакций обмена ионов ионов Na из раствора натриевой соли на ионы Mg из почвы, определить графически константу уравнения Никольского:
Концентрация ионов в растворе Количество сорбированных ионов
С·103,кмоль/м3 на почве Г.105, кмоль/кг
Na Mg Na Mg
13,82 41,92 1,16 25,40
21,25 38,30 1,89 26,13
38,19 31,90 3,62 27,20
65,0 21,14 8,01 29,32
79,25 14,73 11,66 32,84
22. Используя экспериментальные данные адсорбции анилина из его водного раствора на угле, определить графически константы уравнения Лэнгмюра и построить изотерму адсорбции для следующих с1:
C1· 104, кмоль/м3……………………3 5 10 15 20
Концентрация раствора
анилина с·104, кмоль/м …………1,0 4,0 7,5 12,5 17,5
Величина сорбции
А ·109,кмоль/м2 …………….……0,3 0,58 0,70 0,87 0,92
23. По экспериментальным данным построить кривую адсорбции углекислого газа на цеолите при 293º и с помощью графического метода определить константы уравнения Лэнгмюра:
Равновесное давления
Р· 10-2, н/м2……………….1,0 5,0 10,0 30,0 75,0 100,0 200,0
Величина адсорбции
А· 103, кг/кг………………35,0 86,0 112,0 152,0 174,0 178,0 188,0
24. Используя уравнение Лэнгмюра, вычислить величину адсорбции азота на цеолите при давлении р =2,8·102, если А∞= 38,9·10-3 кг/кг, а k =0,156·10-2.
25. Найти площадь, приходящуюся на одну молекулу в насыщенном адсорбционном слое анилина на поверхности его водного раствора, если предельная адсорбция А∞ =6,0·10-9 кмоль/м
26. По экспериментальны данным адсорбции углекислого газа на активированном угле, найти константы уравнения Лэнгмюра, пользуясь которыми рассчитать и построить изотерму адсорбции:
Равновесное давление
P ·10-2, Н/м2……………..9,9 49,7 99,8 200,0 297,0 398,5
Величина адсорбции
Г ·103, кг/кг……………..32,0 70,0 91,0 102,0 107,3 108,0.
27. По константам уравнения Лэнгмюра А∞ =182·10-3 и k =0,1·10-2 рассчитать и построить изотерму адсорбции углекислого газа на активированном угле в пределах следующих равновесных давлений газа: 10·102 – 400·102 Н/м.
28. Построить кривую адсорбции углекислого газа на активированном угле при 231º и определить константы эмпирического уравнения Фрейндлиха, пользуясь следующими экспериментальными данными:
Равновесное давление
Р ·10-2, Н/м2………………10,0 44,8 100,0 144,0 250,0 452,0
Величина адсорбции
А ·103, кг/кг……………….32,3 66,7 96,2 117,2 145,0 177,0.
29. Используя константы эмпирического уравнения Фрейндлиха k =1,6·10-3 и 1/n =0,48, построить кривую адсорбции углекислого газа на активированном угле при 271º в интервале давлений от 2·102 до 30·102 Н/м2.
30. Определить постоянные эмпирического уравнения Фрейндлиха, используя следующие данные для адсорбции при 231К углекислого газа на угле из коксовой скорлупы:
Р, Па·10-3……………….1,000 4,480 10,000 14,40 25,0 45,2
А, кг/кг·102………………3,23 6,67 9,62 11,72 14,5 17,7.
31. Вычислите площадь поверхности катализатора, если для образования монослоя на нем должно адсорбироваться 103 см3/г азота (объем приведен к 760 мм рт.ст. и 0ºС). Адсорбция измеряется при температуре 195ºС. Эффективная площадь, занимаемая молекулой азота при этой температуре, равна 16,2 А2.
32.Площадь поверхности 1 г активированного угля равна 1000 м2. Какое количество аммиака может адсорбироваться на поверхности 45 г угля при 45ºС и 1 атм, если принять в качестве предельного случая полное покрытие поверхности? Диаметр молекулы аммиака равен 3·10-10 м. Принимается, что молекулы касаются друг друга так, что центры четырех соседних сфер расположены в углах квадрата.
33. Ниже представлены данные по хемосорбции водорода на порошке меди при 25ºС. Подтвердите, что они подчиняются изотерме Ленгмюра. Затем найдите значение К для адсорбционного равновесия и адсорбционный объем, соответствующий полному покрытию.
Р, мм рт ст…………………..0,19 0,97 1,90 4,05 7,5 11,95
Vа, см3……………………….0,042 0,163 0,221 0,321 0,411 0,471.
34. Определите, какая изотерма – Лэнгмюра или Фрейндлиха – лучше соответствует данным для адсорбции метана на 10 г сажи при 0ºС, приведенным ниже:
Р, мм рт ст …………….100 200 300 400
Va, см3………………….97,5 144 182 214.
Глава 6. Электрокинетические явления в дисперсных системах
Электрокинетические явления, наблюдаемые в дисперсных системах, представляют собой либо относительное смещение фаз под действием внешнего электрического поля (электроосмос, электрофорез), либо возникновение разности потенциалов в направлении относительного движения фаз, вызываемого гидродинамическими силами (потенциал течения, потенциал седиментации).
Электроосмос и электрофорез были обнаружены в 1808г. Ф.Ф. Рейсом, потенциал течения ¾ в 1859г. Г. Квинке, потенциал седиментации ¾ в 1878г. Е. Дорном.
|
|
|
|
|
Дата добавления: 2015-08-31; Просмотров: 3503; Нарушение авторских прав?; Мы поможем в написании вашей работы!