
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Растворенного вещества
|
|
|
|
Техника приготовления раствора с заданной массовой долей
Массовой долей растворенного вещества
Опыт 1. Приготовление раствора хлорида натрия с заданной
Приготовление растворов
Лабораторная работа № 1
Цель: освоение навыков в приготовлении растворов заданной концентрации.
Вопросы и упражнения для самоподготовки к лабораторной работе
1. Что такое растворы?
2. Что такое насыщенные, ненасыщенные растворы?
3. Что называется массовой долей растворенного вещества? По каким формулам можно рассчитать массовую долю растворенного вещества; массу раствора?
4. Что называется молярной концентрацией? По какой формуле можно рассчитать молярную концентрацию раствора?
5. Каков порядок действия при приготовлении растворов с массовой долей растворенного вещества и молярной концентрации?
6. 200 г морской воды выпарили, получили 8 г осадка. Какова массовая доля солей в морской воде?
7. К 300 г 15%-ного раствора соли добавили 50 г воды. Какова массовая доля полученного раствора?
8. Определить молярную концентрацию раствора, содержащего 14 г гидроксида калия в 500 мл раствора
9. Какая масса (г) KNO3 содержится в 2 л 0,1 М KNO3?
Оборудование. Весы учебные с разновесом. Колба коническая (100 мл). Колба мерная (250 мл). Воронка химическая. Промывалка. Ареометр тяжелее воды. Цилиндр для определения плотности. Палочка стеклянная.
Реактивы. Хлорид натрия. Карбонат натрия, десятиводный.
Для приготовления ________ г. раствора хлорида натрия с массовой
долей ω (NaCl) = ________ % рассчитать:
массу хлорида натрия, m (NaCl) = ______________________________
________________________________________________________________
массу воды, m (H2O) = _______________________________________
объем воды (ρ = 1 г/см3), V (H2O) =_____________________________
________________________________________________________________
Таким образом, для приготовления ________ г раствора хлорида натрия с массовой долей ω (NaCl) = _________ % потребуется __________ г
хлорида натрия и ________ см3 воды.
1. Взвесить рассчитанную массу (навеску) растворяемого вещества на весах.
2. Высыпать навеску в колбу.
3. Измерить мерным цилиндром рассчитанный объем дистиллированной воды.
4. Вылить воду из цилиндра в колбу с растворяемым веществом.
5. Перемешать раствор стеклянной палочкой до полного растворения вещества.
6. Измерить температуру приготовления раствора и, если она не равна температуре, которая указана в приложении 2, довести ее до указанной величины, нагревая или охлаждая раствор.
Измерить плотность полученного раствора. Для этого вылить раствор в сухой (или ополоснутый этим раствором) высокий узкий цилиндр и опустить в него ареометр так, чтобы он не касался стенок сосуда. Отметить то деление шкалы, которая совпадает с уровнем жидкости в цилиндре, производя отчет по шкале сверху вниз. Записать значение плотности приготовленного раствора хлорида натрия ρопыт. (NaCl) = ________г/см3. Найти плотность хлорида натрия (Приложение №1) и записать его значение ρтабл. (NaCl) = ________ г/см3.
Рассчитать абсолютную погрешность: ∆ = 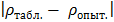
∆ =  =
=
Рассчитать относительную погрешность: ε =  ∙ 100%
∙ 100%
ε =  ∙ 100% =
∙ 100% =
Вывод: _____________________________________________________
________________________________________________________________________________________________________________________________
|
|
|
|
|
Дата добавления: 2017-02-01; Просмотров: 94; Нарушение авторских прав?; Мы поможем в написании вашей работы!