
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Сушка влажных материалов
|
|
|
|
Задачи
Примеры
Методические указания
Изучение процессов перегонки и ректификации следует начать с рассмотрения диаграмм состояния жидких бинарных смесей. Обратите внимание на диаграммы состояния, имеющие точки перегиба, характеризующие нераздельно кипящие смеси, разделение которых производится специальными методами. Затем необходимо ознакомиться с методами простой перегонки и научиться составлять материальные и тепловые балансы.
Особое внимание следует уделить рассмотрению процессов многократной перегонки-ректификации. Нужно ознакомиться с принципами работы ректификационной установки непрерывного и периодического действия, разобрать материальный баланс процесса ректификации и изучить уравнения концентраций (рабочих линий) для верхней и нижней частей колонны, выяснить влияние флегмы и расхода смеси на работу ректификационной колонны, научиться рассчитывать теоретическое и действительное число ступеней (тарелок) графическим методом.
Уясните гидравлические явления и явления тепло-массообмена, протекающие на тарелках, и влияние отдельных факторов на величину КПД тарелки. Необходимо рассмотреть методы расчета основных размеров тарельчатых и насадочных ректификационных колонн. Ознакомьтесь с методами азеотропной и экстрактивной ректификации.
Пример 3.3.1. Определить равновесные составы жидкости и пара для смеси метиловый спирт-вода при температуре t и давлении П.
РЕШЕНИЕ
Принимаем, что смесь метилового спирта в воде является идеальным раствором. Идеальные растворы следуют законам Рауля и Дальтона. Согласно закону Рауля, парциальное давление каждого компонента, например, низкокипящего компонента А в паре рА, пропорционально мольной доле хА этого компонента в жидкости.
Для бинарной смеси, состоящей из компонентов А (метиловый спирт) и В (вода), по закону Рауля
рА = хА . 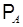 , ,
| (3.11) |
где 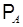 – коэффициент пропорциональности, равный давлению насыщенного пара компонента А над чистой жидкостью при данной температуре t.
– коэффициент пропорциональности, равный давлению насыщенного пара компонента А над чистой жидкостью при данной температуре t.
рВ = хВ . 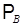 = (1 – хА) . = (1 – хА) . 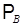 , ,
| (3.12) |
где хА + хВ = 1 (для бинарной смеси); хВ – мольная доля компонента В, давление насыщенного пара которого над чистой жидкостью при данной температуре t равно 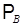 .
.
Согласно закону Дальтона общее давление пара над раствором П равно сумме парциальных давлений его компонентов
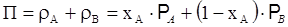 . .
| (3.13) |
Решая зависимость (3.13) относительно хА, получим
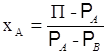 . .
| (3.14) |
Значения 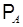 и
и 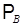 при данной температуре t определяем из справочной литературы, например [4].
при данной температуре t определяем из справочной литературы, например [4].
Вместе с тем, согласно второму закону Дальтона (при условии применимости к парам каждого из компонентов уравнения состояния газа) парциальное давление рА данного компонента А пропорционально его мольной доле уА в паре:
| рА = П . уА, | (3.15) |
где П – общее давление пара над смесью.
Тогда, из (3.11) и (3.15) зависимость между составами равновесных жидкой и паровой фаз будет равна
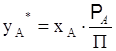 . .
| (3.16) |
Пример 3.3.2. Gf кг бинарной смеси бензол-толуол, содержащей 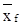 бензола, подвергают простой перегонке под атмосферным давлением. Определить количество и состав дистиллята, если содержание бензола в кубовом остатке равно
бензола, подвергают простой перегонке под атмосферным давлением. Определить количество и состав дистиллята, если содержание бензола в кубовом остатке равно 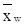 . Воспользоваться данными таблицы 17.
. Воспользоваться данными таблицы 17.
Таблица 17 – Равновесие между жидкостью и паром бинарной смеси бензол-толуол
| t, °С | 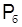 ,
мм рт.ст. ,
мм рт.ст.
| 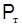 ,
мм рт.ст. ,
мм рт.ст.
| П, мм рт.ст. | 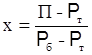
| 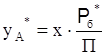
|
| 300,0 | |||||
| 333,0 | 0,823 | 0,922 | |||
| 379,5 | 0,669 | 0,830 | |||
| 432,0 | 0,508 | 0,720 | |||
| 492,5 | 0,376 | 0,596 | |||
| 559,0 | 0,256 | 0,453 | |||
| 625,5 | 0,155 | 0,304 | |||
| 704,5 | 0,058 | 0,128 | |||
| 760,0 |
РЕШЕНИЕ
Для решения задачи используем уравнение материального баланса простой перегонки
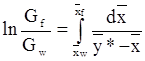 . .
| (3.17) |
где Gf – начальное количество перегоняемой смеси, кг;
Gw – остаток жидкости в кубе после перегонки, кг;
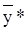 и
и 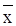 - равновесные концентрации низкокипящего (бензола) компонента в паре и в жидкости, масс. доли;
- равновесные концентрации низкокипящего (бензола) компонента в паре и в жидкости, масс. доли;
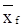 ,
, 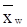 – массовое содержание низкокипящего компонента в начальной смеси и в остатке после перегонки, доли.
– массовое содержание низкокипящего компонента в начальной смеси и в остатке после перегонки, доли.
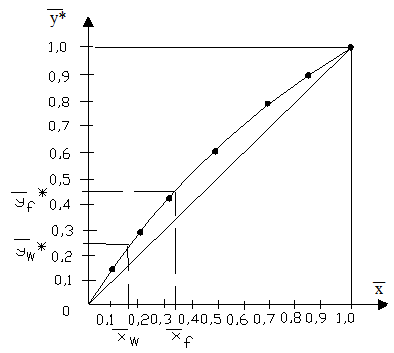
|
| Рис. 11 – К примеру 3.3.2. |
Так как данные по равновесию бинарной смеси бензол-толуол (табл. 17) приведены в мольных долях, а в условии задачи 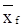 ,
, 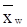 приведены в массовых долях, выполним пересчет мольных долей в массовые по формуле
приведены в массовых долях, выполним пересчет мольных долей в массовые по формуле
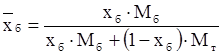
| (3.18) |
и 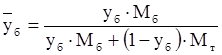
| (3.19) |
где 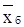 ,
, 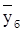 – массовые концентрации бензола в жидкой и паровой фазах, соответственно, доли;
– массовые концентрации бензола в жидкой и паровой фазах, соответственно, доли;
Мб, Мт – мольные массы бензола и толуола.
По пересчитанным данным строим диаграмму 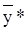 -
- 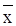 (рис. 11).
(рис. 11).
Интеграл уравнения (3.17) решаем графически. Для этого строим график зависимости 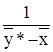 от
от 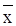 для бензольно-толуольной смеси (рис. 12).
для бензольно-толуольной смеси (рис. 12).
Для ряда значений 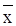 в пределах от
в пределах от 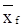 до
до 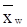 находим из диаграмм
находим из диаграмм 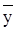 -
- 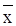 (рис. 11) равновесные им значения
(рис. 11) равновесные им значения 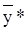 и по размеру площади под кривой, ограниченной абсциссами
и по размеру площади под кривой, ограниченной абсциссами 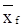 и
и 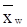 , определяем (с учетом масштабов диаграммы) величину искомого интеграла.
, определяем (с учетом масштабов диаграммы) величину искомого интеграла.
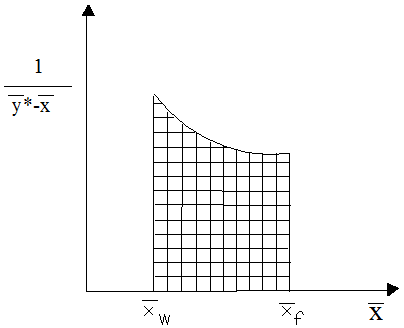
|
| Рис. 12 – К примеру 3.3.2. |
По уравнению (3.17) находим количество остатка Gw.
Средний состав (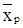 )ср получаемого дистиллята рассчитываем по уравнению
)ср получаемого дистиллята рассчитываем по уравнению
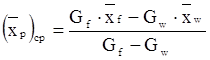 . .
| (3.20) |
Пример 3.3.3. В ректификационную колонну непрерывного действия поступает жидкость F кмоль/ч с хf легколетучего компонента. Концентрация дистиллята хр, концентрация кубового остатка хw легколетучего компонента. В дефлегматор поступает Gy кмоль/ч пара, в колонну из дефлегматора поступает Ф кмоль/ч флегмы. Сколько получается кубового остатка.
РЕШЕНИЕ
Используем уравнения материального баланса ректификационной колонны
| F = P + W | (3.21) |
и материального баланса по низкокипящему компоненту:
| F . хf = P . хp + W . хw, | (3.22) |
где F – количество исходной смеси, поступающей в колонну, кмоль/ч;
Р – количество получаемого дистиллята, кмоль/ч;
W – количество удаляемого из колонны остатка, кмоль/ч;
хf, хp и хw – состав исходной смеси, дистиллята и кубового остатка, соответственно, мольных долей НК.
Решая совместно уравнения (3.21) и (3.22) получим:
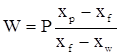 , ,
| (3.23) |
где Р = Gy – Ф; Ф – количество флегмы, возвращаемой в колонну после дефлегматора на орошение верхней части колонны и укрепления паров, поступающих в дефлегматор, причем ее состав равен составу дистиллята (хф = хр мол. долей).
Пример 3.3.4. В ректификационную колонну непрерывного действия подается F кмоль/ч смеси, содержащей хf мольных долей НК. Верхний продукт содержит хр, нижний – хw мольных долей НК. Определить количество верхнего и нижнего продуктов (в кг/ч), а также количество пара, конденсирующегося в дефлегматоре, если известно, что тангенс угла наклона рабочей линии верхней (укрепляющей) части колонны равняется 0,75.
РЕШЕНИЕ
1) Количество нижнего продукта (кубового остатка) можно определить, используя уравнение материального баланса (3.21) и (3.22):
F = P + W
F . хf = P . хp + W . хw.
Далее F . хf = W . хw + F . хp + W . хр.
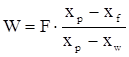 ;
;
где W – количество нижнего продукта, кмоль/ч.
Gw = W . Mw, кг/ч.
Mw – мольная масса кубового остатка, кг/кмоль.
Mw = MA . хw + MB (1 – хw), кг/кмоль.
MA, MB – мольные массы компонентов А и В бинарной смеси, кг/кмоль.
2) Для определения массового количества верхнего продукта (дистиллята), выразим мольное количество подаваемой смеси F в единицах массового расхода по формуле:
Gf = F . Mf, кг/ч.
где Mf – мольная масса исходной смеси, кг/кмоль.
Mf = MA . хf + MB (1 – хf), кг/кмоль.
Тогда, количество верхнего продукта Gp, будет равно
Gp = Gf – Gw.
3) Количество пара Gу, конденсирующегося в дефлегматоре, равно
| Gу = Gф + Gp = R . Gp + Gp = Gp (R + 1), | (3.24) |
где Gф – количество флегмы, кг/ч; R = Gф / Gp – флегмовое число, представляющее собой отношение количества возвращаемой в колонну после дефлегматора жидкости к количеству отбираемого верхнего продукта (дистиллята).
Для определения флегмового числа R воспользуемся уравнением рабочей линии верхней части колонны:
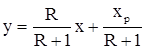 , ,
| (3.25) |
где у и х – рабочие (текущие) концентрации низкокипящего компонента в паровой и жидкой фазах верхней части колонны, мольные доли.
Уравнение (3.25) представляет собой уравнение прямой линии вида
у = А . х + В,
которая наклонена к горизонту под углом, тангенс которого равен 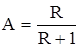 , и отсекает на оси ординат отрезок, равный
, и отсекает на оси ординат отрезок, равный 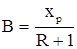 .
.
По условию задачи известно, что тангенс угла наклона рабочей линии верхней части колонны равен 0,75, т.е.
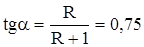 . .
| (3.26) |
Решая (3.26) относительно R, получим R = 3. Тогда,
Gу = Gp (3 + 1), кг/ч.
Пример 3.3.5. Уравнения рабочих линий ректификационной колонны для разделения смеси бензола и толуола под атмосферным давлением:
у = 0,723 х + 0,263;
у = 1,25 х - 0,0188.
В колонну подается F кмоль/ч смеси при температуре кипения. Греющий пар в кубе колонны имеет избыточное давление 3 кгс/см2. Определить требуемую поверхность нагрева в кубе колонны и расход греющего пара, имеющего влажность 5%. Коэффициент теплопередачи К = 580 Вт/ (м2 . К). Тепловыми потерями пренебречь. Температуру кипения жидкости в кубе принять как для чистого толуола.
РЕШЕНИЕ
1) Требуемую поверхность нагрева в кубе колонны определяем на основе уравнения теплопередачи:
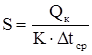 . .
| (3.27) |
где S – площадь поверхности нагрева в кубе колонны, м2;
К – коэффициент теплопередачи, Вт/ (м2 . К);
Δtcp – средняя разность температур, °С;
Qк – расход теплоты, получаемой кипящей жидкостью от конденсирующегося греющего пара в кубе-испарителе, Вт.
Из уравнения теплового баланса колонны с дефлегматором-конденсатором:
| Qк = Gp . (R + 1) . rp + Gp . Cp . tp + Gw . Cw . tw – Gf . Cf . tf + Qпот, | (3.28) |
где Gf, Gp, Gw – массовые расходы питания, дистиллята, кубового остатка, кг/с;
Сf, Сp, Сw – средние удельные теплоемкости, Дж/(кг . К);
tf, tp, tw – температуры кипения исходной смеси, дистиллята и кубового остатка, соответственно, °С;
R – число флегмы;
rp – удельная теплота конденсации паров в дефлегматоре, Дж/кг;
Для определения величины каждого слагаемого уравнения (3.28) используем приведенные в условии задачи уравнения рабочих линий ректификационной колонны.
Из уравнения рабочей линии
у = 0,723 х + 0,263
следует, что 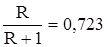 . Откуда, R = 2,6.
. Откуда, R = 2,6.
Далее, 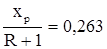 .
.
При R = 2,6 получим хр = 0,95.
Состав исходной смеси определим как точку пересечения рабочих линий:
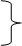 уf = 0,723 хf + 0,263
уf = 0,723 хf + 0,263
уf = 1,25 хf - 0,0188
или
0,723 хf + 0,263 = 1,25 хf - 0,0188.
Откуда, хf = 0,535.
Состав кубового остатка определим, используя аналитическое выражение уравнения рабочей линии нижней части ректификационной колонны:
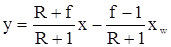 , ,
| (3.29) |
где 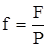 - относительный (на 1 кмоль дистиллята) мольный расход питания.
- относительный (на 1 кмоль дистиллята) мольный расход питания.
Из условия задачи следует, что уравнение рабочей линии нижней части колонны имеет вид
у = 1,25 х – 0,0188.
Из сравнения этого уравнения с уравнением (3.29) следует
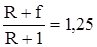 .
.
При R = 2,6, получим f = 1,9.
Далее, 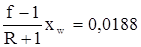 .
.
Решая это выражение относительно хw, получим хw = 0,075.
Зная мольный расход исходной смеси F и ее состав хf, определим массовый расход Gf:
Gf = F . Mf, кг/ч
где Mf = Mб . хf + Мт (1 – хf); Mб, Мт – мольные массы бензола и толуола, кг/кмоль.
Тогда, 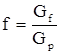 ,
,
где Gp – массовый расход дистиллята, кг/ч.
Gp = Gf / 1,9.
Из уравнения материального баланса колонны определим массовый расход кубового остатка
Gw = Gf – Gp.
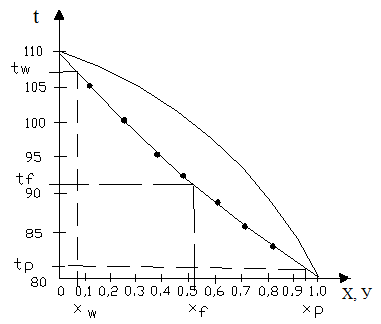
Используя опытные данные по равновесию между жидкостью и паром смеси бензол-толуол (табл. 16) строим диаграмму в координатах t – x, y (рис. 13).
|
| Рис. 13 – Диаграмма t – x, y. |
Из диаграммы t – x, y, определяем температуры tw, tf, tp.
Для определения удельных теплоемкостей бензола Ср и толуола Сw (принимаем дистиллят и кубовый остаток как чистые бензол и толуол, соответственно при температурах tp и tw). Удельную теплоту конденсации паров в дефлегматоре rp, определяем из справочной литературы [4] или по таблице 11.
Удельную теплоемкость исходной смеси Сf определяем по формуле
Сf = Сб . 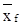 + Ст (1 – + Ст (1 – 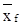 ), ),
| (3.30) |
где Сб, Ст – удельные теплоемкости бензола и толуола при температуре tf, Дж/(кг . К);
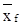 – массовая доля бензола (низкокипящего компонента) в исходной смеси.
– массовая доля бензола (низкокипящего компонента) в исходной смеси.
Подставив значения всех полученных величин в уравнение (3.28), определяем Qк.
Для определения средней разности температур используем формулу (2.9)
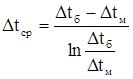 ,
,
где Δtб и Δtм определяем из температурной схемы.
 143 143
143 143
 98 98
98 98
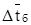 = 45 °С.
= 45 °С. 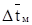 = 45 °С.
= 45 °С.
Так как, 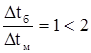 , то можно
, то можно
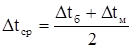 = 45 °С.
= 45 °С.
В приведенной температурной схеме цифры:
143 – температура конденсации водяного пара при давлении Рабс = 4 кгс/см2;
98 – температура кипения (парообразования) толуола.
Подставив в формулу (3.27) значения Qк, К и Δtср определяем требуемую поверхность нагрева в кубе колонны S.
2) Расход греющего пара определяем по уравнению (2.2):
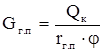 ,
,
где rг.п – удельная теплота конденсации греющего пара при Рабс = Ризб + Ро, Дж/кг;
Ро – атмосферное давление;
φ – паросодержание (степень сухости) греющего пара.
Значения rг.п определяем из таблицы 10 свойств насыщенного водяного пара.
3.3.1. Определить состав равновесного пара и температуру кипения смеси, содержащей 30% (мол.) воды и 70% (мол.) уксусной кислоты.
3.3.2. Вычислить равновесные составы фаз и построить диаграммы равновесия в координатах у* – х и t – x, y для системы н-пентан-н-гексан при давлении 765 мм рт.ст., считая, что смесь характеризуется законом Рауля. Данные об изменении давления насыщенных паров чистых компонентов при различной температуре приведены в таблице 18.
Таблица 18 – К построению кривой равновесия для системы н-пентан-н-гексан
| Температура, °С | Давление паров, мм рт.ст. | |
н-пентан, 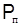
| н-гексан, 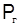
| |
| 36,3 | ||
3.3.3. Определить температуру конденсации смеси паров, содержащей (в мольных долях): н-пентана – 0,42, н-гексана – 0,58 при давлении П = 765 мм рт.ст., используя данные задачи 3.3.2.
3.3.4. Определить требуемую поверхность и расход воды в дефлегматоре ректификационной колонны для разделения бензольно-толуольной смеси при следующих условиях: количество верхнего продукта 600 кг/ч; число флегмы 3,75; начальная и конечная температуры охлаждающей воды 20 и 45 °С; коэффициент теплопередачи 700 Вт/(м2 . К). Считать верхний продукт за чистый бензол. Давление в колонне атмосферное.
3.3.5. В ректификационной колонне непрерывного действия необходимо разделить смесь бензол-толуол, содержащую 40% (масс.) бензола. Расход смеси 30000 кг/ч. Дистиллят содержит 97% (масс.) бензола, а кубовый остаток – 98% (масс.) толуола. Определить количества полученных продуктов и число теоретических тарелок, если флегмовое число R = 3,5.
|
|
|
|
|
Дата добавления: 2017-02-01; Просмотров: 547; Нарушение авторских прав?; Мы поможем в написании вашей работы!