
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Понятие теплоемкости
|
|
|
|
Теплоемкость идеального газа.
Первое начало термодинамики.
Основу термодинамики составляют ее первые два начала.
Первое начало устанавливает количественные соотношения, имеющие место при превращениях энергии из одних видов в другие. Второе начало определяет условия, при которых возможны эти превращения, то есть определяет возможные направления протекания процессов (см. главу 4.5.).
Первое начало термодинамики (закон сохранения энергии): количество тепла, сообщенное системе, идет на приращение внутренней энергии системы и на совершение работы над внешними телами:
в интегральной форме 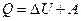 , (4.3.10)
, (4.3.10)
в дифференциальной форме 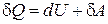 , (4.3.11)
, (4.3.11)
где 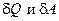 - элементарные (бесконечно малые) теплота и работа;
- элементарные (бесконечно малые) теплота и работа;
dU - полный дифференциал внутренней энергии (поскольку внутренняя энергия есть функция состояния).
Согласно первому закону термодинамики (4.3.10, 11), количество тепла d Q, сообщенное системе, идет на изменение ее внутренней энергии dU и работу d A, которую система совершает над внешними телами.
В термодинамическом описании процессов важную роль играет величина, называемая теплоемкостью.
Рассмотрим систему, которая получает энергию в процессе теплообмена. Пусть для нагревания системы на dТ градусов потребовалось количество теплоты 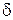 Q.
Q.
Теплоемкостью тела (системы) называют количество тепла, которое необходимо сообщить этому телу, чтобы увеличить его температуру на один кельвин:
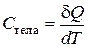 (4.3.12)
(4.3.12)
Размерность теплоемкости 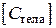 =
= 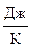
Теплоемкость, отнесенная к единице массы вещества, называется удельной теплоемкостью (c):
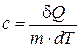 (4.3.13)
(4.3.13)
Размерность удельной теплоемкости [с] = 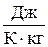
Теплоемкость, отнесенная к одному молю вещества, называется молярной теплоемкостью (C):
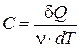 (4.3.14)
(4.3.14)
Размерность молярной теплоемкости [C] = 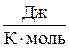
Между молярной и удельной теплоемкостями существует очевидное соотношение:
C = m × c, (4.3.15)
где m – молярная масса вещества.
|
|
|
|
|
Дата добавления: 2013-12-12; Просмотров: 428; Нарушение авторских прав?; Мы поможем в написании вашей работы!