
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Адиабатический процесс. Процесс без обмена теплотой с окружающей средой называется адиабатическим
|
|
|
|
Процесс без обмена теплотой с окружающей средой называется адиабатическим. Он может происходить, если газ (или другое тело) окружен абсолютно не проводящей тепло оболочкой или процесс происходит очень быстро, так что газ не успевает обменяться теплом с другими телами.
При таких процессах первое начало термодинамики упрощается:
δQ = 0; dU = – δА. (32).
Это означает, что если над газом производить работу ( δ А < 0), то dU > 0. Внутренняя энергия газа возрастает, он нагревается. Если же газ расширяется, то он сам производит работу δ А > 0 за счет собственной внутренней энергии и dU < 0. В результате он охлаждается.
Согласно (25): dU =ν · CV · dT. Дляδ А используем соотношение (20). Тогда выражение (32) для адиабатического процесса можно записать так:
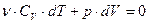 (33).
(33).
Подставим сюда р из уравнения Клапейрона-Менделеева (4) иполучим:
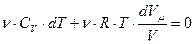 ;
; 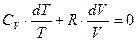 (34).
(34).
Проинтегрируем последнее выражение для пределов изменения переменных от T 1 до T 2 и от V 1 до V 2 и введя обозначение 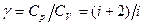 (35). получим:
(35). получим: 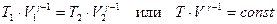 (36),
(36),
а используя Т = p·V/(ν·R), получаем 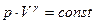 (37).
(37).
Соотношения (36-37) носят название уравнений Пуассона или адиабаты. γ – показатель адиабаты.
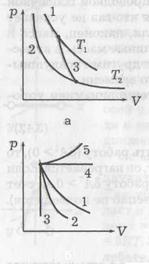 Поскольку γ > 1, давление в (37) обратно пропорционально не V, как было при изотермическом процессе, а Vγ, т. е. давление убывает с увеличением объема быстрее. На рисунке a кривые 1 и 2 – изотермы (Т 2 < T 1), а кривая 3 – адиабата.
Поскольку γ > 1, давление в (37) обратно пропорционально не V, как было при изотермическом процессе, а Vγ, т. е. давление убывает с увеличением объема быстрее. На рисунке a кривые 1 и 2 – изотермы (Т 2 < T 1), а кривая 3 – адиабата.
При любых других процессах (неизотермических и неадиабатических) всегда можно связь между р и V написать в виде (37), но γ уже не будет равна Ср/СV.
В этих случаях процесс называется политропическим, а γ – показателем политропы.
Можно сказать, что для изотермического (T =const) процесса γ = 1, для изобарического (р = const) γ = 0, для изохорического (V = const) γ = ∞. На рисунке б показаны различные процессы расширения газа: 1 – изотерма, 2 – адиабата, 3 – изохора, 4 – изобара, 5 – политропа. Процессы 2, 3 идут с охлаждением, а 4, 5 – с нагреванием газа.
|
|
|
|
|
Дата добавления: 2013-12-12; Просмотров: 491; Нарушение авторских прав?; Мы поможем в написании вашей работы!