
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Гальванический элемент Даниэля-Якоби
|
|
|
|
Гальванический элемент Даниэля-Якоби состоит из медной пластинки, погруженной в раствор СuSO4. и цинковой пластинки, погруженной в раствор ZnSO4. Для предотвращения смешения электролитов электроды отделены друг от друга пористой перегородкой, пропускающей ионы.
На поверхности цинковой пластины возникает двойной электрический слой и устанавливается равновесие следующего типа:
Zn D Zn2+ + 2ē
В результате протекания этого процесса возникает электродный потенциал цинка (рис.5.2).
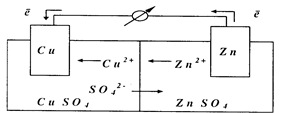
Рис.5.2.
На поверхности медной пластины также возникает двойной электрический слой и устанавливается равновесие:
Сu D Cu2+ + 2ē
В результате возникает электродный потенциал меди. Потенциал цинкового электрода имеет более отрицательное значение, чем потенциал медного, поэтому при замыкании внешней цепи электроны будут переходить с цинкового электрода на медный. В результате этого перехода равновесие на цинковом электроде сместится вправо, поэтому в раствор перейдет дополнительное количество ионов цинка. На медном электроде равновесие сместится влево, и произойдет дополнительный разряд ионов меди.
При замыкании внешней цепи возникает самопроизвольный процесс растворения цинка на цинковом электроде и выделение меди на медном электроде. Эти процессы будут продолжаться до тех пор, пока не выровняются потенциалы электродов, или не растворится весь цинк, или не высадится вся медь.
При работе элемента Даниэля-Якоби протекают следующие процессы:
1. Окисление цинка
Zn ‒ 2ē →Zn2+
Процессы окисления в электрохимии называются анодными процессами, а электроды, на которых они протекают называются анодами.
2. Восстановление ионов меди
Сu2+ + 2е → Сu
Процессы восстановления в электрохимии называются катодными процессами, а электроды, на которых идут эти процессы называются катодами.
3. Перенос электронов во внешней цепи.
4. Движение ионов в растворе:
анионов SO4 2--к аноду; катионов Zn2+, Сu2+ - к катоду. Движение ионов SO4 2- из раствора СuSO4 в другой раствор (ZnSO4) связано с преобладанием заряда анионов во 2-ом растворе над зарядом Сu2+, а в 1-ом, наоборот, преобладает заряд Zn2+.
Движение ионов замыкает электрическую цепь гальванического элемента. Суммируя электродные реакции, получим
Zn + Cu2+ →Zn+2 + Cu
В результате этой реакции в гальваническом элементе возникает движение электронов во внешней цепи, т. е. электрический ток. Поэтому суммарная реакция в гальваническом элементе называется токообразующей.
(Анод) Zn│Zn2+││Cu2+│Cu (Катод)
В гальваническом элементе совершается электрическая работа за счет энергии химической реакции.
|
|
|
|
|
Дата добавления: 2013-12-12; Просмотров: 1412; Нарушение авторских прав?; Мы поможем в написании вашей работы!