
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Потенциалов
|
|
|
|
Стандартный водородный потенциал. Водородная шкала
Электродвижущая сила гальванического элемента
Стандартная ЭДС элемента — это ЭДС элемента, если относительные парциальные давления всех участков реакции равны единице или концентрации исходных веществ и продуктов реакции равны 1.
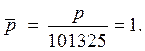
Максимальная разность потенциалов электродов, которая может быть получена при работе гальванического элемента называется электродвижущей силой элемента (ЭДС). Она равна разности равновесных потенциалов катода и анода.
Изменение потенциала электрода зависит от концентрации или от парциальных давлений всех участников реакции.
Условие самопроизвольного протекания реакции в нужном направлении это положительное значение ЭДС.
Потенциал электрода экспериментально измерить невозможно, но можно определить через ЭДС. ЭДС гальванического элемента равна разности равновесных потенциалов электродов:
ЕЭ = ЕК - ЕА,
где ЕК - потенциал катода; ЕА - потенциал анода.
Если потенциал одного из электродов принять равным 0, то относительный потенциал второго электрода будет равен ЭДС элемента.
За 0 принят потенциал водородного электрода 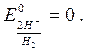
Электрод выполнен из платинированной Pt, контактирующей с газообразным водородом, находящимся при р- 101кПа и раствором, в котором концентрация ионов [Н+] равна 1 или рH =0.
Для определения потенциала электрода по водородной шкале собирают гальванический элемент, одним из электродов которого является измеряемый, а вторым - стандартный водородный электрод:
H2, Pt | H+ || Сu2+ | Сu
H2 - 2e = 2H+ Сu2+ + 2e = Сu
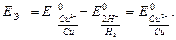
ЭДС этого элемента будет равна потенциалу медного электрода.
Токообразующей реакцией в этом элементе будет следующая реакция:
Сu2+ + H2 = Сu + 2H+.
Водородный электрод называют газовым. К газовым электродам относятся кислородный O2,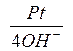 , хлористый Cl2,
, хлористый Cl2,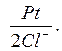
Расположив металлы в порядке возрастания потенциала, что приводит к уменьшению восстановительной и увеличению окислительной активности соответствующих систем получили ряд напряжений металлов, где каждый предыдущий активнее последующего и может вытеснить его из раствора.
|
|
|
|
|
Дата добавления: 2013-12-12; Просмотров: 371; Нарушение авторских прав?; Мы поможем в написании вашей работы!