
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Работа и теплопередача
|
|
|
|
Термодинамическая система. Внутренняя энергия идеального газа
Лекция 9
ГЛАВА 7. ОСНОВЫ ТЕРМОДИНАМИКИ
Термодинамическая система (ТС) - это совокупность макроскопических тел обменивающихся энергией в форме работы и тепла как друг с другом, так и внешней средой.
Внутренняя энергия системы U складывается из внутренних энергий тел, входящих в данную систему и является однозначной функцией параметров ее состояния P, V, T: U = f(P,V,T).
Изменение внутренней энергии ΔU при переходе системы из одного состояния в другое не зависит от вида процесса (ΔU =U2 – U1). Если система совершает круговой процесс, то изменение ее внутренней энергии не происходит.
Внутренняя энергия идеального газа складывается из хаотического поступательного, вращательного и колебательного движения молекул.
Внутренняя энергия одного моля идеального газа равна произведению средней энергии одной молекулы 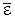 и числа Авогадро NA:
и числа Авогадро NA:
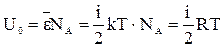 .
.
Внутренняя энергия произвольной массы М идеального газа
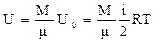 . (7.1)
. (7.1)
где μ – молярная масса; М/ μ – число молей.
Внутренняя энергия идеального газа зависит только от его температуры.
Обмен энергией между (ТС) и окружающими ее телами может проходить в двух формах: макроскопической (в форме работы) и микроскопической (в форме теплопередачи, или теплооборота).
Работа – это мера обмена энергией между рассматриваемой (ТС) и окружающими ее телами, в результате которого изменяются ее параметры P, V, T. Так, при расширении (ТС) совершает работу против внешних сил и отдает свою энергию. В качестве примера рассмотрим расширение газа в цилиндре с поршнем (рис. 7.1). Предположим, что газ расширяется равновесно, т. е. в любой момент времени внешнее давление Рвн практически равно давлению газа под поршнем Р. При перемещении поршня на dх сила F совершает работу dА = Fdх и создает давление на поршень. Работа газа dА = Fdx=РSdx = РdV, где dV – приращение объема при перемещение поршня площадью S на dx. При изменении объема газа от V1 до V2 работа
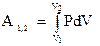 . (7.2)
. (7.2)
 Приращение объема может быть как положительным (dV >0), так и отрицательным (dV<0). В первом случае совершается работа над внешними телами (отдается им часть энергии), во втором – внешние тела совершают работу
Приращение объема может быть как положительным (dV >0), так и отрицательным (dV<0). В первом случае совершается работа над внешними телами (отдается им часть энергии), во втором – внешние тела совершают работу
(ТС система энергию извне).
Состояние ТС, при котором все ее параметры при неизменных внешних условиях изменяются во времени, называется равновесным. Равновесное состояние на РV-диаграмме изображается точкой (рис. 7.2, 7.3).
|
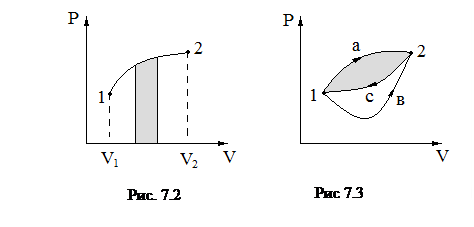
Переход ТС из одного равновесного состояния в другое изображается линией. Работа dА, совершенная ТС при изменении ее объема на dV, равна площади заштрихованной полоски (рис 7.2.). Полная работа перехода ТС из первого положения во второе А1,2 равна площади криволинейной трапеции под кривой 1,2. Работа зависит от направления перехода системы из одного состояния в другое. Так, если ТС переходит из состояния 1 в состояние 2 один раз по пути а), а другой по пути b (рис. 7.3), то А1a2 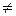 А1b2 (не равны площади под кривыми перехода).
А1b2 (не равны площади под кривыми перехода).
Процесс, при котором ТС, пройдя некоторую последовательность состояний, вновь возвращается в исходное, называется круговым процессом (циклом). Работа, совершаемая ТС за цикл, отличается от нуля (Ац 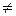 0). Если цикл идет по часовой стрелке (1a2c1), то Ац>0, против часовой стрелки (1b2c1) Ац<0. В первом случае ТС отдает энергию, во втором получает.
0). Если цикл идет по часовой стрелке (1a2c1), то Ац>0, против часовой стрелки (1b2c1) Ац<0. В первом случае ТС отдает энергию, во втором получает.
Теплопередача – процесс передачи энергии неупорядоченного движения молекул от одних тел к другим.
Теплопередача осуществляется либо путем непосредственного взаимодействия частиц системы с частицами среды при их случайных столкновениях, либо путем обмена электромагнитным излучением (лучеиспускание).
Энергия, полученная или отданная ТС в процессе теплообмена, называется количеством тепла δ Q.
В зависимости от того, в какой форме система обменивается энергией с внешними телами, она может быть замкнутой и адиабатически замкнутой. В замкнутой системе отсутствует теплообмен (δ Q = 0) и не совершается работа (А = 0), т.е. имеет место полная энергетическая изоляция. В адиабатически замкнутой системе отсутствует теплообмен (δ Q = 0), но совершается работа (А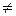 0).
0).
|
|
|
|
|
Дата добавления: 2013-12-11; Просмотров: 1143; Нарушение авторских прав?; Мы поможем в написании вашей работы!