
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Основы термодинамики
|
|
|
|
1. Внутренняя энергия термодинамической системы.
Внутренняя энергия U- это энергия хаотического (теплового) движения микрочастиц системы (молекул, атомов, электронов, ядер и т.д.) и энергия взаимодействия этих частиц.
К внутренней энергии не относятся кинетическая энергия движения системы как целого и потенциальная энергия системы во внешних полях.
Внутренняя энергия - однозначная функция термодинамического состояния системы - в каждом состоянии система обладает вполне определенной внутренней энергией.
Поэтому, внутренняя энергия не зависит от того, каким образом система пришла в данное состояние.
При переходе системы из одного состояния в другое изменение внутренней энергии определяется только разностью значений внутренней энергии этих состояний и не зависит от пути перехода.
2. Число степеней свободы.
Число степеней свободы - это число независимых переменных, полностью определяющих положение системы в пространстве.
Число степеней свободы для идеального газа жестких молекул.

В реальных молекулах нет жесткой связи между атомами в молекуле, поэтому необходимо учитывать также степени свободы колебательного движения атомов внутри молекулы.
Независимо от общего числа степеней свободы молекулы, три степени свободы всегда поступательные. На каждую из них приходится треть кинетической энергии поступательного движения молекулы ( 0):
0):

3. Закон Больцмана о равномерном распределении энергии по степеням свободы (закон Равнораспределения).
Для системы, находящейся в состоянии термодинамического равновесия на каждую поступательную и вращательную степень свободы приходится в среднем кинетическая энергия, равная  а на каждую колебательную степень свободы - в среднем энергия, равная kТ
а на каждую колебательную степень свободы - в среднем энергия, равная kТ
Энергия колебательных степеней свободы вдвое больше, поскольку колебательная система обладает равными г10 величине средними значениями как кинетической, так и потенциальной энергии.
Таким образом, средняя энергия молекулы. 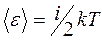
где i - сумма поступательных, числа вращательных и удвоенного числа колебательных степеней свободы молекулы: i=iпост+iвращ+2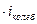 . В классической теории рассматривают молекулы с жесткой связью между атомами; для них i совпадает с числом степеней свободы молекулы.
. В классической теории рассматривают молекулы с жесткой связью между атомами; для них i совпадает с числом степеней свободы молекулы.
В идеальном газе молекулы между собой не взаимодействуют и их потенциальная энергия равна нулю. Поэтому внутренняя энергия одного моля идеального газа Uμ и произвольной массы m газа U будут соответственно:

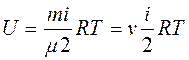
|
|
|
|
|
Дата добавления: 2013-12-13; Просмотров: 505; Нарушение авторских прав?; Мы поможем в написании вашей работы!