
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Скорость химической реакции
|
|
|
|
ВВЕДЕНИЕ
Химическая кинетика изучает скорость химических процессов и зависимость ее от различных факторов.
Прикладное значение кинетики заключается в том, что для управления химической реакцией необходимо знать скорость ее протекания в данных условиях и способы ее изменения.
Теоретическое значение кинетики заключается в выяснении механизма химических реакций.
В химической кинетике возникают дополнительные трудности в связи с появлением новой переменной – времени и влиянием большого числа других факторов, часто даже трудно учитываемых.
Кинетические исследования состоят в решении таких проблем, как определение порядка и константы скорости реакций, числа и характера промежуточных продуктов, энергии активации реакции и т.д.
Скоростью химической реакции называется число молекул или молей данного вещества, реагирующих в единицу времени в единице объема.
В общем виде химическую реакцию можно написать так:
n1А1 + n2А2 + ……+niАi ® n`1A`1 + n`A`2 + …..+n`iA`i,
где ni и n`i - стехиометрические коэффициенты исходных и полученных веществ; Аi и А`i - исходные и полученные вещества.
Для определения скорости химической реакции достаточно знать изменение концентрации количества одного из присутствующих в реакции веществ, так как изменение количества всех остальных веществ можно определить из уравнения химической реакции.
Реагируют только те молекулы, которые сталкиваются. Число столкновений прямо пропорционально числу имеющихся молекул, поэтому скорость реакции должна быть пропорциональна концентрации реагирующих веществ в степени стехиометрического коэффициента:
v = k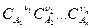 ,
,
где v – скорость химической реакции; k – константа скорости химической реакции.
Это выражение иногда называют основным постулатом химической кинетики.
Физический смысл коэффициента k можно установить, если принять все концентрации равными единице:
СА1 = СА2 = …. = САп = 1.
При этом условии v = k, т.е. константа скорости химической реакции есть скорость реакции при условии, что концентрации реагирующих веществ равны единице. Эту величину иногда называют удельной скоростью химической реакции.
Обычно скорость данной химической реакции при постоянных внешних условиях не остается постоянной, а изменяется во времени. По мере израсходования исходных веществ скорость процесса уменьшается.
Поэтому численные значения скорости реакции будут различными в зависимости от того, для какого момента или промежутка времени рассматривается изменение концентраций.
Существует понятие средней скорости реакции:
v = ± .
.
И истинной скорости химической реакции:
v = ±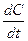 .
.
Скорость реакции всегда считается положительной. Производная 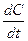 может быть как положительной, так и отрицательной, в зависимости от подстановки концентраций исходных веществ или продуктов реакции. Если скорость определяется по концентрации исходных веществ, то перед производной ставят знак минус, если по концентрации продуктов реакции – знак плюс.
может быть как положительной, так и отрицательной, в зависимости от подстановки концентраций исходных веществ или продуктов реакции. Если скорость определяется по концентрации исходных веществ, то перед производной ставят знак минус, если по концентрации продуктов реакции – знак плюс.
КИНЕТИЧЕСКАЯ КЛАССИФИКАЦИЯ РЕАКЦИЙ
Реакции разделяют по следующим признакам:
1. По числу молекул, участвующих в реакции (молекулярность и порядок реакции).
Молекулярность реакции определяется числом молекул, одновременным взаимодействием между которыми осуществляется акт химического взаимодействия.
По этому признаку реакции разделяются на одно-, дву-, и трехмолекулярные.
Порядок реакции равен сумме показателей степеней концентраций в уравнении, выражающем зависимость скорости реакции от концентраций реагирующих веществ.
Реакция первого порядка - - = k C.
Реакция второго порядка - - = k C1C2.
Реакциями нулевого порядка называют процессы, в которых скорость процесса сохраняется постоянной во времени – v = const.
Примером несовпадения молекулярности и порядка может служить способ проведения реакции на примере следующей реакции:
СН3СООС2Н5 + Н2О = СН3СООН + С2Н5ОН.
В зависимости от способа контактирования реагирующих веществ, в этой реакции при неизменной молекулярности, равной двум, порядок реакции может равняться двум, единице и нулю.
2. По природе частиц, участвующих в реакции.
Реакции, в которых участвуют молекулы, называются молекулярными.
Реакции с участием ионов называются ионными.
Реакции с участием атомов или свободных радикалов называются цепными.
3. По числу фаз, участвующих в реакции.
Реакции, протекающие в одной фазе, называются гомогенными. Реакции, протекающие на границе раздела фаз, называются гетерогенными.
4. По степени сложности реакции подразделяются на:
а) обратимые и необратимые.
Обратимые реакции, это реакции в которых продукты реакции могут взаимодействовать с образованием исходных веществ.
Необратимыми являются обычно такие реакции, в ходе которых хотя бы один из продуктов удаляется из сферы реакции;
б) изолированные и параллельные.
Изолированные реакции – реакции, дающие продукт только одного типа. Параллельные реакции – такие, в которых взятые вещества одновременно реагируют в двух или более направлениях
в) сопряженные реакции.
Это совместные реакции вида
A + B ®M;
A + C ® N, из которых одна протекает лишь совместно с другой;
г) последовательные реакции (многоступенчатые или консекутивные).
В этих реакциях наблюдаются промежуточные стадии А®В®С. Вещество В является промежуточным продуктом в процессе получения вещества С.
Если одна из составляющих реакций обладает много меньшей скоростью, чем остальные, то общая скорость реакции определяется этой наиболее замедленной стадией.
|
|
|
|
|
Дата добавления: 2014-01-05; Просмотров: 509; Нарушение авторских прав?; Мы поможем в написании вашей работы!