
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Необратимая реакция первого порядка
|
|
|
|
Кинетическое уравнение реакции первого порядка можно вывести следующим образом. Пусть в начальный момент времени имеется а моль исходного вещества А. Если к моменту времени t прореагировало x моль вещества, то в смеси осталось (а — х) моль, Тогда концентрация вещества А в момент времени t равна
CA = 
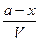 ,
,
где V — объем системы.
Согласно определению скорость реакции первого порядка прямо пропорциональна концентрации реагирующего вещества в первой степени. Следовательно, из основного кинетического уравнения получим
-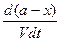 =
= 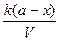 .
.
Сократив обе части уравнения на V, будем иметь
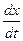 = k(a-x).
= k(a-x).
Это и есть дифференциальное уравнение скорости необратимой реакции первого порядка. Разделив переменные, получим
 = kdt.
= kdt.
После интегрирования получим
- ln (а - х) = kt + С.
Постоянную интегрирования С можно найти, подставив начальные условия (t = 0; х = 0) в выражение
-lna = С;
k = ln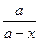 .
.
Выражение путем деления числителя и знаменателя дроби, стоящей под знаком логарифма, на объем (при условии, что он постоянен) можно переписать:
k = ln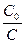 ,
,
где Со— исходная концентрация реагирующего вещества; C — концентрация этого вещества к моменту времени t.
Как видно из выражений, величина k имеет размерность обратного времени.
Следовательно, константу скорости реакции первого порядка можно выражать в с-1,мин-1 или ч-1.
Освободившись от логарифма, получим
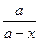 = еkt;
= еkt;
a-x = ae-kt;
x = a(1 – e-kt).
По уравнениям можно определить количество (а—х) вещества А, непрореагировавшее к моменту времени t, количество х этого вещества, прореагировавшее к моменту времени t, или, другими словами, количество вещества В, образовавшегося к моменту времени t.
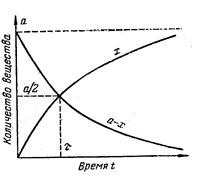
На рисунке зависимости прореагировавшего х и оставшегося а—х количества исходного вещества А от времени показаны графически. Из рисунка и из уравнений видно, что полное исчезновение исходного вещества произойдет через бесконечно большой промежуток времени. В практических расчетах за конец реакции принимается тот момент, когда аналитическим способом исходное вещество обнаружить невозможно. Время, соответствующее точке пересечения кривых, обозначено через t. Очевидно, что в точке пересечения
а – х = х;
х =,
т. е. к моменту времени t прореагирует половина исходного вещества.
Поэтому время t называется временем полураспада.
ае-kt = a(1 – e-kt);
2e-kt = 1;
ekt = 2;
t =.
Таким образом, время полураспада не зависит от количества исходного вещества. Это понятно для простых мономолекулярных реакций, так как превращение молекул в этих реакциях является спонтанным (не зависящим от присутствия остальных).
|
|
|
|
|
Дата добавления: 2014-01-05; Просмотров: 1161; Нарушение авторских прав?; Мы поможем в написании вашей работы!