
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Спін і магнітний момент електрона
|
|
|
|
10. Розглядаючи невідповідність теорії та експерименту Штерна та Герлаха також потрібно взяти до уваги результати дослідів Ейнштейна й де Гааза з визначення гіромагнітного відношення. Для заліза виявилося, що гіромагнітне відношення дорівнює
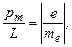 (11.9)
(11.9)
тобто є удвічі більшим, ніж випливає з класичної теорії.
Також, виявилося, що спектральні терми лужних металів мають так звану дублетну структуру, тобто складаються із двох близько розміщених рівнів. Для опису цієї структури трьох квантових чисел n,l,m виявилося недостатньо – необхідно було ввести четверте квантове число. Це було головним мотивом, через який Уленбек й Гаудсміт у 1925 р. ввели гіпотезу про спін електрона. Сутність цієї гіпотези полягає в тому, що в електрона є не тільки момент імпульсу й магнітний момент, які пов'язані з переміщенням цієї частинки як цілого. Електрон має також власний, або внутрішній механічний момент імпульсу. Цей власний момент імпульсу й називається спіном (від англійського слова to spin – вертітися). Відповідний йому магнітний момент називається спіновим магнітним моментом. Ці моменти позначаються відповідно через Ls і pm,s на відміну від орбітальних моментів Ll і pm,l. Четверте квантове число позначають просто через s і називають спіном.
Самі Уленбек і Гаудсміт припускали, що спін виникає через обертання електрона навколо власної осі. Через це існуюча в той час модель атома отримала ще більшу подібність до Сонячної системи. Електрони (планети) не тільки обертаються навколо ядра (Сонця), Але й навколо власних осей. Однак відразу ж з'ясувалася хибність такого класичного уявлення про спін (такі уявлення не змогли пояснити результат (94.7)). У 1928 р. Дірак показав, що спін електрона автоматично випливає з його теорії електрона, яка була заснована на релятивістському хвильовому рівнянні. У теорії Дірака було отримано гіромагнітне відношення для власних моментів, яке збігалося з дослідом (див. (94.7)). Таким чином, спін електрона є квантово-релятивістським ефектом, який не має класичного тлумачення. Потім концепція спіну як внутрішнього моменту імпульсу була поширена на інші елементарні й складні частинки й знайшла підтвердження й широке застосування в сучасній фізиці.
20. У загальному курсі фізики немає можливості викласти докладну теорію спіну. Ми візьмемо як вихідне положення, що спіновому моменту імпульсу відповідає векторний оператор, проекції якого мають властивості, подібні до властивостей оператора орбітального моменту імпульсу. Із цього випливає, що визначені значення в одному і тому самому стані можуть мати тільки квадрат повного спіну й одна з його проекцій на визначену вісь (вісь Z). Якщо максимальне значення проекції Lz,s дорівнює 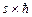 (s – спінове квантове число, співвідношення написане за аналогією з Lz,l = mmax
(s – спінове квантове число, співвідношення написане за аналогією з Lz,l = mmax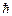 , де mmax = l), то число всіх можливих проекцій, які відповідають даному квантовому числу s, буде дорівнювати 2 s +1 (у випадку орбітального руху має місце аналогічне співвідношення 2 l +1).
, де mmax = l), то число всіх можливих проекцій, які відповідають даному квантовому числу s, буде дорівнювати 2 s +1 (у випадку орбітального руху має місце аналогічне співвідношення 2 l +1).
У Дослідах Штерна й Герлаха атоми водню перебували в s -стані, тобто їх орбітальні моменти дорівнювали нулю (l = 0). Тому Уленбек і Гаудсміт припустили, що розщеплення пучка обумовлене не орбітальним, а спіновим магнітним моментом. Те саме стосується й дослідів з атомами срібла. Атом срібла має єдиний зовнішній електрон. Атомний остов через його симетрію спінового і магнітного моментів не має. Весь магнітний момент атома срібла створюється тільки одним зовнішнім електроном. Коли атом перебуває в нормальному, тобто s -стані, то орбітальний момент валентного електрона дорівнює нулю – весь момент є спіновим. Тому результати дослідів у цьому випадку визначалися виключно спіновими моментами електрона.
30. Досліди Штерна й Герлаха показали, що для атома срібла та водню (l = 0) пучок розщеплювався на два пучки. Це означає, що 2 s +1 = 2. Звідси отримуємо для електрона s =1/ 2.
Для електрона, таким чином, спінове квантове число дорівнює 1/2:
s = 1/ 2. (11.10)
Для власного моменту імпульсу є справедливим співвідношення, аналогічне до орбітального моменту імпульсу електрона:
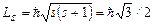 . (11.11)
. (11.11)
Проекція власного моменту імпульсу на вісь Z визначається співвідношенням
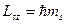 (ms = ± s = ±1/ 2). (11.12)
(ms = ± s = ±1/ 2). (11.12)
Виміри проекції магнітного моменту pm,z в досліді Штерна й Герлаха показали, що для атомів водню й срібла величина pm,z дорівнює магнетону Бору mБ. Таким чином, було отримано гіромагнітне відношення для електрона
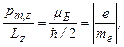 (11.13)
(11.13)
яке відповідає результату, що був знайдений Ейнштейном і де Гаазом (див. (11.9)).
4. Отже, стан електрона в атомі задається головним n, орбітальним 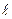 , магнітним
, магнітним 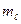 і магнітним спіновим
і магнітним спіновим 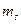 квантовим числом.
квантовим числом.
Коли всі електрони квантово-механічної системи мають однакові фізичні властивості (масу, заряд, спін та ін.), тобто є тотожними, їx неможливо експериментально розпізнати. Це є фундаментальний принцип квантової механіки - принцип нерозрізненості тотожних частинок
 , (11.14)
, (11.14)
де 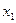 і
і 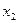 – відповідно сукупність просторових i спінових координат першої i другої частинок. 3 виразу (11.14) випливає
– відповідно сукупність просторових i спінових координат першої i другої частинок. 3 виразу (11.14) випливає
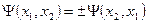 , (11.15)
, (11.15)
тобто принцип нерозрізненості тотожних частинок приводить до певної симетрії хвильової функції. Коли при зміні частинок місцями хвильова функція не змінює знаку, то вона називається симетричною, коли змінює – антисиметричною. Властивість симетрії або антисиметрії – ознака даного типу мікрочастинок і визначається їx спіном. Частинки з напівцілим спіном (електрони, протони, нейтрони) описуються антисиметричними хвильовими функціями і підпорядковуються статистиці Фермі - Дірака. Ці частинки називаються ферміонами. Частинки з нульовим або цілим спіном (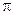 -мезони, фотони) описуються симетричними хвильовими функціями i підпорядковуються статистиці Бозе-Ейнштейна. Ці частинки називаються бозонами.
-мезони, фотони) описуються симетричними хвильовими функціями i підпорядковуються статистиці Бозе-Ейнштейна. Ці частинки називаються бозонами.
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 3764; Нарушение авторских прав?; Мы поможем в написании вашей работы!