
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Ключевые слова. Для успешного усвоения этой темы необходимо
|
|
|
|
Уметь
Знать
РЕАКЦИИ БИОЛОГИЧЕСКОГО ОКИСЛЕНИЯ В ОРГАНИЗМЕ ЧЕЛОВЕКА
Для успешного усвоения этой темы необходимо
-определение реакция окисления и восстановления в приложении к органическим сокдинениям
- последовательность превращения кислородсодержащих функциональных групп в реакциях окисления-ввосстановления
-особенности протекания окислительно-восстановительных реакций с участием переносчиков электронов в составе ферментов оксидоредуктаз
- механизм действия коферментов НАД+ , НАДФ+, пары хинон/гидрохинон, липоевой кислоты, витамина С.
-клапссификацию карбоновых кислот
- физические и химические свойства карбоновых кислот, участвующих в превращениях цикла Кребса
- составить схемы химических окислительно-восстановительных реакций
- написать формулы коферментов НАД (Ф)+ / НАД(Ф)Н
- написать формулы биоорганических соединений, участвующих в превращениях цикла Кребса
Выработка энергии в организме человека и синтез новых жизненно важных соединений связаны с протеканием окислительно-восстановительных реакций.
2.1.1. Окислительно-восстановительные реакции биоорганических соединений
Реакция окисления - изменяется состав вещества – добавляются атомы кислорода или удаляются атомы водорода.
Реакции восстановления – изменяется состав вещества – удаляются атомы водорода или добавляются атомы водорода..
К процессам окисления относятся превращения, сопровождающиеся внутримолекулярным дегидрированием (обратный процесс гидрирование – восстановление)
А. С (sp3) ———> С (sp2) ———> С (sp)
алкан алкен алкин
- СН2-СН2- - СН= СН-
последовательность
процессов окисления
Б. R– СН3 ———> R– СН2 – ОН ———> R– СН= О
спирт альдегид
В. Окисление тиолов происходит как межмолекулярная реакция дегидрирования, сопровождается, в первую очередь, образованием дисульфидов.
2 R – SH + [ O ] ———> R – S – S – R + НОН
тиол дисульфид
Реакция имеет большое значение в регуляции количества свободных SH групп и дисульфидных связей в белках. Окислители уменьшают содержание свободных тиольных групп, а восстановители - уменьшают число дисульфидных связей.
Тиольные группы в белках играют важную роль в выполнении белками ферментативных и других функций, например, активная форма гормона инсулина содержит две дисульфидные связи. Прикрепление внеклеточных белков к мембране клетки также может осуществляться с участием дисульфидных групп (белок фибронектин).
В биохимических реакциях окисления и восстановления принимают участие ферменты – оксидоредуктазы. Белковые молекулы не могут осуществлять перенос электронов,
поэтому в составе ферментов обязательно присутствуют органические молекулы или катионы металлов, способные передавать электроны, то есть существовать в окисленной и восстановленной форм е (витамин С, липоевая кислота, кофермент НАД+ / НАДН,
ФАД / ФАДН2, гем, содержащий ионы железа (+2) / (+3), ионы меди (+1) / (+2) и др.)
Реакции окисления- дегидрирования - типичны для насыщенных атомов углерода,
и функциональных групп; альдегидной, гидроксильной, тиольной и аминогруппы. Наиболее распространенным переносчиком атомов водорода является кофермент НАД+ в реакциях окисления и кофермент НАДН в реакциях восстановления (большинство реакций обратимы).
Окисление этанола и других алкоголей алкогольдегидрогеназой – первый этап метаболизма экзогенных спиртов, попадающих в организм в составе лекарственных препаратов, алкогольных напитков.
Фермент алкогольдегидрогеназа
СН3 – СН2 – О – Н + НАД+ <————————> СН3 – СН= О + НАДН + Н +
этанол этаналь
Превращения молочной и пировиноградной кислот друг в друга происходит во всех тканях организма. В анаэробных (бескислородных) условиях образование лактата – конечный этап метаболизма глюкозы. Присутствие кислорода снижает образование молочной кислоты и стимулирует ее окисление в пировиноградную, процесс весьма важен для сердечной мышцы, печени.
фермент лактатдегидрогеназа
СН3 –СН – СООН + НАД+ <————————> СН3 – С – СООН + НАДН + Н +
| | |
ОН О
2-гидроксипропановая кислота 2- оксопропановая кислота
молочная кислота (лактат) пировиноградная кислота(пируват)
2.1.2 Механизм реакции окисления с участием кофермента НАД +
Окисляемое вещество отдает два атома водорода, один – в виде иона гидрида, другой- в виде протона Атом углерода отдает два электрона химический связи атому водорода, который превращается в отрицательно заряженный анион – гидрид Н –.. Протон уходит из гидроксильной группы и оставляет два электрона связи. Эти да электрона образуют двойную связь.
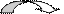
Н Н – 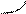 гидрид- ион присоединяется к молекуле НАД + в положение 4
гидрид- ион присоединяется к молекуле НАД + в положение 4
СН3 – С- СООН + НАД +——> СН3 – С- СООН + НАДН + Н+
| | |
О •• Н О
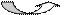 Н+
Н+
Протон переходит в раствор
Оставшаяся пара электронов образует двойную связь.
Кофермент НАД + принимает только один отрицательно заряженный ион гидрида, превращается в НАДН, а протон остается в растворе
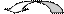
удаляется
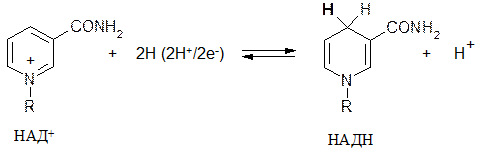
Восстановленная форма НАДН является неустойчивой, поскольку в пиридиновом цикле
исчезает ароматический секстет и единая пи-электронная система. Атом углерода в положении-4 имеет тетраэдрическое строение. Именно вновь присоединенный (в виде гидрида Н–) атом водорода (он выделен жирным шрифтом) затем удаляется при окислении восстановленной формы НАДН и передается следующему окислителю(это называется «молекулярная память») и до образования конечных продуктов обмена (молочная кислота в анаэробных условиях или вода в аэробных условиях)
НАД Н + Н+ + Х ——> НАД + + Х-Н
2.2. Карбоновые кислоты и их производные – участники реакций цикла Кребса
2.2.1 Цикл Кребса
Цикл Кребса – особая циклическая последовательность превращений трикарбоновых
(лимонной, цис-аконитовой, изолимонной) и дикарбоновых кислот (янтарной, фумаровой, яблочной, щавелевоуксусной), в процессе которой создаются условия для синтеза универсального макроэргического соединения АТФ. Цикл начинается с взаимодействия щавелевоуксусной кислоты с активной формой уксусной кислоты АцКоА и заканчивается вновь образованием щавелевоуксусной кислоты.
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 412; Нарушение авторских прав?; Мы поможем в написании вашей работы!