
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Кислотность и основность по Бренстеду-Лоури
|
|
|
|
Кислотные и основные функции веществ
КИСЛОТНЫЕ И ОСНОВНЫЕ СВОЙСТВА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Кислотность и основность – важнейшие понятия, определяющие многие фундаментальные физико-химические свойства и биологическую активность органических соединений.
Основные теории кислот и оснований:
· Ионная теория (С. Аррениус, 1887 г.)
· Протолитическая теория Бренстеда-Лоури (1923 г.).
· Апротонная теория Льюиса.
· Концепция жестких и мягких кислот и оснований (ЖМКО) Р. Пирсона (1963 г.).
Согласно ионной теории кислоты – это электролиты, отщепляющие в водном растворе ионы Н +, а основания – электролиты, отщепляющие в водном растворе ионы ОН –. В результате ассоциации этих ионов между кислотой и основанием происходит реакция нейтрализации с образованием воды и соответствующей соли.
Кислоты – вещества, способные отдавать протон (доноры протона).
Основания – вещества, способные присоединять протон (акцепторы протона).
Таблица 13 – Типы органических кислот по Бренстеду.
| Тип кислоты | Нейтральные молекулы | Положительно заряженные ионы | ||
| Класс соединения | Формула | Класс соединения | Формула | |
| CH | Углеводороды | 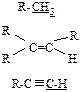
| σ -комплекс |
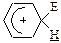
|
| NH | Амины Амиды | 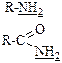
| Алкиламмоний | 
|
| OH | Спирты Фенолы Енолы Карбоновые кислоты Сульфоновые кислоты | 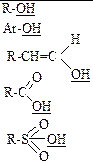
| Алкилоксоний Арилоксоний |
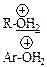
|
| SH | Тиолы | 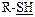
| – | – |
Таблица 14 – Типы органических оснований по Бренстеду.
| Тип основания | Нейтральные молекулы | Формула | Отрицательно заряженные ионы | ||
| Класс соединения | Класс соединения | Формула | |||
| π - | Алкены | 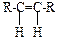
| карбанион | 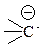
| |
| Продолжение таблицы 14 | |||||
| π - | Алкины Арены |

| карбанион | 
| |
| n - | аммониевые- | амины азометины нитрилы | 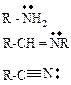
| амид-ион |
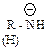
|
| оксониевые- | спирты простые эфиры альдегиды, кетоны карбоновые кислоты | 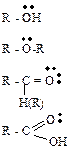
| алкоксид-ион карбоксилат-ион | 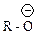

| |
| сульфониевые- | тиолы сульфиды | 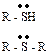
| сульфид-ион | 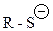
| |
| – | – | – | гидрид-ион | 
|
Количественная сравнительная оценка кислотности и основно-сти. Оценивается на основании уравнения кислотно-основного взаимо-действия, одним из компонентов которого является растворитель (вода или неводные растворители – ледяная CH3COOH, формамид, диметил-формамид, ДМСО и др.).
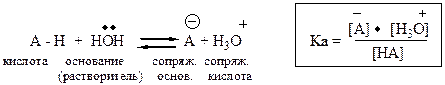
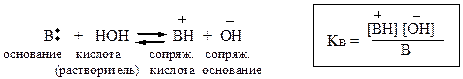
а – [ от англ. acid – кислота ]; в – [от англ. base – основание]
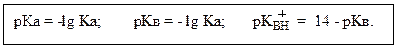
Качественная сравнительная оценка кислотности и основности органических соединений. Проводится с позиций статического и кинетического факторов.
Статический фактор, обуславливающий собственную кислотность или основность соединения в соответствии с его электронным строением в нереагирующем состоянии. Ка и Кв определяются в газовой фазе.
Кинетический фактор, обуславливающий кислотные и основные свойства в соответствии со стабильностью сопряженных оснований (анион) и кислот (катион), образующихся в результате кислотно-основного взаимодействия.
Таблица 15 – Факторы, определяющие степень кислотности и основности
| Факторы, определяющие степень кислотности и основности | В газовой фазе | В растворах |
| - Электроотрицательность атома кислотного или основного центра. - Поляризуемость атома. - Электронные эффекты заместителей. - Стерические эффекты. - Орто - эффект. - Эффект сольватации. | + + + + + – | + + + + + + |
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 1947; Нарушение авторских прав?; Мы поможем в написании вашей работы!