
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Давление пара растворителя над раствором, первый закон Рауля
|
|
|
|
Эксперименты показывают, что при растворении в данном растворителе какого-нибудь растворенного вещества равновесное давление пара растворителя над раствором понижается. Исследуя растворы кислот, щелочей, солей, ряда органических соединений Рауль (1887) открыл количественную зависимость между понижением давления пара и составом раствора. Пусть 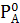 – давление пара над чистым растворителем (при температуре Т),
– давление пара над чистым растворителем (при температуре Т), 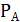 – давление пара растворителя над раствором (при температуре Т). Разность
– давление пара растворителя над раствором (при температуре Т). Разность 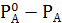 − понижение давления пара растворителя над раствором.
− понижение давления пара растворителя над раствором. 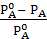 − относительное понижение давления пара для данного раствора.
− относительное понижение давления пара для данного раствора.
Согласно первому закону Рауля: относительное понижение давления пара растворителя над раствором равно мольной доле растворенного вещества в жидкости.
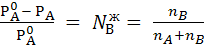 (7.8)
(7.8)
Левая часть уравнения не зависит от природы растворителя, растворенного вещества и температуры раствора.
Исходя из давления пара раствора можно рассчитать МВ (молярную массу растворенного вещества).Так как первый закон Рауля справедлив для разбавленных растворов, когда  ,то можно записать:
,то можно записать:
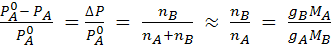 (7.9)
(7.9)
где МА − молярная масса растворителя;
МВ − молярная масса растворенного вещества;
gA– навеска растворителя;
gB − навеска растворенного вещества.
Рассмотрим свойства растворов, содержащих нелетучие растворенные вещества, а именно:
1) относительное понижение давления пара растворителя над раствором;
2) понижение температуры замерзания растворов;
3) повышение температуры кипения раствора по сравнению с чистым растворителем;
4) осмотическое давление.
Эти свойства называются коллигативными, так как они зависят от природы растворителя и концентрации растворенного вещества, т.е. от числа его частиц в единице объема, но не зависят от свойств этих частиц.
Коллигативные свойства растворов проявляются в тех случаях, когда в равновесии находятся две фазы, причем одна из них растворитель и растворенное вещество, вторая – только чистый растворитель.
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 749; Нарушение авторских прав?; Мы поможем в написании вашей работы!