
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Принцип расчета результатов гравиметрического анализа
|
|
|
|
Сущность и общая оценка метода. Классификация методов гравиметрического анализа. Общая схема анализа в методе осаждения. Осаждаемая и гравиметрическая формы, требования к ним.
Общие положения
Гравиметрический анализ (гравиметрия)
И.П.Калинкин, Т.Э.Маметнабиев
Гравиметрическим анализом называют метод количественного химического анализа, основанный на точном измерении массы определяемого вещества или его составной части, выделенной в элементарном виде, или в виде малорастворимого соединения определенного состава.
Гравиметрические методы делятся на три группы: методы осаждения, методы отгонки и методы выделения. Наиболее распространены методы осаждения, поэтому можно встретить и такую формулировку: гравиметрия – метод количественного анализа, в котором переведенную в раствор составную часть пробы осаждают в виде малорастворимого соединения, по массе которого на основе законов стехиометрии находят количество (массу, массовую долю) определяемого компонента.
Гравиметрические методы разработаны для большинства неорганических анионов и катионов, для нейтральных соединений таких, как вода, диоксид серы, углекислый газ, йод а также для целого ряда органических соединений.
Достоинством гравиметрических методов является их высокая точность: при анализе простых образцов с содержанием определяемого аналита более 1% погрешность анализа можно снизить до 0.1 – 0.2 % что редко удается другими методами. При увеличении сложности состава образца погрешности неизбежно возрастают или приходится затрачивать массу времени на их преодоление.
Недостатками гравиметрических методов являются, во – первых, то, что реагенты, используемые в гравиметрии, за редким исключением, не очень специфичны, поскольку они способны образовывать осадки с группой ионов. Следовательно, требуется предварительное отделение или маскирование мешающих ионов. Во – вторых, как следует из схемы 3.1, в которой представлена последовательность операций гравиметрического анализа в самом общем случае, его длительность и трудоемкость. Поэтому эти методы оправдывают себя, как правило, при анализе единичных образцов, когда требуется высокая точность анализа (см с.).
Осаждаемой формой (ОФ) называют малорастворимое соединение, в виде которого из раствора выделяют определяемый компонент. Часто осаждаемая форма не имеет определенного состава, например, Fe(OH)3· n H2O, Al(OH)3· n H2O. Требования к осаждаемой форме:
1. Должна быть обеспечена полнота выделения определяемого компонента (аналита) не менее, чем на 99,9%. Для выполнения этого условия осадок должен обладать очень малой растворимостью: не более, чем
1∙10−6 моль∙л−1 . Осаждение определяемого аналита считается количе–
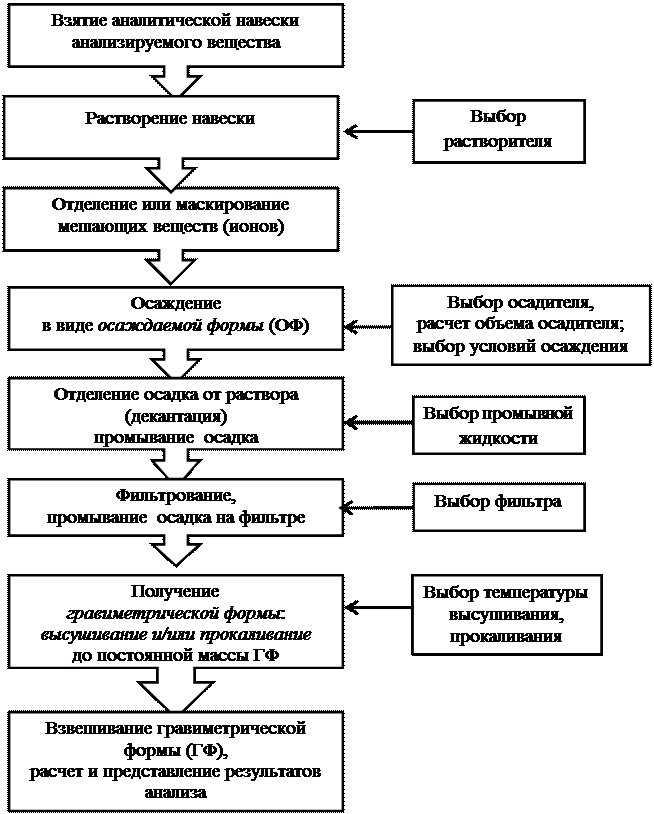
Схема 3.1 – Общая схема гравиметрического анализа
ственным, если, потери за счет растворимости осадка, включая потери при его промывании, будут меньше пределов точности взвешивания на аналитических весах, которая обычно составляет ±0.1 мг (±0.0001г).
2. Осадок должен получаться в форме, удобной для отделения его от раствора (фильтрованием или центрифугированием) и его промывания и не должен быть загрязнен примесями, не удаляемыми при промывке. Как правило, наибольшие проблемы в этом плане представляют аморфные осадки (Fe(OH)3 ·n Н2O, Al(OH)3 ·n H2O), сильно адсорбирующие посторонние ионы. Кроме того, некоторые кристаллические осадки также сорбируют посторонние ионы (BaSО4) или способны образовывать коллоидные растворы (AgCl). И в том, и в другом случае приходится подбирать особые условия осаждения и промывания осадка, а иногда и маскировать посторонние ионы.
Осадок должен легко и полно переходить в гравиметрическую форму при просушивании или прокаливании. В принципе стараются избегать слишком высоких температур прокаливания (>900–1000°C), но, к сожалению, это не всегда возможно. В подавляющем большинстве случаев высушивание дает менее "точные" результаты, чем прокаливание.
Гравиметрической (весовой) формой (ГФ) называют соединение, массу
которого непосредственно измеряют взвешиванием. Требования к гравиметрической форме:
1. Гравиметрическая форма осадка должна быть стехиометрическим соедине-нием определенного состава. Это абсолютно необходимое условие лежит в основе всех расчетов.
2. Гравиметрическая форма должна иметь высокую химическую устойчивость на воздухе, то есть не поглощать влагу или CO2, не окисляться кислородом. Так, например, CaO не является идеальной весовой формой, поскольку он весьма гигроскопичен и образует CaCO3 за счет поглощения CO2 из воздуха. В ряде случаев для выполнения этого условия приходится сильно повышать температуру прокаливания: осадок Al(OH)3· n H2O полностью переходит в Al2O3 уже при 700–800°C, но полученный при такой температуре Al2O3слишком гигроскопичен.
3. Желательно, чтобы содержание определяемого элемента в гравиметрической форме было как можно меньше. В этом случае уменьшается погрешность и увеличивается чувствительность анализа.
Получаемые в ходе осаждения и прокаливания осадки часто имеют различный состав, то есть химик взвешивает не то соединение, которое было получено при осаждении, а какое - то другое, как видно из таблицы 2.1.
При расчете результатов гравиметрического анализа исходят из уравнения
материального баланса (закона сохранения массы), согласно которому число атомов данного типа в изолированной системе неизменно.
Принцип расчета рассмотрим на примере определения бария, магния и Fe3O4. Ионы бария осаждают в виде малорастворимого соединения BaSO4, которое взвешивают после прокаливания. Первым этапом расчета является написание уравнения реакции
 Ba2+ + SO42−= BaSO4↓ или схемы превращения Ba → BaSO4↓
Ba2+ + SO42−= BaSO4↓ или схемы превращения Ba → BaSO4↓
На втором этапе составляют уравнение материального баланса, исходя из постоянства количества вещества, участвующего в реакции:
n (Ba) = n (BaSO4).
Учитывая, что в общем случае количество вещества n( X) связано с его массой m (X) и молярной массой М (Х) уравнением 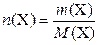 ,
,
Таблица 3.1 - Схемы некоторых гравиметрических определений(подробно [ ])
| Определяемый ион | Осадитель | Осаждаемая форма | Температура высушивания или прокаливания | Гравиметрическая форма |
| Ba2+ | H2SO4 | BaSO4 | 800 – 900°C | BaSO4 |
| SO42– | BaCl2 | BaSO4 | 800 – 900°C | BaSO4 |
| Fe3+ | NH3 (aq) | Fe(OH)3· n H2O | 800 – 900°C | Fe2O3 |
| Al3+ | NH3 (aq) C9H6NOH | Al(OH)3· n H2O Al(C9H6NO)3 | 1200°C 130°C | Al2O3 Al(C9H6NO)3 |
| Ca2+ | C2O42– | CaC2O4·H2O | 900 – 1200°C | CaO |
| Mg2+ | (NH4)2HPO4 | MgNH4PO4·6H2O | 1100°C | Mg2P2O7 |
| Ni2+ | C4H8O2N2 | Ni(C4H7O2N2) | 110 – 120°C | Ni(C4H7O2N2) |
можно записать 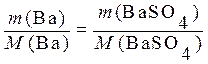 .
.
Отсюда: 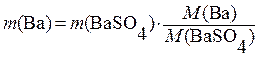 ,
,
где отношение молярной массы определяемого компонента к молярной массе гравиметрической формы осадка называют гравиметрическим фактором и обозначают буквой F. Следовательно,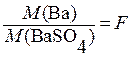 . Тогда можно записать:
. Тогда можно записать: 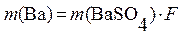 .
.
В общем случае массу определяемого компонента X в гравиметрическом анализе рассчитывают по формуле: m (X) = m (ГФ)∙ F, где m (ГФ) – масса гравиметрической формы осадка. Численные значения F для различных гравиметрических форм приведены в справочниках. При вычислении гравиметрического фактора необходимо учитывать стехиометрию реакции осаждения или термического превращения. Если в общем случае количества вещества определяемого компонента 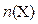 и его гравиметрической формы
и его гравиметрической формы  связаны стехиометрическим соотношением
связаны стехиометрическим соотношением 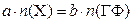 , то
, то 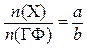 , где a и b стехиометрические коэффициенты. Гравиметрический фактор в этом случае выражается формулой:
, где a и b стехиометрические коэффициенты. Гравиметрический фактор в этом случае выражается формулой: 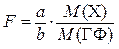
Таким образом гравиметрический фактор − это отношение молярной массы определяемого компонента к молярной массе гравиметрической формы с соответствующими стехиометрическими коэффициентами.
Например:
1) при определении магния в виде пирофосфата магния (ГФ) гравиметрический фактор вычисляют, исходя из схемы: 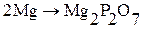
Поскольку в этом превращении a = 2, b = 1, то 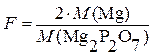 , то масса
, то масса
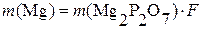
2) при расчете массы Fe3O4 по массе гравиметрической формы Fe2O3 исходят из схемы превращения:
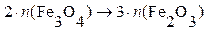
Здесь a = 2, b = 3, поэтому выражение для гравиметрического фактора имеет вид:
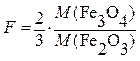 ,а масса
,а масса 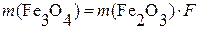 При анализе сложных по составу объектов часто необходимо рассчитать не массу, а массовую долю определяемого компонента ω (X)(% масс):
При анализе сложных по составу объектов часто необходимо рассчитать не массу, а массовую долю определяемого компонента ω (X)(% масс):
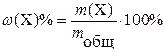

|
|
|
|
|
Дата добавления: 2014-01-11; Просмотров: 3507; Нарушение авторских прав?; Мы поможем в написании вашей работы!