
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Растворимость осадков под действием сильных кислот (при
|
|
|
|
заданном значении рН раствора)
Часто в состав осадка входит анион слабой двух‑ или трехоснόвной кислоты. При введении сильной кислоты в раствор, находящийся в динамическом равновесии с осадком, будут протекать следующие взаимодействия:
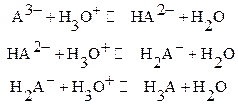
В результате этого концентрация свободного (несвязанного) аниона в растворе уменьшается и, в соответствии с вышерассмотренной схемой, начинается растворение осадка. Для количественного учета действия сильной кислоты необходимо предварительно рассчитать мольную долю свободных (не связанных) анионов (вывод уравнений в коллоквиум не входит):
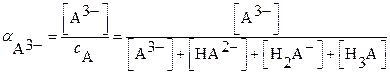
Значения [HA], [H2A] и [H3A] выражают через концентрационные константы ионизации кислоты и известные значения [H+] из соответствующих уравнений.
В расчетных формулах (кроме уравнений реакций) для упрощения вместо иона гидроксония Н3О+ обычно пишут Н+, подразумевая, что в растворе протон существует в сольватированном состоянии.
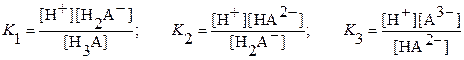
Откуда
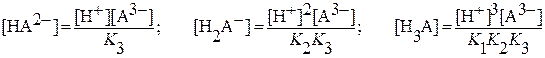
Подставив значения [HA2–],[H2A– ] и [H3A] в выражение для  , и после
, и после
очевидных преобразований получим: 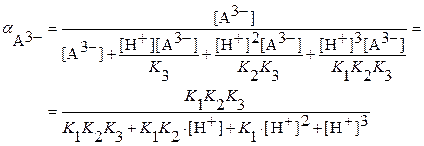
Это выражение для расчета значений  в случае образования осадка анионом слабой трехоснόвной кислоты.
в случае образования осадка анионом слабой трехоснόвной кислоты.
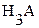 :
: 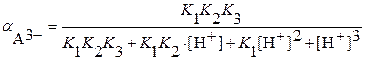 (3.21)
(3.21)
Аналогично, в случае образования осадка анионом слабой двухоснόвной кислоты
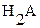 :
: 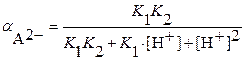 (3.22)
(3.22)
а для осадка, образованного анионом однооснόвной кислоты:
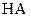 :
: 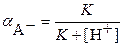 (3.23)
(3.23)
Пример: Рассчитать растворимость Ag2C2O4 в его насыщенном растворе при pH = 3.0 и сравнить с растворимостью в чистой воде (солевым эффектом пренебречь). Из справочных данных находим  . Для Н2С2О4 K 1 = 5.6·10–2 и K 2 = 5.4·10–5.
. Для Н2С2О4 K 1 = 5.6·10–2 и K 2 = 5.4·10–5.
Так как щавелевая кислота двухоснóвная, то в растворе присутствуют ионы 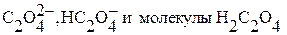 . Следовательно расчет мольной доли не протонированных оксалат – ионов
. Следовательно расчет мольной доли не протонированных оксалат – ионов
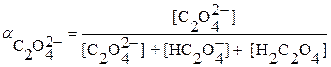
выполняется по уравнению (3.22):
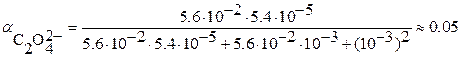
Далее расчет возможен по двум вариантам.
Вариант а) 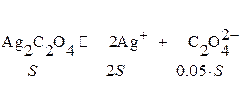
 ;
; 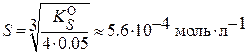
Вариант б) Согласно формуле (3.5) можно сразу записать 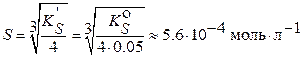
В насыщенном водном растворе (согласно формуле (3.4): 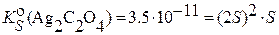 и растворимость осадка равна:
и растворимость осадка равна:
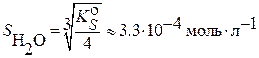
|
|
|
|
|
Дата добавления: 2014-01-11; Просмотров: 1488; Нарушение авторских прав?; Мы поможем в написании вашей работы!