
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Инверсионная вольтамперометрия
|
|
|
|
Результаты полярографических измерений иногда искажаются появлением так называемых полярографических максимумов, т.е. резким (в несколько десятков раз) превышением тока на отдельных участках вольтамперных кривых над предельным диффузионным током. Существует ряд причин возникновения этих максимумов. Полярографические максимумы первого рода (рис. 2.14.1) возникают в разбавленных растворах и вызываются неравномерным распределением потенциала вдоль электрода, (капли ртути). Это приводит к различию значений из-
 Р и с. 2.14.1. Полярографические максимумы I рода (1) и II рода (2).
Р и с. 2.14.1. Полярографические максимумы I рода (1) и II рода (2).
| быточной поверхностной энергии на разных участках поверхности и отсюда к тангенциальным движе-ниям жидкой поверхности ртути: сокращению участков с высокой избыточной энергией за счет расширения участков с низкой. В результате этих движений резко увеличивается конвективная диф-фузия реагентов к поверхности. Эти максимумы образуются только на некотором удалении от потенциала нулевого заряда и обычно имеют вид узких высоких пиков тока. |
Максимумы второго рода, наоборот, наблюдаются чаще в концентрированных растворах. Они охватывают более широкую область потенциалов, но меньше по высоте. Максимальная высота достигается вблизи точки нулевого заряда.
Причина их возникновения - тангенциальные движения поверхности ртутной капли, вызванные вытеканием ртути из капилляра (рис. 2.14.2):
| ртуть движется вниз по внутреннему объему капли и потом поднимается вдоль ее поверхности. Полярографические максимумы обоих родов могут быть устранены путем добавления поверхностно-активных органических веществ. Изменение адсорбции этих веществ, возникающее при тангенциальных движениях поверхности, оказывает резко тормозящее действие на эти движения. К таким веществам относятся агар-агар, желатин, столярный клей и др. Кроме того, максимумы первого рода устраняются применением достаточно концентрированных фонов. | 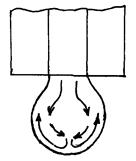 Р и с. 2.14.2. Схема дви
жения ртути в ртутной
капле.
Р и с. 2.14.2. Схема дви
жения ртути в ртутной
капле.
|
Наличие в растворе кислорода искажает полярограммы, так как он восстанавливается на катоде и дает две полярографические волны.
Одна волна (от 0,15 до 0,2 В) соответствует восстановлению кислорода до пероксида водорода, а другая (от -1,7 до -1,3 В) - восстановлению пероксида водорода до воды или группы ОН-. Кислород удаляют из испытуемого раствора пропусканием через него в течение 10...20 минут инертного газа (Ar, N2, He) или введением в раствор со щелочной или нейтральной средой сульфита натрия до 1г. Восстановление О2 и окисление сульфита до сульфата происходит в течение 2...5 минут.
Полярография с РКЭ характеризуется рядом достоинств:
1) чистота электрода вследствие постоянного обновления электрода в процессе капания ртути;
2) процессу анализа на РКЭ, по сравнению с платиновым электродом, практически не мешает восстановление ионов водорода;
3) возможность анализа растворов с малой концентрацией исследуемых веществ приблизительно (1...5) 10-5 моль/л и из пробы объемом до 1 мл;
4) классической полярографией можно обнаружить менее 0,01 мг исследуемого вещества с погрешностью ± 2 %.
Основными недостатками классической полярографии являются:
1) невозможность использования для анализа веществ, которые подвергаются только окислению, а не восстановлению, т.е. при потенциалах положительнее равновесного потенциала ртути в данном растворе (> 0,2 В);
2) невозможность резкого увеличения чувствительности из-за искажающего влияния тока заряжения РКЭ;
3) токсичность и неудобство в работе (например, в полевых условиях);
4) относительно большое время измерения (от 3 до 10 мин для одной пробы раствора).
Налаживание производств новых видов сверхчистых материалов, а также возрастающая острота экологических проблем потребовали разработки более чувствительных методов анализа, позволяющих обнаружить различные примеси с концентрацией 10-8 моль/л.
Для уменьшения влияния тока заряжения в современных полярографах предусмотрены электрические схемы для автоматической его компенсации и для непосредственной записи фарадеевского тока. Однако точность такой компенсации ограничена, особенно при малых концентрациях реагирующего вещества.
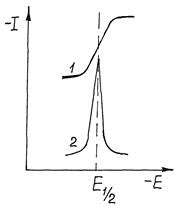 Р и с. 2.14.3. Интегральная (1)
и дифференциальная (2) полярограммы
Р и с. 2.14.3. Интегральная (1)
и дифференциальная (2) полярограммы
| В дифференциальной полярографии чувствительность и селективность классической полярографии можно повысить, если регистрировать зависимость от потенциала не тока, а его производной от потенциала (dI/dE). В этом случае вместо полярографической волны получают кривую с максимумом (рис. 2.14.3). Потенциал максимума соответствует потенциалу полуволны обычной полярограммы, а высота максимума пропорциональна концентрации исследуемого вещества. Сигнал, пропорциональный производной тока от потенциала, формируется в полярографе с помощью сравнительно простой электрической |
схемы. Для увеличения отношения полного сигнала (фарадеевский ток) к фону (ток заряжения) можно воспользоваться разной временной зависимостью фарадеевского тока I ф и тока заряжения I з при росте ртутной капли. Установлено, что I ф растет во времени пропорционально t 1/6, а ток заряжения падает пропорционально t -1/3. Таким образом, при отрыве капли соотношение I ф к I з максимально и условия измерения наиболее благоприятны. В методе так называемой таст-полярографии (от нем. tasten - зондировать) измерения тока проводят не непосредственно во время “ жизни “ капли, а только в течение короткого времени - 5...20 мс - перед отрывом капли. Этим способом удается чувствительность метода увеличить на порядок, т.е. до (1...5) 10-6 моль/л.
Амперометрическое титрование - это метод анализа, возникший на основе классической полярографии. В нем предельный диффузионный ток используют для нахождения точки эквивалентности при проведении титрования. Амперометрическое титрование возможно только при условии электроактивности (способности разряжаться на электроде) определяемого вещества или вещества титранта или хотя бы одного продукта их реакции. Для проведения амперометрического титрования аликвотную часть анализируемого раствора помещают в электролизер. В раствор опускают РКЭ или твердый (чаще всего платиновый) микроэлектрод и электрод сравнения. На электроды подают напряжение, отвечающее области предельного тока электроактивного вещества, и проводят титрование. После добавления из бюретки каждой отдельной порции титранта отмечают силу тока.
Пусть электроактивным является определяемое вещество, например, Pb2+, тогда добавление титранта (H2SO4), реагирующего с ним, будет уменьшать концентрацию определяемого вещества в растворе, в соответствии с этим будет уменьшаться и предельный диффузионный ток.
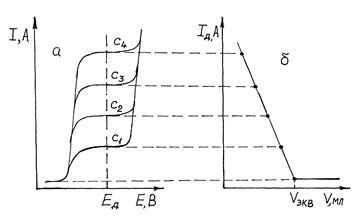
Р и с. 2.14.4. Схема получения кривой амперометрического
титрования (б)электроактивного определяемого вещества по
его полярограммам (а) при концентрациях  .
.
Поскольку предельный диффузионный ток, согласно уравнению
I д = К×С, пропорционален концентрации, то амперометрические кривые титрования, построенные в координатах I д - V, являются линейными (рис. 2.14.4). По ним графически находят объем титранта в точке эквивалентности (V экв).
Значение напряжения, при котором следует проводить титрование, предварительно устанавливают по полярограммам анализируемого раствора, титранта или раствора продуктов реакции.
Если электроактивным является вещество титранта, то ток останется практически равным нулю, пока не будет достигнута конечная точка титрования и не появится в растворе избыток титранта. Начиная с этого момента, ток будет расти. Такую кривую титрования можно получить, напри- мер, при титровании ионов цинка раствором K4[Fe(CN)6], окисляющегося на платиновом электроде (рис. 2.14.5, а).
Титрование возможно, если электроактивен образующийся продукт реакции определяемого вещества и титранта. Кривая титрования тогда имеет вид, изображенный на рис. 2.14.5, б.
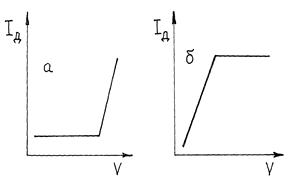 Р и с. 2.14.5. Кривые амперометрического титро-вания при электроактивном титранте (а) или про-дукта реакции титрования (б).
Р и с. 2.14.5. Кривые амперометрического титро-вания при электроактивном титранте (а) или про-дукта реакции титрования (б).
| Для амперометрического титрования пригодны реакции комплексообразования, оса-ждения, а также редокси-реакции. Концентрация титруемого раствора обычно порядка 10-3 моль/л. Определять мо-жно не только неорганические, но и органические вещества (например, фенолы). Метод значительно проще, экс- |
пресснее и доступнее полярографии и вольтам перометрии.
Инверсионная вольтамперометрия (вольтамперометрия с накоплением) - это метод, отличающийся от других не формой используемого импульса, а принципом проведения анализа. Исследуемое вещество сначала частично или полностью осаждают электрохимическим путем из пробы раствора на инертный электрод-подложку (стадия накопления, концентрирования). Чаще всего этот метод применяют для катионов металлов, которые катодно осаждают на стационарном (не капающем!) ртутном электроде или на платиновых, золотых, графитовых и т.д. твердых индифферентных электродах. На второй стадии, после извлечения ионов из раствора, электрод с пленкой осажденного металла подвергают анодной поляризации с линейно изменяющимся (с постоянной скоростью) потенциалом.
При превышении в ходе поляризации равновесного значения потенциала, отвечающего определяемому металлу, он начинает растворяться, причем тем активнее, чем больше поляризующее напряжение. Соответственно с этим растет регистрируемый самописцем-потенциометром ток растворения. Выходная кривая (вольтамперограмма) данного метода имеет вид кривой с максимумом, отвечающим окончанию растворения концентрата и выходу фронта растворения на поверхность индифферентного электрода (рис. 2.14.6).
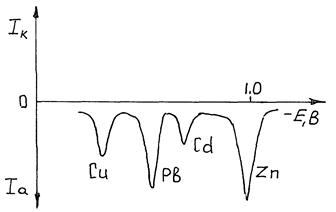
Р и с. 2.14.6. Инверсионная вольтамперограмма раствора, содер-
жащего цинк, кадмий, свинец и медь (фон 0,1 М НСООН,
Енакоп =1,2 В).
Положение и высота максимумов тока на вольтамперограмме характеризуют как природу, так и общее количество (концентрацию) исследуемого вещества. В присутствии нескольких определяемых веществ в специально подобранных условиях (фоновый электролит, потенциал накопления и т.д.) на кривой можно получить несколько максимумов тока, отвечающих каждому веществу. Данный метод чрезвычайно чувствителен - в отдельных случаях могут быть обнаружены примеси металлов с концентрацией 10-9 моль/л и даже ниже. Необходимо иметь в виду, что при очень малых концентрациях для полного осаждения ионов из раствора требуется значительное время накопления - иногда до одного часа, но этот недостаток компенсируется простотой применяемого оборудования. Для определения неизвестной концентрации применяют в основном метод стандартной серии или метод добавок.
|
|
|
|
|
Дата добавления: 2014-01-13; Просмотров: 1208; Нарушение авторских прав?; Мы поможем в написании вашей работы!