
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Пример 4. Разделить с помощью группового реагента катионы Al+3 и Mg+2
|
|
|
|
Пример 3
Разделить с помощью группового реагента катионы Al+3 и Mg+2.
Решение. Al+3 относится к катионам IV группы, а Mg+2 – V группы. Групповым реагентом на катионы IV и V групп является гидроксид натрия. В качестве аналитического сигнала наблюдается выпадение в осадок соответствующих гидроксидов:
Al+3 + 3ОН–⇄ Al(ОН)3↓;
Mg+2 + 2ОН– ⇄ Mg(ОН)2↓.
Однако при добавлении избытка реагента Al(ОН)3 растворяется с образованием комплексного соединения, а Mg(ОН)2 – нет:
Al(ОН)3 + NаОН ⇄ Nа[Al(ОН)4];
Mg(ОН)2 + NаОН ¹.
Таким образом, при разделении катион Al+3 будет находиться в фильтрате, а катион Mg+2 – в осадке.
Какой объём раствора AgNO3 с массовой долей 2 % потребуется для осаждения хлорида из навески СаСl2 ∙ 6 Н2О массой 0,4382 г?
Решение. Массу AgNO3 вычисляем на основании закона эквивалентов.
m (AgNO3) = m (СаСl2 ∙ 6Н2О) 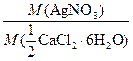 .
.
Подставляя числовые значения, получаем
m (AgNO3) = 0,4382 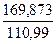 = 0,67 г.
= 0,67 г.
Плотность 2 %-го раствора AgNO3 близка к единице, поэтому можно записать пропорцию:
в 100 г (мл) раствора содержится 2 г AgNO3
в Vx (мл) раствора содержится 0,67 г AgNO3
Vx = 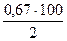 ≈ 34 мл.
≈ 34 мл.
Таким образом, для осаждения хлорида потребуется объём раствора AgNO3, равный Vx ≈ 34 мл.
Пример 5. Рассчитайте молярную массу эквивалента тетрабората натрия Na2B4O7 в реакции с НСl по схеме
Na2B4O7 + 2НСl + 5Н2О = 4Н3BO3 + 2NaСl.
Решение. Из уравнения реакции следует, что фактор эквивалентности тетрабората натрия равен
f = 1 /z = ½.
Следовательно, молярная масса эквивалента тетрабората натрия в данном случае равна
M э(1/2 Na2B4O7) = M (Na2B4O7)/2=201,219 / 2 =
= 100,610 г/моль.
Пример 6. Сколько мл 0,035 н раствора гидроксида натрия необходимо для нейтрализации 40 мл 0,2 н раствора соляной кислоты?
Решение. Так как вещества взаимодействуют в эквивалентных количествах, можно применить формулу
С н,к · V к = С н,щ · V щ,
где С н,к, С н,щ – молярные концентрации эквивалента кислоты и щелочи соответственно, V к, V щ – их объемы.
Определяем объем NaOH:
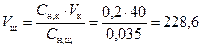 мл.
мл.
Таким образом, для нейтрализации 40 мл 0,2 н раствора соляной кислоты потребуется объем щелочи равный V щ = 228,6 мл.
Пример 7. Определить титр гидроксида натрия по уксусной кислоте, если концентрация рабочего раствора (NaOH) равна 0,01 н.
Решение. Находим титр NaOH по CH3COOH.
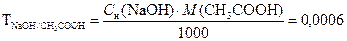 г/мл.
г/мл.
Таким образом, титр гидроксида натрия по уксусной кислоте равен 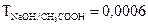 г/мл.
г/мл.
|
|
|
|
|
Дата добавления: 2014-11-06; Просмотров: 791; Нарушение авторских прав?; Мы поможем в написании вашей работы!