
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Фотометричне визначення феруму з о-фенантроліном
|
|
|
|
Реактиви
Апаратура
Спектрофотометр або фотоелектроколориметр (λ = 682 нм, червоний світлофільтр).
Кювети з товщиною поглинального шару 1 і 5 см.
Водяна баня.
Такі самі, як і при визначенні вмісту ортофосфатів (див. вище).
Персульфат калію К2SО4, х.ч. або ч.д.а.
Розчин сірчаної кислоти, 34%-й: 337 см3 концентрованої Н2SO4, х.ч., невеликими порціями доливають до 600 см3 дистильованої води і після охолодження доводять об'єм розчину до 1 дм3.
Розчин аміаку (1:1): 50 см3 концентрованого розчину NH4OH, х.ч., добавляють до 50 см3 дистильованої води.
Розчин α-динітрофенолу: 0,1 г динітрофенолу С6H4O5N2 розчиняють у 20 см3 95%-го етанолу і доводять об'єм розчину до 100 см3 дистильованою водою.
Фосфор органічних сполук
Вміст фосфору органічних сполук Сх (мг Р/дм3) обчислюють за рівнянням
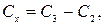
де С 3 − вміст загального розчиненого фосфору, мг Р/дм3; С2 − сумарний вміст орто- і поліфосфатів, мг Р/дм3.
Лабораторна робота № 5
Принци методу. Ферум є постійним компонентом природних вод. Він знаходиться в ступенях окиснення +2 та +3 і може бути як в розчиненому, так і в нерозчиненому стані. При низьких значеннях рН та електрохімічного потенціалу (Ео) домінують в природних водах сполуки феруму(ІІ) – Fe(Н2О)n2+, FeOH+, FeCO3 і його комплекси з органічними речовинами, в першу чергу з фульвокислотами. При підвищенні Ео і рН ≥ 6 характерним для поверхневих вод суші є наявність сполук феруму (III). В природних водах іони феруму (III) міцно зв’язуються в розчинні стійкі комплексні сполуки, в першу чергу з гуміновими та фульвокислотами. Загальний вміст заліза у поверхневих водах становить 0,01−15 мг/л.
О-фенантролін при рН 2-9 у присутності ЕДТА, який усуває заважаючий вплив інших металів, є практично специфічним реактивом для визначення феруму (ІІ). Комплексоутворення відбувається за схемою:
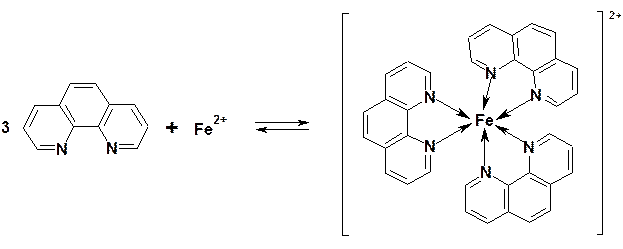
Іони феруму (Ш) з о-фенантроліном утворюють безбарвну сполуку, яка не заважає фотометричному визначенню Fe (ІІ). При визначенні загального вмісту заліза (ІІ, ІІІ) весь ферум попередньо відновлюють гідроксиламіном або іншим відновником для переведення його у ступінь окиснення +2. Межа визначення становить 0,05 мг/л.
Консервація:
· Для визначення вмісту форм слабкозв'язаного феруму використовують відфільтровану воду, законсервовану NaAc і HAc (по 2,5 мл NaAc і HAc на 100 мл води);
· Для визначення вмісту загального феруму використовують нефільтровану воду, законсервовану HNO3 (2,5 мл HNO3(конц.) на 100 мл води).
Реактиви:
(NH4)2Fe(SO4)2, стандартний розчин 0,005 мг Fe/мл;
О-фенантролін 0,28 % водний розчин, зберігають у склянці з темного скла на холоді;
NH2OH, 10 % водний розчин;
HCl (1: 9);
Універсальний індикаторний папірець;
NH3∙H2O, конц.;
NaOH, 10 М;
HNO3, конц.;
H2SO4, конц.
Апаратура:
1. Фотоелектроколориметр КФК-2;
2. Кварцеві кювети з l =5,0 cм. (2 шт.).
|
|
|
|
|
Дата добавления: 2014-11-06; Просмотров: 1263; Нарушение авторских прав?; Мы поможем в написании вашей работы!