
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Задачи для самостоятельного решения. 141. Вычислите рН растворов, если концентрации ионов ОН- (в моль/л) в них равны: а) 10-7; б) 5×10-12; в) 5×10-6
|
|
|
|
141. Вычислите рН растворов, если концентрации ионов ОН - (в моль/л) в них равны: а) 10-7; б) 5×10-12; в) 5×10-6.
142. Вычислите рН растворов следующих кислот, считая их диссоциацию на ионы полной:
а) СМ (HCl) = 0,002 моль/л; б) СМ (H2SO4) = 0,0025 моль/л.
143. Вычислите рН раствора, полученного прибавлением к 10 л воды концентрированной соляной кислоты объемом 2 мл (w (HCl) =3 6%, r = 1,19 г/мл). (Ответ: 2,63)
144. рН крови здорового человека составляет 7,35; желудочного сока составляет 1,5. Рассчитайте концентрацию ионов водорода в крови и в желудочном соке.
145. Вычислите рН раствора, в 100 мл которого содержится 0.1 г NaOH, считая диссоциацию щелочи полной.
146. Как изменится рН раствора HCl с концентрацией 0,1 моль/л, если его вдвое разбавить водой?
147. Смешали 100 мл раствора HCl с концентрацией 0,1 моль/л и 900 мл раствора этой же кислоты с концентрацией 0,01 моль/л. Вычислите рН полученного раствора, считая диссоциацию кислоты полной.
(Ответ: 1,72)
148. Рассчитайте рН желудочного сока, если массовая доля HCl в нем составляет 0,5 %. Плотность желудочного сока примите равной 1 г/см3. (Ответ: 0,86)
149. Среднее значение рН внеклеточной среды 7,4, а внутриклеточной составляет 6,9. Чему равно соотношение концентраций ионов водорода? (Ответ: в 3,16 раза больше внутри клеток)
150. Рассчитайте рН крови при 37 0С, если концентрация ОН - -ионов в этих условиях равна 5,63×10-7 моль/л.
151. Рассчитайте растворимость фторида кальция CaF2 в воде (в г/л), если 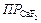 =3,9×10-11. (Ответ: 0,0167 г/л)
=3,9×10-11. (Ответ: 0,0167 г/л)
152. Рассчитайте массу карбоната кальция в его насыщенном при 25 0С растворе объемом 2,5 л.  =1×10-8. (Ответ: 0,0173 г)
=1×10-8. (Ответ: 0,0173 г)
153. Для растворения 1,16 г PbI2 при некоторой температуре потребовалось 2,5 л воды. Найдите произведение растворимости PbI2 при данной температуре. (Ответ: 4×10-9)
154. Вычислите объем воды, необходимый для растворения при 25 0С 1 г сульфата бария. 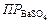 =1×10-8 (Ответ: 408 л)
=1×10-8 (Ответ: 408 л)
155. Будет ли образовываться осадок CaSO4 если к раствору, содержащему 0,02 моль/л CaCl2 прибавить равный объем раствора содержащего 0,2 моль/л Na2SO4? (Ответ: осадок образуется)
156. В 500 мл насыщенного при некоторой температуре раствора PbF2 содержится 245 мг растворенного вещества. Вычислите произведение растворимости PbF2. (Ответ: 3,2×10-8)
157. Произведение растворимости хромата серебра Ag2CrO4 при 250С равно 2×10-12. Выпадет ли осадок при смешении равных объемов растворов AgNO3 и K2CrO4 одинаковой концентрации, равной 0,01 моль/л? (Ответ: выпадет)
158. Произведение растворимости хлорида серебра AgCl равно 1,4×10-4 при 100 0С. Найдите растворимость (в г/л) AgCl в кипящей воде. (Ответ: 1,70 г/л)
159. Выпадет ли осадок PbSO4, если к 1 л раствора H2SO4 c концентрацией 0,001 моль/л добавить твердый Pb(NO3)2 количеством 0,002 моль, полностью переходящий в раствор? 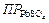 =1,7×10-8.
=1,7×10-8.
(Ответ: да)
160. Вычислите и сравните растворимость CaCO3 в чистой воде и в растворе соды Na2CO3 концентрации 0,1 моль/л.  = 1×10-8.
= 1×10-8.
(Ответ: 1,7×10-5)
Раздел 9
|
|
|
|
|
Дата добавления: 2014-11-07; Просмотров: 1796; Нарушение авторских прав?; Мы поможем в написании вашей работы!