
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Химические свойства. 1. Взаимодействие кислотного оксида с водой (для кислородсодержащих кислот):
|
|
|
|
Получение
1. Взаимодействие кислотного оксида с водой (для кислородсодержащих кислот):
SO3 + H2O  H2SO4
H2SO4
P2O5 + 3H2O  2H3PO4
2H3PO4
2. Взаимодействие водорода с неметаллом и последующим растворением полученного продукта в воде (для бескислородных кислот):
H2 + Cl2  2HCl
2HCl
H2 + S  H2S
H2S
3. Реакциями обмена соли с кислотой
Ba(NO3)2 + H2SO4  BaSO4
BaSO4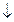 + 2HNO3
+ 2HNO3
в том числе, вытеснение слабых, летучих или малорастворимых кислот из солей более сильными кислотами:
Na2SiO3 + 2HCl  H2SiO3
H2SiO3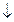 + 2NaCl
+ 2NaCl
2NaCl(тв.) + H2SO4(конц.)  Na2SO4 + 2HCl
Na2SO4 + 2HCl
1. Действие на индикаторы.
акмус – красный, метилоранж - розовый
2. Взаимодействие с основаниями (реакция нейтрализации):
H2SO4 + 2KOH  K2SO4 + 2H2O
K2SO4 + 2H2O
2HNO3 + Ca(OH)2  Ca(NO3)2 + 2H2O
Ca(NO3)2 + 2H2O
3. Взаимодействие с основными оксидами:
CuO + 2HNO3  Cu(NO3)2 + H2O
Cu(NO3)2 + H2O
4. Взаимодействие с металлами:
Zn + 2HCl  ZnCl2 + H2
ZnCl2 + H2
2Al + 6HCl  2AlCl3 + 3H2
2AlCl3 + 3H2
(металлы, стоящие в ряду напряжений до водорода, кислоты-неокислители).
Взаимодействие с солями (реакции обмена), при которых выделяется газ или образуется осадок:
H2SO4 + BaCl2  BaSO4
BaSO4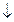 +2HCl
+2HCl
2HCl + K2CO3  2KCl + H2O + CO2
2KCl + H2O + CO2
|
|
|
|
|
Дата добавления: 2014-10-22; Просмотров: 515; Нарушение авторских прав?; Мы поможем в написании вашей работы!