
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Пример решения 3.1
|
|
|
|
Пусть по условию задачи в реакцию вступает 20 г алюминия. При взаимодействии с кислородом выделяется 619,85 кДж тепла (Q).
Энтальпией образования (Δ H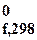 ) сложного соединения называется тепловой эффект образования 1 моля этого соединения из простых веществ, взятых в устойчивом состоянии при стандартных условиях. Единицей измерения является кДж/моль.
) сложного соединения называется тепловой эффект образования 1 моля этого соединения из простых веществ, взятых в устойчивом состоянии при стандартных условиях. Единицей измерения является кДж/моль.
Записываем уравнение химической реакции
4 Al (тв) + 3 O2 = 2 Al2O3 (тв).
Определяем количество тепла (Q) для одного моля соединения, для этого проводим сокращение и получаем
2 Al (тв) + 3/2 O2 (г) = Al2O3 (тв).
По условию задачи:
при соединении 20 г алюминия выделяется 619,85 кДж
при соединении 2-х молей алюминия, т.е. 2×27, выделяется Q кДж
Q = 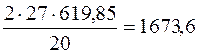 кДж.
кДж.
Так как тепло выделяется, то энтальпия системы уменьшается
Δ H 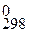 = - 1673,6 кДж/моль.
= - 1673,6 кДж/моль.
Следовательно, реакция образования оксида Al2O3 является экзотермической.
Задание 3.2. Для приведенной по варианту реакции (табл. III.2) рассчитайте: Δ H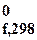 (кДж), Δ S
(кДж), Δ S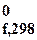 (Дж/К), Δ G
(Дж/К), Δ G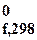 (кДж) химической реакции, вероятность ее протекания при Р = 101,3 кПа и Т = 298 К и температуру начала реакции.
(кДж) химической реакции, вероятность ее протекания при Р = 101,3 кПа и Т = 298 К и температуру начала реакции.
|
|
|
|
|
Дата добавления: 2014-10-23; Просмотров: 751; Нарушение авторских прав?; Мы поможем в написании вашей работы!