
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Квантовые числа
|
|
|
|
| Положение электрона в атоме описывается набором из четырех квантовых чисел. Охарактеризовать электронное строение атома – это значит указать значения четырех квантовых чисел для всех его электронов. | |
| Главное квантовое число (n) определяет размер электронного облака, размер орбитали, номер энергетического уровня и энергию электрона на данном уровне, соответствует номеру периода в таблице Менделеева. | У атомов элементов первого периода – один энергетический уровень (n = 1), второго периода – 2 уровня (n = 2), третьего – 3 уровня (n = 3) и т.д. |
Орбитальное квантовое число (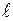 ) характеризует энергию электрона на данной орбитали (энергетическом подуровне) ) характеризует энергию электрона на данной орбитали (энергетическом подуровне) 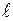 = 0, 1, 2,...(n – 1). Оказалось, что в пределах одного квантового слоя электроны могут образовывать облака различной формы. = 0, 1, 2,...(n – 1). Оказалось, что в пределах одного квантового слоя электроны могут образовывать облака различной формы.
| Число орбиталей равно числу значений 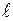 на данном энергетическом уровне.
Если на данном энергетическом уровне.
Если 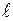 = 0 (s-электроны), то орбиталь имеет сферическую форму; = 0 (s-электроны), то орбиталь имеет сферическую форму; 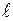 = 1 (р-электроны) – гантелеобразную; = 1 (р-электроны) – гантелеобразную; 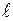 = 2 (d-электроны) – форму четырех лепестковой розы. = 2 (d-электроны) – форму четырех лепестковой розы.
|
Число n обозначается цифрой, а 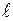 строчной буквой: 0 – s, 1 – р, 2 – d, 3 – f. Число электронов для данного строчной буквой: 0 – s, 1 – р, 2 – d, 3 – f. Число электронов для данного 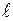 указывается индексом сверху.
Например: Бор – 5В 1s22s22р1 – это означает, что в атоме бора есть 2 электрона, у которых n = 1, а указывается индексом сверху.
Например: Бор – 5В 1s22s22р1 – это означает, что в атоме бора есть 2 электрона, у которых n = 1, а 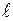 = 0; 2 электрона с n = 2 и = 0; 2 электрона с n = 2 и 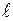 = 0, и 1 электрон с n = 2 и = 0, и 1 электрон с n = 2 и 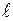 = 1. = 1.
| |
Магнитное квантовое число (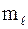 ) характеризует энергию электрона на данной ориентации орбитали и принимает значения – ) характеризует энергию электрона на данной ориентации орбитали и принимает значения –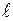 , 0, , 0, 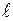 ; ;
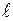 = n –1.
Допускаются лишь строго определенные ориентации электронных облаков в пространстве. = n –1.
Допускаются лишь строго определенные ориентации электронных облаков в пространстве.
| Число возможных значений 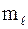 для данного значения определяет число возможных ориентации данного облака в пространстве. Так, s-облако имеет 1 ориентацию, р – 3 ориентаций, d – 5 ориентаций, а f – 7 ориентаций. для данного значения определяет число возможных ориентации данного облака в пространстве. Так, s-облако имеет 1 ориентацию, р – 3 ориентаций, d – 5 ориентаций, а f – 7 ориентаций.
|
| ms – магнитное спиновое числохарактеризует собственный момент количества движения электрона, в результате вращения вокруг собственной оси. Такое движение называется спином. Спин – это собственный момент импульса электрона, не связанный с движением в пространстве. | Для всех электронов абсолютное значение спина всегда равно s=1/2. Проекция спина на ось z (магнитное спиновое число ms) может иметь лишь два значения: ms = +1/2 или ms = –1/2. |
|
|
|
|
|
Дата добавления: 2014-10-31; Просмотров: 309; Нарушение авторских прав?; Мы поможем в написании вашей работы!