
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Визначте максимальну кількість електронів на четвертому енергетичному рівні
|
|
|
|
Елементи, в яких валентні електрони знаходяться на s – орбіталі, називають s-елементами. До них відносять елементи І А та ІІ А груп. Загальна електронна формула верхнього енергетичного рівня для цих елементів ns1 або ns2. Наприклад, атом Натрію має таку електронну будову:
+11 Na 1s22s22p63s1
Елементи, в яких валентні електрони знаходяться на р-орбіталі, називають р-елементами. До групи р-елементів належать елементи IIIA, IVA, VA, VIA, VIIA, VIIIA груп періодичної системи елементів. Для них характерна електронна конфігурація ns2np1-6. Наприклад, для атому Фосфору характерна наступна електронна будова:
+ 15 Р 1s22s 22p63s23p3
Елементи, в атомах яких валентні електрони знаходяться на d-орбіталі, називають d-елементами. Біоелементам з родини d-елементів відповідає загальна формула ns2(n-1)d1-10. Наприклад, для атому Мангану характерна така електронна будова:
+25 Mn 1s22s22p63s23p64s23d5
Елементи, для яких характерно заповнення електронами f-орбіталі називають f-елементами. Електронна будова із заповненням f-підрівня характерна для лантаноїдів та актиноїдів. Для більш повного уявлення про розподіл електронів на енергетичних рівнях та підрівнях користуються електронно-графічними формулами. Вони показують розташування електронів не тільки на рівнях та підрівнях, а й на атомних орбіталях. Наприклад, представимо електронно-графічні формули для атомів елементів родини s-, p-, d- елементів.
Літій Li – представник родини s-елементів (мал.2). Електронна формула s-елемента Літія Li: 1s22s2.
Енергетични рівні (Е) 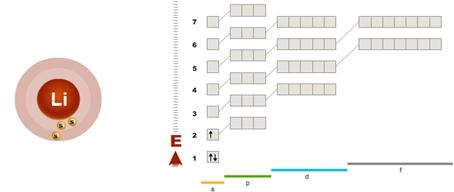
Орбіталі (s-, p-, d-, f-)
Мал. 2. Електронна будова атому Літію
Нітроген N -представник родини р-елементів (мал.3). Електронна формула р-елемента Нітрогену N: 1s22s22р3.
Енергетичні рівні(Е)
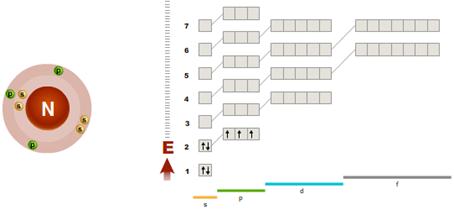 |
Орбіталі (s-, p-, d-, f-)
Мал. 3. Електронна будова атому Нітрогену
Манган Mn – представник родини d-елементів (мал.4). Електронна формула d –елемента Мангану Mn: 1s22s22p63s23p64s23d5.
Енергетичні рівні(Е)
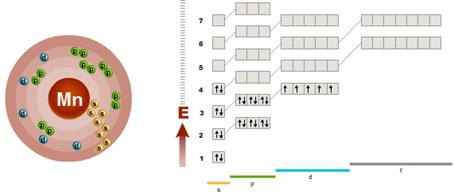 |
Орбіталі(s-, p-, d-, f-)
Мал. 4. Електронна будова атому Мангану
|
|
|
|
|
Дата добавления: 2014-11-25; Просмотров: 1968; Нарушение авторских прав?; Мы поможем в написании вашей работы!