
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Внутримолекулярное окисление-восстановление
|
|
|
|
Окислительно-восстановительные свойства пероксида водорода
Поскольку в молекулах пероксида водорода атомы кислорода находятся в промежуточной степени окисления (–1), то это вещество, в зависимости от условий, может окисляться до простого вещества кислорода (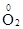 ), восстанавливаться до воды (
), восстанавливаться до воды (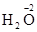 ) или диспропорционировать с одновременным образованием указанных веществ. Стандартные потенциалы соответствующих полуреакций:
) или диспропорционировать с одновременным образованием указанных веществ. Стандартные потенциалы соответствующих полуреакций:
Окисление H2O2 до простого вещества кислорода:
H2O2 – 2e– → О2 + 2H+ ; E ° = 0,68 B.
Восстановление H2O2 до воды:
H2O2 + 2H+ + 2e– → 2H2O; E ° = 1,78 B.
Если в составвещества входят одновременно частицы-восстановители и частицы-окислители, оно может подвергаться внутримолекулярному окислению-восстановлению. К таким реакциям относится, например, реакция термического разложения дихромата аммония (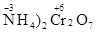 . При нагревании этого вещества начинается ОВР за счёт того, что содержащиеся в нём частицы
. При нагревании этого вещества начинается ОВР за счёт того, что содержащиеся в нём частицы 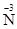 являются восстановителями, а частицы
являются восстановителями, а частицы 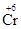 – окислителями.
– окислителями.
|
|
|
|
|
Дата добавления: 2014-11-25; Просмотров: 960; Нарушение авторских прав?; Мы поможем в написании вашей работы!