
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Электролиз растворов и расплавов электролитов. Электродные правила
|
|
|
|
В электрохимии стандартный электродный потенциал, обозначаемый Eo, E0, или EO, является мерой индивидуального потенциала обратимого электрода (в равновесии) в стандартном состоянии, которое осуществляется в растворах при эффективной концентрации в 1 моль/кг и в газах при давлении в 1 атмосферу или 100 кПа (килопаскалей).
Объёмы чаще всего взяты при 25 °C. Основой для электрохимической ячейки, такой как гальваническая ячейка всегда является окислительно-восстановительная реакция, которая может быть разбита на две полуреакции: окисление на аноде (потеря электрона) и восстановление на катоде (приобретение электрона). Электричество вырабатывается вследствие различия электростатического потенциала двух электродов. Эта разность потенциалов создаётся в результате различий индивидуальных потенциалов двух металлов электродов по отношению к электролиту.
Совокупность окислительно-восстановительных реакций, которые протекают на электродах в растворах или расплавах электролитов при пропускании через них электрического тока, называют электролизом.
1. На аноде могут протекать следующие процессы:
а) при электролизе растворов содержащих в своем составе анионы F-, SO42-, NO3-, PO43-, а также растворов щелочей, происходит окисление аниона кислорода: 2H2O - 4e = O2 + 4H+. (4OH- - 4e = O2 + 2H2O)
б) при окислении анионов Cl-, Br-, I- выделяется соответственно хлор, бром, йод: 2Cl- - 2e = Cl2
в) при окислении анионов органических кислот происходит процесс: 2RCOO- = R-R + 2CO2.
2. При электролизе растворов солей, содержащих ионы, расположенные в ряду напряжений левее Al3+, на катоде выделяется водород: 2H2O + 2e = H2 + 2OH-. Если ион расположен в ряду напряжений правее водорода, то на катоде выделяется металл.
3. При электролизе растворов солей, содержащих ионы, расположенные в ряду напряжений между Al3+ и H+, на катоде могут протекать конкурирующие процессы, как восстановление катионов, так и выделение водорода.
4. Активные металлы (в ряду напряжений от Li до Al) получают электролизом расплава солей.
23. Предмет и задачи аналитической химии. Методы количественного анализа: химические, физико-химические, физические
Основная цель аналитической химии - обеспечить в зависимости от поставленной задачи точность, высокую чувствительность, экспрессность и (или) избирательность анализа. Разрабатываются методы, позволяющие анализировать микрообъекты (смотри Микрохимический анализ), проводить локальный анализ(в точке, на поверхности и т.д.), анализ без разрушения образца (см. Неразрушающий анализ), на расстоянии от него (дистанционный анализ), непрерывный анализ (например, в потоке), а также устанавливать, в виде какого химического соединения и в составе какой фазы существует в образце определяемый компонент (фазовый анализ). Важные тенденции развития аналитической химии - автоматизация анализов, особенно при контроле технологических процессов и математизация, в частности широкое использование ЭВМ.
Структура. Можно выделить три крупных направления аналитической химии: общие теоретические основы; разработка методов анализа; аналитическая химия отдельных объектов. В зависимости от цели анализа различают качественный анализи количественный анализЗадача первого - обнаружение и идентификация компонентов анализируемого образца, второго - определение их концентраций или масс. В зависимости от того, какие именно компоненты нужно обнаружить или определить, различают изотопный анализ, элементный анализ, структурно-групповой (в т. ч. функциональный анализ), молекулярный анализ, фазовый анализ. По природе анализируемого объекта различают анализ неорганических и органических веществ.
В теоретич. основах аналитической химии существенное место занимает метрология химического анализа, в том числе статистическая обработка результатов. Теория аналитической химии включает также учение об отборе и подготовкеаналитических проб. о составлении схемы анализа и выборе методов, принципах и путях автоматизации анализа, применения ЭВМ, а также основы народнохозяйств. использования результатов хим. анализа. Особенность аналитической химии - изучение не общих, а индивидуальных, специфических свойств и характеристик объектов, что обеспечивает избирательность мн. аналитичекских методов. Благодаря тесным связям с достижениями физики, математики, биологии и разл. областей техники (это особенно касается методов анализа) аналитическая химия превращена в дисциплину на стыке наук.
В аналитической химии различают методы разделения, определения (обнаружения) и гибридные, сочетающие методы первых двух групп. Методы определения подразделяют на химические методы анализа (гравиметрический анализ, титриметрия), физико-химические методы анализа (например, электрохимические, фотометрические, кинетические),физические методы анализа (спектральные, ядерно-физические и другие) и биологические методы анализа. Иногда методы определения делят на химические, основанные на химических реакциях, физические, базирующиеся на физических явлениях, и биологические, использующие отклик организмов на изменения в окружающей среде.
Аналитическая химия определяет общий подход к выбору путей и методов анализа. Разрабатываются способы сопоставления методов, условия их взаимозаменяемости и сочетания, принципы и пути автоматизации анализа. Для практич. использования анализа необходима разработка представлений о его результате как показателе качества продукции, учение об экспрессном контроле технол. процессов, создание экономичных методов. Большое значение для аналитиков, работающих в различных отраслях народного хозяйства, имеет унификация и стандартизация методов. Разрабатывается теория оптимизации кол-ва информации, необходимой для решения аналитической задачи.
Методы анализа. В зависимости от массы или объема анализируемого образца методы разделения и определения иногда подразделяют на макро-, микро- и ультрамикрометоды.
К разделению смесей обычно прибегают в тех случаях, когда методы прямого определения или обнаружения не позволяют получить правильный результат из-за мешающего влияния других компонентов образца. Особенно важно так называемое относительное концентрирование - отделение малых количеств определяемых компонентов от значительно больших количествв основных компонентов пробы. Разделение смесей может базироваться на различии в термодинамических, или равновесных, характеристиках компонентов (константы обмена ионов, константы устойчивости комплексов) или кинетических параметров. Для разделения применяют главным образом хроматографию, экстракцию, осаждение, дистилляцию, а также электрохимические методы, например электроосаждение.
Физико-химические методы анализа, основаны на зависимости физических свойств вещества от его природы, причем аналитический сигнал представляет собой величину физического свойства, функционально связанную сконцентрацией или массой определяемого компонента. Физико-химические методы анализа могут включать химические превращения определяемого соединения, растворение образца, концентрирование анализируемого компонента, маскирование мешающих веществ и других. В отличие от «классических» химических методов анализа, где аналитическим сигналом служит масса вещества или его объем, в физико-химические методы анализа в качестве аналитического сигнала используют интенсивность излучения, силу тока, электропроводность, разность потенциалов и др.
Важное практическое значение имеют методы, основанные на исследовании испускания и поглощения электромагнитного излучения в различных областях спектра. К ним относится спектроскопия (например, люминесцентный анализ, спектральный анализ, нефелометрия и турбидиметрия и другие). К важным физико-химическим методам анализа принадлежат электрохимические методы, использующие измерение электрических свойств вещества.
24. Основные положения теории электролитической диссоциации. Количественные характеристики процесса диссоциации:константа и степень ионизации. Закон разбавления В.Оствальда
Электролитическая диссоциация — процесс распада электролита на ионы при его растворении или плавлении.
Диссоциация на ионы в растворах происходит вследствие взаимодействия растворённого вещества с растворителем; по данным спектроскопических методов, это взаимодействие носит в значительной мере химический характер. Наряду ссольватирующей способностью молекул растворителя определённую роль в электролитической диссоциации играет также макроскопическое свойство растворителя — его диэлектрическая проницаемост Константа диссоциации — вид константы равновесия, которая показывает склонность большого объекта диссоциировать(разделяться) обратимым образом на маленькие объекты, как например когда комплекс распадается на составляющиемолекулы, или когда соль разделяется в водном растворе на ионы. Константа диссоциации обычно обозначается 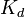 и обратнаконстанте ассоциации. В случае с солями, константу диссоциации иногда называют константой ионизации.
и обратнаконстанте ассоциации. В случае с солями, константу диссоциации иногда называют константой ионизации.
В общей реакции 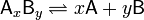 , где комплекс
, где комплекс 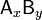 разбивается на x единиц A и y единиц B, константа диссоциации определяется так:
разбивается на x единиц A и y единиц B, константа диссоциации определяется так:
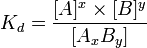
где [A], [B] и [AxBy] — концентрации A, B и комплекса AxBy соответственно.
1. Электролиты при растворении в воде распадаются (диссоциируют) на ионы – положительные и отрицательные.
2. Под действием электрического тока ионы приобретают направленное движение: положительно заряженные частицы движутся к катоду, отрицательно заряженные – к аноду. Поэтому положительно заряженные частицы называются катионами, а отрицательно заряженные – анионами.
3. Направленное движение происходит в результате притяжения их противоположно заряженными электродами (катод заряжен отрицательно, а анод – положительно).
4. Ионизация – обратимый процесс: параллельно с распадом молекул на ионы (диссоциация) протекает процесс соединения ионов в молекулы (ассоциация).
Степень ионизации и молекулярная масса лекарственного средства - через плаценту хорошо проникают неионизированные лекарственные средства с небольшой молекулярной массой (этиловый спирт, сульфаниламиды, непрямые антикоагулянты и др.), а высокоионизированные вещества и (или) вещества с большой молекулярной массой (гепарин, инсулин и др.) через плаценту проникают плохо или вообще не проникают.
Морфофункциональная зрелость плаценты. По мере увеличения срока беременности происходят выраженные изменения в структуре плаценты. При этом тканевый слой, находящийся между капиллярной сетью плода и материнским кровотоком, толщина которого в ранние сроки беременности 25 мк, уменьшается до 2 мк к концу беременности, что увеличивает трансплацентарный переход лекарственных средств (в основном, за счет их пассивного транспорта).
Метаболическая функция плаценты, которая проявляется биотрансформацией ряда лекарственных веществ в плаценте, поэтому к плоду возможно проникновение не только лекарственных средств, но и их метаболитов.
Интенсивность маточно-плацентарного кровотока и фегоплацентарного кровотока.
В свою очередь, на уровень маточно-плацентарного кровотока могут влиять лекарственные средства, которые разделены на 2 группы.
Закон разбавления Оствальда - соотношение, выражающее зависимость эквивалентной электропроводностиразбавленного раствора бинарного слабого электролита от концентрации раствора:
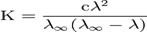
Здесь К — константа диссоциации электролита, с — концентрация, λ и λ∞ — значения эквивалентной электропроводности соответственно при концентрации с и при бесконечном разбавлении. Соотношение является следствием закона действующих масс и равенства
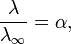
где α — степень диссоциации.
Закон разбавления Оствальда выведен им в 1888 и им же подтвержден опытным путём. Экспериментальное установление правильности закона разбавления Оствальда имело большое значение для обоснования теории электролитической диссоциации.
|
|
|
|
|
Дата добавления: 2014-11-25; Просмотров: 881; Нарушение авторских прав?; Мы поможем в написании вашей работы!