
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Невозможен вечный двигатель первого рода (двигатель, совершающий работу без затраты энергии)
|
|
|
|
Полная энергия изолированной системы постоянна;
Энергия неуничтожаема и несотворяема; она может только переходить из одной формы в другую в эквивалентных соотношениях;
Элементарную работу dW обычно записывают в виде двух слагаемых:
dW = dW¢ + pdV (2)
где dW¢ - элементарная полезная работа,
pdV - элементарная работа расширения, она относится к случаю, когда система сама совершает работу против внешнего давления.
Если система совершает работу только против внешнего давления, тогда d W ¢ = 0 и d W = pdV. В дальнейшем будем рассматривать именно такие системы.
В общем случае выражение первого закона термодинамики в дифференциальной форме можно записать как:
dQ = dU + pdV (3)
Интегральная форма записи первого закона термодинамики имеет вид:
Q = DU + W или (4)
DU = Q – W (5)
При р = const:
Q = DU + pDV (6)
Рассмотрим приложение первого начала термодинамики для определения работы расширения, причем будем рассматривать простейший случай – работу расширения идеального газа:
– Изохорный процесс
Поскольку работа расширения равна произведению давления на изменения объема (ΔV = 0) получаем:
 (7)
(7)
∆U = Qv (8)
Таким образом, тепловой эффект изохорного процесса равен изменению внутренней энергии системы.
– Изотермический процесс
С учетом уравнения состояния идеального газа 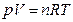 получаем:
получаем:
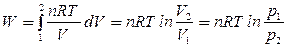 (9)
(9)
Внутренняя энергия идеального газа зависит только от температуры, поэтому ∆U = 0 и для теплового эффекта имеем
 (10)
(10)
– Изобарный процесс
 (11)
(11)
|
|
|
|
|
Дата добавления: 2014-11-16; Просмотров: 460; Нарушение авторских прав?; Мы поможем в написании вашей работы!