
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Характеристика вагонов 81-717(714) 13 страница
|
|
|
|
114. Структурообразование в дисперсных системах. Физико-химическая механика твердых тел и дисперсных структур. Как указывалось в § 105, дисперсные системы разделяют на две большие группы: свободнодисперсные, или неструктурированные, и связно-дисперсные, или структурированные системы. Последние образуются в результате возникновения контактов между дисперсными частицами. Особенности этих контактов зависят от природы, величины, формы, концентрации дисперсных частиц, а также от их распределения по размерам и взаимодействия с дисперсионной средой.
| *Петр Александрович Ребиндер (1898—1972) — советский фи-зико-химик, академик, Герой Социалистического Труда, лауреат Государственных премий, основатель крупной научной школы в области физической химии дисперсных систем. Разработанные им пути управления свойствами дисперсных систем, процессами их образования и разрушения тесно связаны с решением крупных технических задач. |
На рис. 104 схематично показаны виды возможных контактов между частицами в структурированных дисперсных системах. Выделяют два, резко различающихся по своим свойствам, типа пространственных структур, названных П. А. Ребиндером ко а гул я -ционными и конденсационными структурами. Основное различие этих структур состоит в неодинаковой природе контакта между частицами дисперсной фазы. В коагуляционных структурах этот контакт осуществляется или через очень тонкие прослойки дисперсионной среды (рис. 104, а) и точечные контакты (рис. 104, в)', или при участии макромолекул (рис. 104,6). Конденсационные структуры возникают как результат склеивания, сваривания, срастания частиц дисперсной фазы на отдельных участках поверхности (рис. 104, г).

Коагуляционные пространственные структуры образуются из с$ободнодисперсных систем, когда дисперсионное притяжение Между частицами преобладает над электростатическим отталкиванием. Ё этом случае энергия результирующего взаимного притяжения частиц сравнима с энергией их теплового броуновского Движения.
На первых этапах коагуляционного взаимодействия возникают агрегаты из двух, трех, а иногда и цепочки первичных дисперсных частиц; коллоидный раствор сохраняет текучесть, так как развитие структуры не дошло до образования непрерывной сетки. Возникает жидкообразная коагуляционная структура (соответствующая стадии скрытой коагуляции, см. § 113). В потоке жидкости агрегаты распадаются и внствь образуются; каждой скорости потока соответствует своя равновесная величина агрегатов, а следовательно, и оказываемого ими сопротивления потоку жидкости. Поэтому возникновение пространственных структур в растворах обнаруживается по изменению вязкости в зависимости от скорости потока жидкости *.
Дальнейший рост агрегатов приводит к образованию коагулята (седимента) или геля (рис. 89 на Стр. 300). Возникает твердооб-разная пространственная коагуляционная структура, которая может быть плотной или рыхлой.
| * Для обычных жидкостей в условиях ламинарного (послойного) потока вязкость (коэффициент внутреннего треиия) не завист от скорости течения жидкости. |
Плотная структура (рис. 89, б) возникает, когда частицы дисперсной фазы укладываются в осадке наиболее плотно, «скользя» друг относительно друга; если первичные частицы соединяются в цепочки, то коагуляционная структура будет рыхлой — «арочной» (рис. 89, в). Образованию геля (рис. 89, а) особенно благоприятствует вытянутая форма частиц дисперсной фазы, но при больших концентрациях гелеобразование возможно и в случае сферических частиц, если они склонны к цепочкообразованию.
Свежеполученные коагуляты во многих случаях способны вновь переходить в состояние золя. Такой изотермический переход коагулят->золь называют пептизацией, а вызывающие его вещества — п е пт из а то р а м и. Пептизаторы являются стабилизаторами дисперсных систем и могут быть веществами как ионной (электролиты), так и молекулярной природы. Адсорбируясь на поверхности первичных частиц, пептизаторы ослабляют взаимодействие между ними, что приводит к распаду агрегатов и переходу коагулята в состояние золя. Пептизацию часто наблюдают при промывании дистиллированной водой находящихся на фильтре свежеполученных осадков гидроксидов и сульфидов металлов. Промывание дистиллированной водой уменьшает концентрацию электролитов, что приводит к изменению структуры двойного электрического слоя — часть противоионов переходит из адсорбционного в диффузный слой, возрастает электрокинетический потенциал частиц коагулята. В результате осадок гидроксида или сульфида на фильтре уменьшается — пептизируется, проходя через поры фильтра в виде золя.
Обычно пептизируемость коагулятов уменьшается со временем в результате развития точечных контактов между первичными частицами; происходит упрочнение коагуляционных структур. Подобное самопроизвольное изменение свойств коллоидных растворов, коагулятов, студней и гелей называют старением коллоидов. Оно проявляется в агрегации частиц дисперсной фазы, в уменьшении их числа и степени их сольватации (в случае водных растворов — гидратации), а также в уменьшении поверхности раздела между фазами и адсорбционной способности.
Коагуляционные структуры обладают определенным комплексом механических свойств, обусловленным тонкими прослойками дисперсионной среды на участках контактов частиц дисперсной фазы. Сетчатый каркас из дисперсных частиц удерживается за счет межмолекулярных сил, которые невелики. Поэтому прочность коагуляционных структур незначительна.
Для коагуляционных структур, образованных частицами вытянутой или пластинчатой формы, а также цепочечными агрегатами, характерна т и к с о -тропия (от греч, «тиксис»— встряхивание, «трепо»— изменяется). Так называют обратимое разрушение структуры с переходом в текучее состояние при механических воздействиях, например при встряхивании, и самопроизвольное восстановление структуры, «отвердевание» в покое. Тиксотропность может быть полезным свойством: например, масляные краски, будучи разжижены механическим воздействием, не стекают с вертикальных поверхностей в результате тиксотропного структурирования.
Коагуляционные структуры проявляют структурную вязкость, т. е. изменение вязкости от предельно высоких значений, когда структура еще не разрушена, до предельно низких величии прн полном разрушении структуры и ориентации частиц их длинной осью по направлению потока жидкости. Различие между этими предельными значениями вязкости может достигать 108—109 раз. Высококоицентрированные коагуляционные структуры (пасты) пластичны, т. е. их деформация необратима,
При высушивании материалов, имеющих коагуляционпую структуру, коагуляционные контакты переходят в точечные, прочность материала быстро возрастает, но он теряет пластичность. Оводнение такого высушенного материала (например, бумажной массы, высушенной глины, керамической массы) приводит к его размоканию со снижением прочности.
Слабое взаимодействие частиц в сухих дисперсных системах обусловливает их пылевидность, что, в частности, отрицательно сказывается на плодородии слабоструктурированных почв. Плохую структуру почв исправляют, внося в них органические удобрения. В настоящее время структуру почв улучшают также, вводя в них синтетические полимеры, например полиакриламиды. Концентрация их в почве должна быть такова, чтобы макромолекулы, адсорбируясь на почвенных частицах, связали несколько таких частиц в единый агрегат (рис. 104,6). Аналогичным путем достигают закрепления песков и создают упрочненные грунтовые дороги.
Конденсационные дисперсные структуры в зависимости от механизма возникновения фазового контакта (рис. 104, г) между частицами дисперсной фазы подразделяются на два подтипа: а) структуры спекания (срастания) и б) кристаллизационные структуры твердения.
Конденсационные структуры спекания (срастания) возникают в результате сварки, сплавления, спекания или склеивания дисперсных частиц в точках касания. Такая структура получается при термической обработке коагуляционной структуры, когда частицы дисперсной фазы «свариваются» по местам точечных контактов. Она характерна для ряда адсорбентов (силикагель, алюмогель), которые вследствие рыхлой их структуры являются хрупкими.
При высокой плотности упаковки дисперсных частиц конденсационные структуры спекания приобретают высокую прочность и часто жаропрочность. Таковы композиции из металла и тугоплавкого оксида металла, например спеченный алюминиевый порошок (САП). На алюминиевый порошок наращивают тонкую оксидную пленку и порошок спекают под давлением. Структура САП представляет собой каркас нз пленки А1203 толщиной 10—20 им, в ячейки которой включены зерна алюминия с сохранением частичных контактов между ними. Таким образом, конденсационные структуры представляют собой непрерывные каркасы дисперсной фазы и дисперсионной среды, вдвинутые друг в друга и не потерявшие дисперсности.
Конденсационная структура может быть получена и при конденсации дисперсной фазы из пересыщенных паров, растворов или расплавов. При образовании и росте зародышей новой фазы из концентрированных пересыщенных систем может возникнуть непрерывный сетчатый каркас путем срастания и переплетения растущих частиц дисперсной фазы. Если эти частицы представляют собой кристаллы, возникающие структуры называют кристаллиза-ционио-конденсационными структурами твердения.
Образование кристаллизационных структур в процессе гидратационного твердения минеральных вяжущих материалов (алюминатно-силикатных цементов, гипса, извести) детально изучено школой П. А. Ребиндера.
Бетонная смесь состоит из цемента, заполнителей — песка, гравия, щебня—■ и воды. Зерна цемента, представляющие собой алюминаты и силикаты кальция, постепенно растворяются, н из пересыщенного раствора выделяются менее растворимые кристаллы гидратов. Твердение бетонной массы состоит в срастании и переплетении этих кристаллов, связывающих песок, гравий и щебень в монолит. Введение в бетонные смеси поверхностно-активных веществ, электролитов, применение вибрационных механических воздействии привели к разработке новой технологии изготовления бетонных изделий повышенной прочности и твердости с одновременным улучшением экономических показателей производства.
Сцепление элементов конденсационных структур осуществляется путем образования химических связей, что обусловливает значительную прочность этих структур. Конденсационные структуры не тиксотропиы и не пластичны, это упруго-хрупкие, необратимо разрушаемые структуры, в отличие от тиксотропно-Обратимых коагуляционных структур.
Область науки, изучающая физическую химию процессов деформирования, разрушения и образования материалов и дисперсных структур, называется ф и -зико-химической механикой твердых тел и дисперсных структур. Она сформировалась в середине нашего века благодаря работам П. А. Ребиндера и его школы как новая область научного знания, погранич' ная коллоидной химии, молекулярной физике твердого тела, механике материалов и технологии их производства. Основной задачей физико-химической механики является создание материалов с заданными свойствами и оптимальной для целей их применения структурой. В частности, физико-химическая механика ставит своей задачей повышение прочности материалов. Этим достигается снижение массы и увеличение срока службы изделий, уменьшение расхода материалов на их изготовление, что приводит к повышению экономической эффективности производства.
Другая задача физико-химической механики тесно связана с механической технологией — обработкой металлов, горных пород, стекол, пластиков путем дробления, давления, резания, волочения — и состоит в управлении происходящими при этом процессами деформации, образования новых поверхностей н диспергирования.
В 1928 г. П. А. Ребиндер обнаружил, что прочность кристаллов каменной соли и кальцита значительно понижается в водных растворах ПАВ по сравнению с их прочностью на воздухе. Так был открыт эффект адсорбционного понижения прочности и облегчения деформации твердых тел, названный «эффектом Ребиндера».
В результате адсорбции ПАВ по местам дефектов кристаллической решетки (микротрещин, зародышевых трещии, границ зерен в поликристаллических материалах) облегчаются деформация и разрушение любых твердых материалов. Адсорбция ПАВ уменьшает поверхностную энергию и тем самым облегчает образование новых поверхностей при разрушении материалов.
Эффект адсорбционного понижения прочности и облегчения деформации твердых тел нашел широкое применение при совершенствовании разнообразных технологических процессов. Используя этот эффект, удалось достигнуть значительного повышения скоростей при бурении и проходке скважин в горных породах, облегчить обработку металлов резанием, давлением и волочением, повысить чистоту поверхностей при шлифовании и полировании, создать более совершенные смазки, облегчившие приработку деталей машнн.
Прочность реальных материалов из-за дефектов их кристаллической структуры значительно ниже прочности идеальных монокристаллов. Если диспергировать материал до частиц, размеры которых соизмеримы с расстояниями между дефектами структуры, то прочность таких высокодисперсных частиц будет близка к прочности идеальных твердых тел. Отсюда возникла идея о повышении прочности материалов путем их измельчения с последующим свариванием, спеканием уплотненных дисперсных порошков. На основе этой идеи разработано производство новых материалов и изделий из них — порошковая металлургия, металлокерамика (см. § 229).
Широкие возможности создания новых материалов открываются на основе композиций из неорганических веществ и полимеров органических соединений. Примером их являются резины, состоящие из вулканизованных каучуков,и сажи, масса которой достигает 50 % массы резины. В зависимости от соотно-
шения компонентов и от распределения серы н сажн в каучуке можно получать резины с разнообразными свойствами. На этом примере полезно подчеркнуть различие понятий о веществах и материалах. Каучук, сажа, сера —это вещества, из которых создается материал определенной структуры — резина.
Глава ВОДОРОД XI
Водород (Hydrogenium)' был открыт в первой половине XVI века немецким врачом и естествоиспытателем Парацельсом. В 1776 г. Г. Кавендиш (Англия) установил его свойства и указал отличия от других газов. Лавуазье первый получил водород из воды и доказал, что вода есть химическое соединение водорода с кислородом (1783 г.).
Водород имеет три изотопа: протий 4Н, дейтерий 2Н или D и тритий 3Н или Т. Их массовые числа равны 1, 2 и 3. Протий и дейтерий стабильны, тритий — радиоактивен (период полураспада 12,5 лет). В природных соединениях дейтерий и протий в среднем содержатся в отношении 1: 6800 (по числу атомов). Тритии находится в природе в ничтожно малых количествах.
Ядро атома водорода 1Н содержит один протон. Ядра дейтерия и трития включают кроме протона соответственно один и два нейтрона.
Молекула водорода состоит из двух атомов. Приведем некоторые свойства, характеризующие атом и молекулу водорода;
Энергия ионизации атома, эВ 13,60
Сродство атома к электрону, эВ 0,75
Относительная электроотрицательиость 2,1
Радиус атома, им 0,046
Межъядериое расстояние в молекуле, им 0,0741
Стандартная эитальпня диссоциации молекул при 436,1 25 °С, кДж/моль
| * Такое большое различие между величинами, выражающими содержание водорода в процентах от общего числа атомов и в процентах по массе, объясняется тем, что атомы водорода намного легче атомов других элементов, в част-, ности наиболее распространенных в земной коре кислорода и кремния. |
115. Водород в природе. Получение водорода. Водород в свободном состоянии встречается на Земле лишь в незначительных количествах. Иногда он выделяется вместе с другими газами при вулканических извержениях, а также из буровых скважин при добывании нефти. Но в виде соединений водород весьма распространен. Это видно уже из того, что он составляет девятую часть массы воды. Водород входит в состав всех растительных и животных организмов, нефти, каменного и бурого углей, природных газов и ряда минералов. На долю водорода из всей массы земной коры, считая воду и воздух, приходится около 1 %. Однако при пересчете на проценты от общего числа атомов содержание водорода в земной коре равно 17 % *.
116. Свойства и применение водорода
|
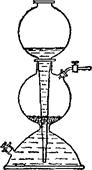
Рис. 105. Аппарат Киппа.
Водород — самый распространенный элемент космоса. На его долю приходится около половины массы Солнца и большинства других звезд. Он содержится в газовых туманностях, в межзвездном газе, входит в состав звезд. В недрах звезд происходит превращение ядер атомов водорода в ядра атомов гелия. Этот процесс протекает с выделением энергии, для многих звезд, в том числе для Солнца, он служит главным источником энергии. Скорость процесса, т. е. количество ядер водорода, превращающихся в ядра гелия в одном кубическом метре за одну секунду, мала. Поэтому и количество энергии, выделяющейся за единицу времени в единице объема, мало. Однако, вследствие огромности массы Солнца. об» щее количество энергии, генерируемой и излучаемой Солнцем, очень велико. Оно соответствует уменьшению массы Солнца приблизительно на 4 млн. т в секунду.
В промышленности водород получают главным образом из при«родного газа. Этот газ, состоящий в основном из метана, смейЫ* вают с водяным паром и с кислородом. При нагревании смеси га» зов до 800—900 °С в присутствии катализатора происходит реакция, которую схематически можно изобразить уравнением!
2СН4 + 02 + 2HsO => 2С02 + 6Н2
Полученную смесь газов разделяют. Водород очищают и либо используют на месте получения, либо транспортируют в стальные баллонах под повышенным давлением.
Важным промышленным способом получения водорода служит также его выделение из коксового газа или из газов переработки нефти. Оно осуществляется глубоким охлаждением, при котором все газы, кроме водорода^.сжижаются.
В лабораториях водород получают большей частью электроли-* зом водных растворов NaOH или КОН. Концентрация этих растворов выбирается такой, которая отвечает их максимальной электрической проводимости (25 % для NaOH и 34 % для КОЙ), Электроды обычно изготовляют из листового никеля. Этот металл не подвергается коррозии в растворах щелочей, даже будучи анодом. В случае надобности получающийся водород очищают от паров воды и от следов кислорода. Из других лабораторных методой наиболее распространен метод выделения водорода из растворов серной или соляной кислот действием на них цинка. Реакцию обычно проводят в аппарате Киппа (рис. 105).
116. Свойства и применение водорода. Водород — бесцветный газ, не имеющий запаха. При температуре ниже —240 °С (критическая температура водорода) он под давлением сжижается!
температура кипения жидкого водорода —252,8 °С (при нормальном атмосферном давлении). Если быстро испарять эту жидкость, то получается твердый водород в виде прозрачных кристаллов, плавящихся при —259,2 °С.
Водород-—самый легкий из всех газов, он в 14,5 раза легче воздуха; масса 1 л водорода при нормальных условиях равна 0,09 г. В воде водород растворим очень мало, но в некоторых металлах, например в никеле, палладии, платине, растворяется в значительных количествах.
С растворимостью водорода в металлах связана его способность диффундировать через металлы. Кроме того, будучи самым легким газом, водород обладает наибольшей скоростью диффузии: его молекулы быстрее молекул всех других газов распространяются в среде другого вещества и проходят через разного рода перегородки. Особенно велика его способность к диффузии при повышенном давлении и высоких температурах. Поэтому работа с водородом в таких условиях сопряжена со значительными трудностями.
Диффузия водорода в сталь при высоких температурах может вызвать водородную коррозию стали. Этот совершенно особый вид коррозии состоит в том, что водород взаимодействует с имеющимся в стали углеродом, превращая его в углеводороды (обычно в метан), что приводит к резкому.ухудшению свойств стали.
Химические свойства водорода в значительной степени определяются способностью его атомов отдавать единственный имеющийся у них электрон и превращаться в положительно заряженные ионы. При этом проявляется особенность атома водорода, отличающая его от атомов всех других элементов: отсутствие промежуточных электронов между валентным электроном и ядром. Ион водорода, образующийся в результате потери атомом водорода электрона, представляет собой протон, размер которого на несколько порядков меньше размера катионов всех других элементов. Поэтому поляризующее действие протона очень велико, вследствие чего водород не способен образовывать ионных соединений, в которых он выступал бы в качестве катиона. Его соединения даже с наиболее активными неметаллами, например с фтором, представляют собой вещества с полярной ковалентной связью.
Атом водорода способен не только отдавать, но и присоединять один электрон. При этом образуется отрицательно заряженный ион водорода с электронной оболочкой атома гелия. В виде таких ионов водород находится в соединениях с некоторыми активными металлами. Таким образом, водород имеет двойственную химическую природу, проявляя как окислительную, так и восстановительную способность. В большинстве реакций он выступает в качестве восстановителя, образуя соединения, в которых степень его окис-ленности равна +1- Но в реакциях с активными металлами он выступает в качестве окислителя: степень окисленности его в соединениях с металлами равна —1.
Таким образом, отдавая один электрон, водород проявляет сходство с металлами первой группы периодической системы, а присоединяя электрон, — с неметаллами седьмой группы. Поэтому водород в периодической системе обычно помещают либо в первой группе и в то же время в скобках в седьмой, либо в седьмой группе и в скобках в первой.
Соединения водорода с металлами называются гидридами. Гидриды щелочных и щелочноземельных металлов представляют собой соли, т.е. химическая связь между металлом и водородом в них ионная. Это кристаллы белого цвета. Все они нестойки и при нагревании разлагаются на металл и водород. При действии на них воды протекает окислительно-восстановительная реакция* в которой гидрид-ион Н~ выступает в качестве восстановителя, а водород воды — в качестве окислителя:
FT = Н° + е"; Н20 + е" = Н° + ОН"
В результате реакции образуются водород и основание. Напри-мер, гидрид кальция реагирует с водой согласно уравнению: СаН2 + 2Н20 = 2H2f -f Са(ОН)2
Эта реакция используется для определения следов влаги и для их удаления.
Кроме солеобразных известны металлообразные и полимерные гидриды. По характеру химической связи в металлообразных гидридах последние близки к металлам. Они обладают значительной электрической проводимостью и металлическим блеском, но очень хрупки. К ним относятся гидриды титана, ванадия, хрома. В полимерных гидридах (например, в гидридах цинка и алюминия) атомы металла связаны друг с другом водородными «мостиками», подобно тому, как это имеет место в молекулах бороводородов (стр. 612).
Если к струе водорода, выходящей из какого-нибудь узкого отверстия, поднести зажженную спичку, то водород загорается и горит несветящимся пламенем, образуя воду:
2Н2 + 02 = 2Н20
При поджигании смеси 2 объемов водорода с 1 объемом кислорода соединение газов происходит почти мгновенно во всей массе смеси и сопровождается сильным взрывом. Поэтому такую смесь называют гремучим газом. Стандартная энтальпия этой реакции в расчете на 1 моль образующейся жидкой воды равна —285,8 кДж, а в расчете на 1 моль водяного пара — 241,8 кДж. Таким образом, при горении водорода выделяется большое количество теплоты. Температура водородного пламени может достигать 2800°С. Водородно-кислородным пламенем пользуются для сварки и резки металлов, для плавления тугоплавких металлов.
При низких температурах водород с кислородом практически не взаимодействуют. Если смешать оба газа и оставить смесь, то и через несколько лет в ней нельзя обнаружить даже признаков воды. Если же смесь водорода с кислородом поместить в запаянный сосуд и держать в нем при 300°С, то уже через несколько дней образуется немного воды. При 500°С водород полностью соединяется с кислородом за несколько часов, а при нагревании смеси до 700°С происходит быстрый подъем температуры и реакция заканчивается практически мгновенно. Поэтому, чтобы вызвать взрыв смеси, нужно нагреть ее хотя бы в одном месте до 700 °С.
Малая скорость взаимодействия водорода с кислородом при низких температурах обусловлена высокой энергией активации этой реакции. Молекулы водорода и кислорода очень прочны; любое столкновение между ними при комнатной температуре оказывается неэффективным. Лишь при повышенных температурах, когда кинетическая энергия сталкивающихся молекул делается большой, некоторые соударения молекул становятся эффективными и приводят к образованию активных центров.
Применение катализатора может сильно увеличить скорость взаимодействия водорода с кислородом. Внесем, например, кусочек платинированного (т. е. покрытого мелко раздробленной платиной)' асбеста в смесь водорода с кислородом. Взаимодействие между газами настолько ускоряется, что через короткое время происходит взрыв.
Напомним, что реакция между водородом и кислородом является цепной и протекает по разветвленному механизму (см. § 62).
При высокой температуре водород может отнимать кислород от многих соединений, в том числе от большинства оксидов металлов. Например, если пропускать водород над накаленным оксидом меди, то происходит восстановление меди:
СиО + Н2 = Си + Н20
| * В основе процессов гидрогенизации лежит присоединение водорода к молекулам исходных веществ, |
Поэтому водород применяют в металлургии для восстановления некоторых цветных металлов из их оксидов. Главное применение водород находит в химической промышленности для синтеза хло-роводорода (см. § 121), для синтеза аммиака (см. § 138), идущего в свою очередь на производство азотной кислоты и азотных удобрений, для получения метилового спирта (см. § 169) и других органических соединений.Он используется для гидрогенизации* жиров (см.§ 173), угля и нефти. При гидрогенизации угля и нефти бедные водородом низкосортные виды топлива превращаются в высококачественные.
Водород используют для охлаждения мощных генераторов электрического тока, а его изотопы находят применение в атомной энергетике (см. стр. 108).
Атомарный водород. При высокой температуре молекулы водорода диссоциируют иа атомы:
Н2 5р±: 2Н
Осуществить эту реакцию можно, например, раскаляя током вольфрамовую проволочку в атмосфере сильно разреженного водорода. Реакция обратима, и чем выше температура, тем сильнее равновесие сдвинуто вправо. При 2000 °С степень диссоциации (т. е. доля молекул, подвергшихся диссоциации) составляет только 0,1%, при 3000 °С — 9%, при 4000 °С — 62,5 %, при 5000 °С — 94,7 % (все величины относятся к случаю, когда давление в системе равно нормальному атмосферному давлению).
Атомарный водород получается также при действии тихого электрического разряда- на молекулярный водород, находящийся под давлением около 70 Па. Образующиеся при этих условиях атомы водорода не сразу соединяются в молекулы, что дает возможность изучить их свойства.
При разложении водорода на атомы поглощается большое количество теплоты:
Н2 = 2Н —436 кДж
Отсюда понятно, что атомы водорода должны быть гораздо активнее его молекул. Чтобы молекулярный водород вступил в какую-либо реакцию, молекулы должны сперва распасться на атомы, для чего необходимо затратить большое количество энергии. При реакциях же атомарного водорода такой затраты энергии не требуется.
Действительно, атомарный водород уже при комнатной температуре восстанавливает многие оксиды металлов, непосредственно соединяется с серой, азотом и фосфором; с кислородом, он образует пероксид водорода.
117. Пероксид водорода Н202. Пероксид (перекись) водорода представляет собой бесцветную сиропообразную жидкость плотностью 1,45 г/см3, затвердевающую при —0,48°С. Это очень непрочное вещество, способное разлагаться со взрывом на воду и кислород, причем выделяется большое количество теплоты:
2Н202(ж) = 2Н20(ж) + 02 +197,5 кДж
Водные растворы пероксида водорода более устойчивы; в прохладном месте они могут сохраняться довольно долго. Пергидроль — раствор, который поступает в продажу, — содержит 30 % Н202. В нем, а также в высококонцентрированных растворах пероксида водорода содержатся стабилизирующие добавки.
Разложение пероксида водорода ускоряется катализаторами. Если, например, в раствор пероксида водорода бросить немного диоксида марганца МпСЬ, то происходит бурная реакция и выделяется кислород. К катализаторам, способствующим разложению пероксида водорода, принадлежат медь, железо, марганец, а также ионы этих металлов. Уже следы этих металлов могут вызвать распад Н2О2.
|
|
|
|
|
Дата добавления: 2014-11-16; Просмотров: 457; Нарушение авторских прав?; Мы поможем в написании вашей работы!