
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Лекция №7. Первичные фотохимические превращения молекул
|
|
|
|
Как уже упоминалось, молекулы при поглощении кванта света могут претерпевать фотоионизацию или переходить в электронно-возбужденное состояние. Химические реакции электронно-возбужденных молекул называют первичными фотохимическими превращениями. Основные типы первичных реакций:
1) Фотодиссоциация.
Если энергия кванта, поглощаемая молекулой достаточна для перевода валентного электрона со связывающей орбитали на разрыхляющую, то молекула распадается на частицы, разлетающиеся с определенной кинетической энергией. Время распада 10–13 с. Кривые потенциальной энергии для этого случая выглядят так, как показано на рисунке 5. По такому механизму идет фотодиссоциация HI:
HI → H· +I· (hv=327нм) и хлора: Cl2 → 2Cl· (hv=500нм)
Диссоциация может происходить также, если электрон, участвующий в образовании какой-нибудь связи, переходит на связывающую орбиталь, которая пересекается с кривой потенциальной энергии разрыхляющей орбитали электрона другой связи (рисунок 6). В этом случае энергия фотона должна быть в 1,5 раза больше энергии самой слабой связи молекулы. Этот процесс называется предиссоциацией.
 |
Рисунок 7.1. Фотодиссоциация молекулы. Кривые потенциальной энергии
 |
Рисунок 7.2. Предиссоциация молекулы. Кривые потенциальной энергии
Реакция фотодиссоциации лежит в основе многих репродукционных процессов. По такому механизму образуются свободные радикалы из фотоинициаторов полимеризации. Пример – фотодиссоциация перекиси бензоила:
|



 |  |  |
Диссоциация происходит и при фотолизе диазосоединений, таких как соль диазония и о-нафтохинондиазиды.
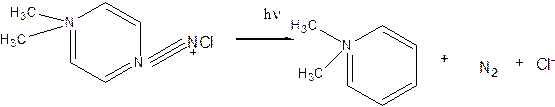
Получающиеся при реакции атомы группы могут претерпевать перегруппировку. Если она идет очень быстро (практически одновременно с поглощением фотонов), то выделяющаяся энергия входит в общий энергетический баланс. В этом случае снижается энергия кванта света, необходимая для диссоциации. Так получается, например, при фотолизе диазосоединений, когда энергия выделяется при образовании молекулы N2. В случае о-нафтохинондиазида продукты фотодиссоциации также подвергаются перегруппировке.
Перегруппировка увеличивает квантовый выход фотодиссоциации j дис, так как уменьшает вероятность рекомбинации полученных радикалов.
2) Фотоперенос электрона.
При поглощении кванта света может произойти перенос электрона от одной части молекулы к другой или от одной молекулы к другой. Примером внутри молекулярного фотопереноса может служить фотолиз ферриоксалата калия, основного компонента химического актинометра. Электрон переходит от аниона щавелевой кислоты к иону железа:
K3[Fe(C2O4)3] ® K3[Fe3+ (C2O4)3*] ® 3K+ + Fe2+ + 2C2O42- + · C2O4 -
Межмолекулярный фотоперенос электрона лежит в основе реакции фотоокисления и фотовосстановления. В обоих случаях электрон переходит от восстановителя к окислителю. Например, при фотохимической реакции красители метиленового голубого со слабым восстановителем (Fe2+, аскорбиновая кислота и другие) краситель восстанавливается до бесцветного лейкооснования, а восстановитель окисляется. Механизм фотовосстановления можно представить следующим образом. При поглощении квантового света красителем один из его электронов переходит на уровень возбуждения. На его место переходит электрон от восстановителя. Вслед за электроном к молекуле присоединяется ион Н+ от восстановителя или из окружающей среды (кислота в растворе).
3) Фотоприсоединение.
Реакции этого типа заключаются в присоединении молекулы по двойной связи другой молекулы. Механизм процессов можно представить так, что при поглощении кванта света один из электронов переходит на уровень возбуждения, изменяя свой спин. Молекула переходит из основного синглетного состояния S0 в возбужденное синглетное состояние S1*, а затем в возбужденное триплетное состояние Т1*. При этом разрывается p - связь молекулы:
>С=С< ® >Сֹ- Сֹ<
Так как энергия p - связи невелика (60 ккал/моль), то для инициирования этой реакции достаточно энергии квантов близкого УФ-излучения и синего света. Триплетно возбужденная молекула вступает в реакцию с молекулой в основном, невозбужденном состоянии.
Примерами реакции фотоприсоединения могут служить:
1)фотодимеризация коричной кислоты в a - труксиловую;
2)фотогидролиз кратоновой кислоты в b - оксимасляную.
Квантовый выход реакции фотоприсоединения зависит от концентрации реагентов.
4) Фотоперегруппировка.
При поглощении фотонов молекулами с двойными связями может произойти изменение строения молекулы по типу стереоизомеризации, валентной таутомеризации и таутомеризации с переносом водорода.
Примером стереоизомеризации может служить превращение транс-формы коричной кислоты в цис-форму.

При поглощении кванта света молекула переходит из основного синглетного состояния в возбужденное синглетное состояние, затем происходит безызлучательный переход молекулы в возбужденное триплетное состояние (в которой происходит диссоциация p - связи), и молекула приобретает способность поворачиваться вокруг оставшейся одинарной s-связи. Молекула легко переходит в триплетное цис-состояние, обладающее меньшей энергией, чем т-транс и, теряя энергию возбуждения, переходит в основное состояние S0 - цис.
Е

S*транс
Т1 транс
h v Т1 цис
S0 транс S0 цис
Рисунок 7.3. Схема энергетических переходов при фотостереизомеризации молекулы
Валентная таутомеризация заключается в размыкании и смыкании кольца при поглощении света. При фототаутомеризации может происходить перенос атома Н из одной части молекулы в другую. Фотоперенос Н может идти через синглетное возбуждающее состояние или через триплетное состояние.
Основная литература (2 осн. [67-69])
Дополнительная литература (3 доп. [23-25])
Контрольные вопросы:
- Первичные фотохимические превращения молекул.
- Понятие предиссоциации
- Основные типы первичных фотохимических реакций
- Фотодиссоциация
- Фотоперенос электрона
- Примеры фотоприсоединения
- Понятие фотоперегруппировки, привести примеры.
|
|
|
|
|
Дата добавления: 2014-11-16; Просмотров: 999; Нарушение авторских прав?; Мы поможем в написании вашей работы!