
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Термодинамическое равновесие и температура
|
|
|
|
Среди фундаментальных понятий термодинамики в первую очередь следует выделить понятия термодинамического (теплового) равновесия и температуры. Квазиравновесная термодинамика изучает закономерности поведения систем, находящихся в равновесных или близких к ним (квазиравновесных) состояниях, а также процессы взаимодействия систем с окружающей средой, в которых все промежуточные состояния являются квазиравновесными (см. раздел 4). Кроме того она устанавливает наиболее общее свойство неравновесных состояний изолированных систем, а именно - направленность и необратимость их эволюции к равновесным состояниям (см. раздел 5.4).
Квазиравновесная термодинамика является классической
областью физической науки, теоретическое развитие которой практически завершено. Современные проблемы термодинамики, выходящие за рамки данного пособия, связаны с изучением открытых систем и существенно неравновесных процессов, которые при определенных условиях могут приводить к самопроизвольному появлению в системах упорядоченных структур (самоорганизация).
Термодинамически равновесным называется такое состояние системы, которое при отсутствии внешних воздействий может сохраняться сколь угодно долго. О равновесии системы, подверженной внешнему воздействию, можно говорить как о равновесии подсистемы, являющейся частью более крупной изолированной и равновесной в целом системы. В этом случае предполагается, что внешнее воздействие на незамкнутую систему стационарно (не меняется с течением времени). Наконец, в случае, когда внешнее воздействие нестационарно, но установление равновесия происходит значительно быстрее, чем заметное изменение внешнего воздействия, изменяющиеся состояния системы называют квазиравновесными (почти равновесными), поскольку за промежутки времени, сравнимые с временем установления равновесия, воздействие можно считать стационарным.
Понятие температуры исторически возникло как количественная характеристика "степени нагретости" тела. Эмпирические температурные шкалы, построение которых основано на прямых измерениях, всегда имеющих сравнительный характер, по сути являются относительными.
Мы будем называть температурой физическую величину, которая указывает направление обмена энергией между частями замкнутой системы (от тела с большей температурой к телу с меньшей температурой) в случае, когда механические внешние условия, в которых находятся эти тела (например, их объемы), остаются неизменными1. В данном определении подразумевается, что при равенстве температур и неизменных внешних механических условиях обмен энергией между телами прекращается, то есть устанавливается равновесие. Температура, таким образом, характеризует равновесное состояние системы в целом или ее части.
Приведенное определение температуры является наиболее общим и, как следствие, недостаточно конкретным в количественном отношении. Его нужно дополнить заданием температурной шкалы, то есть определением начала отсчета и единицы измерения температуры.
В наиболее распространенной и удобной шкале температуры - шкале Цельсия - за начало отсчета (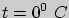 ) принята точка замерзания воды. Точке кипения воды при атмосферном давлении приписана температура
) принята точка замерзания воды. Точке кипения воды при атмосферном давлении приписана температура 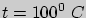 (сто градусов Цельсия). Интервал между этими опорными точками разбивается на сто равных частей (градусов). Определенную таким образом шкалу можно продолжить за рамки интервала
(сто градусов Цельсия). Интервал между этими опорными точками разбивается на сто равных частей (градусов). Определенную таким образом шкалу можно продолжить за рамки интервала 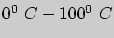 как в большую, так и в меньшую сторону.
как в большую, так и в меньшую сторону.
Другая температурная шкала может быть построена на основе использования уравнения состояния идеального газа:
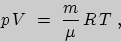
| (1) |
где 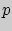 -давление,
-давление, 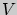 - объем,
- объем, 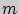 - масса,
- масса, 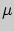 - молярная масса газа,
- молярная масса газа, 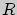 - универсальная газовая постоянная. Принцип действия газовых термометров основан на измерении давления при постоянном объеме газа. Температура
- универсальная газовая постоянная. Принцип действия газовых термометров основан на измерении давления при постоянном объеме газа. Температура 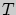 , определяемая при помощи соотношения (1), тоже измеряется в градусах; нулю шкалы Цельсия соответствует температура
, определяемая при помощи соотношения (1), тоже измеряется в градусах; нулю шкалы Цельсия соответствует температура 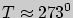 .
.
Введение "газовой" температурной шкалы оставляет открытым вопрос об "универсальности" универсальной газовой постоянной 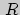 . Для того, чтобы определение температуры
. Для того, чтобы определение температуры 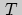 не зависело от конкретного газа, нужно постулировать, что постоянная
не зависело от конкретного газа, нужно постулировать, что постоянная 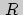 одинакова для всех газов. В молекулярной физике строго доказывается, что
одинакова для всех газов. В молекулярной физике строго доказывается, что 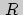 действительно является универсальной постоянной. В частности, если измерять температуру
действительно является универсальной постоянной. В частности, если измерять температуру 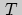 в энергетических единицах, джоулях, то постоянная
в энергетических единицах, джоулях, то постоянная 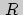 оказывается равной числу Авогадро - количеству молекул в одном моле вещества.
оказывается равной числу Авогадро - количеству молекул в одном моле вещества.
Существует, однако, и термодинамический способ введения абсолютной (не зависящей от экспериментальных условий измерения и используемых в опыте веществ) температурной шкалы. Он основан на соотношении Клаузиуса (4) для идеального цикла Карно (см. раздел 5.2). Это соотношение, как будет показано ниже, не зависит от рабочего вещества, и, следовательно, входящая в него температура является универсальной величиной. Если мысленно представить себе идеальный газовый термометр, в котором термометрическим телом является идеальный газ, то измеренная им температура будет совпадать с абсолютной температурой, входящей в соотношение (4).
Способ градуировки реального термометра в абсолютной температурной шкале был предложен и впервые практически реализован В. Томсоном (лордом Кельвином). Томсон сопоставлял экспериментальные данные, относящиеся к некому тепловому эффекту для реальных газов (эффект Джоуля-Томсона), с термодинамической теорией этого эффекта, в которую входит абсолютная температура 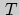 . Это позволило установить однозначную связь между абсолютной температурой и показаниями конкретного термометра.
. Это позволило установить однозначную связь между абсолютной температурой и показаниями конкретного термометра.
Абсолютная температурная шкала называется шкалой Кельвина. Единицу измерения температуры в абсолютной шкале называют градусом Кельвина или кельвином. Сопоставление произвольной эмпирической температурной шкалы с абсолютной шкалой Кельвина принято осуществлять на основе задания температуры тройной точки воды:
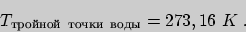
Температура замерзания воды в шкале Кельвина равна
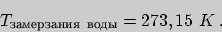
Утверждение о принципиальной возможности термодинамического определения абсолютной температуры иногда называют нулевым началом термодинамики. Оно формулируется следующим образом.
Если системы 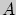 и
и 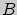 находятся в равновесии между собой и системы
находятся в равновесии между собой и системы 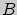 и
и 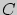 находятся в равновесии между собой, то в равновесии также находятся системы
находятся в равновесии между собой, то в равновесии также находятся системы 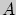 и
и 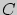 . (Закон транзитивности теплового равновесия).
. (Закон транзитивности теплового равновесия).
На первый взгляд сделанное утверждение представляется тривиальным. Действительно, условие равновесия систем 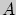 и
и 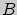 в общем случае можно записать в виде уравнения
в общем случае можно записать в виде уравнения
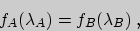
где 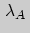 и
и 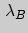 - наборы одних и тех же термодинамических параметров, относящихся соответственно к системам
- наборы одних и тех же термодинамических параметров, относящихся соответственно к системам 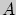 и
и 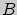 ,
, 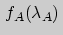 и
и 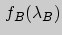 - функции этих параметров. Тогда условие равновесия систем
- функции этих параметров. Тогда условие равновесия систем 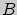 и
и 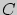 будет иметь вид
будет иметь вид 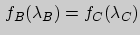 , откуда с очевидностью следует
, откуда с очевидностью следует 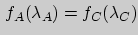 . Если условий равновесия несколько, то подобные рассуждения можно провести в отношении каждого из них.
. Если условий равновесия несколько, то подобные рассуждения можно провести в отношении каждого из них.
На самом деле, среди условий равновесия систем, в соответствии с данным выше определением температуры, всегда будет присутствовать условие равенства температур: 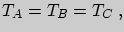 а оно имеет смысл только в том случае, если возможно определение температуры как параметра, не зависящего от свойств системы.
а оно имеет смысл только в том случае, если возможно определение температуры как параметра, не зависящего от свойств системы.
| Термодинамические уравнения состояния |
 Возможность разных вариантов описания одного и того же термодинамического процесса породила в термодинамике проблему, которой нет в механике, а именно, проблему выбора переменных, выбора функций, наиболее удобно (с точки зрения практических приложений) описывающих процесс изменения состояния.
В 1875 году американский физик Гиббс показал, что для решения технических задач термодинамики вполне достаточно знать поведение в термодинамических процессах всего четырех функций, играющих в термодинамике роль, аналогичную роли потенциальной энергии в механике. Эти четыре функции соотносятся с четырьмя рассмотренными ранее процессами (два адиабатных и два изотермических), которых достаточно, чтобы смоделировать работу любого технически интересного термодинамического устройства. Термодинамических потенциалов четыре, так как в термодинамике четыре основные переменные – две механические для работы (давление и объем, то есть сила и перемещение) и две тепловые для теплоты (температура и энтропия), которые могут рассматриваться в качестве независимых координат термодинамических процессов. Это хорошо видно из выражений, описывающих два механизма передачи энергии термодинамической системе: dA = PdV и dQ = TdS.
Удерживая неизменными (закрепляя) по одной механической и одной тепловой координате, мы получаем четыре разновидности основных термодинамических процессов, которых достаточно, чтобы равновесным способом перевести термодинамическую систему из любого начального (равновесного) состояния в любое конечное (равновесное), и соответствующие им четыре термодинамических потенциала. А раз так, то необходимо научиться находить эти основные термодинамические потенциалы (точнее – разность их значений) в разных состояниях, то есть надо найти дифференциальные уравнения, связывающие скорость изменения термодинамических потенциалов со значениями термодинамических параметров и их производными (то есть с величинами, которые могут быть определены опытным путем). Эти уравнения получили название термодинамические уравнения состояния (в отличие от обычных, термических уравнений состояния, в которые входят только термодинамические параметры и которые либо очень сложны, либо вовсе нам неизвестны). Все эти уравнения выводятся из термодинамического тождества (5.3) (термодинамической формы записи закона сохранения энергии, учитывающей существование энтропии) ТdS = dU + dA.
2. Термодинамические уравнения состояния
Начнем с внутренней энергии, которую в термодинамическом тождестве можно представить через полный дифференциал двух переменных - температуры и объема, тогда
Дифференциал энтропии как функции двух переменных (Т,V) можно записать в виде
Сравнивая эти два выражения, находим, что
Поскольку вторые, перекрестные производные от функции двух переменных должны быть равны независимо от порядка дифференцирования, то есть
то, следовательно,
откуда
и мы имеем термодинамическое уравнение состояния для внутренней энергии (как функции объема при постоянной температуре).
Возможность разных вариантов описания одного и того же термодинамического процесса породила в термодинамике проблему, которой нет в механике, а именно, проблему выбора переменных, выбора функций, наиболее удобно (с точки зрения практических приложений) описывающих процесс изменения состояния.
В 1875 году американский физик Гиббс показал, что для решения технических задач термодинамики вполне достаточно знать поведение в термодинамических процессах всего четырех функций, играющих в термодинамике роль, аналогичную роли потенциальной энергии в механике. Эти четыре функции соотносятся с четырьмя рассмотренными ранее процессами (два адиабатных и два изотермических), которых достаточно, чтобы смоделировать работу любого технически интересного термодинамического устройства. Термодинамических потенциалов четыре, так как в термодинамике четыре основные переменные – две механические для работы (давление и объем, то есть сила и перемещение) и две тепловые для теплоты (температура и энтропия), которые могут рассматриваться в качестве независимых координат термодинамических процессов. Это хорошо видно из выражений, описывающих два механизма передачи энергии термодинамической системе: dA = PdV и dQ = TdS.
Удерживая неизменными (закрепляя) по одной механической и одной тепловой координате, мы получаем четыре разновидности основных термодинамических процессов, которых достаточно, чтобы равновесным способом перевести термодинамическую систему из любого начального (равновесного) состояния в любое конечное (равновесное), и соответствующие им четыре термодинамических потенциала. А раз так, то необходимо научиться находить эти основные термодинамические потенциалы (точнее – разность их значений) в разных состояниях, то есть надо найти дифференциальные уравнения, связывающие скорость изменения термодинамических потенциалов со значениями термодинамических параметров и их производными (то есть с величинами, которые могут быть определены опытным путем). Эти уравнения получили название термодинамические уравнения состояния (в отличие от обычных, термических уравнений состояния, в которые входят только термодинамические параметры и которые либо очень сложны, либо вовсе нам неизвестны). Все эти уравнения выводятся из термодинамического тождества (5.3) (термодинамической формы записи закона сохранения энергии, учитывающей существование энтропии) ТdS = dU + dA.
2. Термодинамические уравнения состояния
Начнем с внутренней энергии, которую в термодинамическом тождестве можно представить через полный дифференциал двух переменных - температуры и объема, тогда
Дифференциал энтропии как функции двух переменных (Т,V) можно записать в виде
Сравнивая эти два выражения, находим, что
Поскольку вторые, перекрестные производные от функции двух переменных должны быть равны независимо от порядка дифференцирования, то есть
то, следовательно,
откуда
и мы имеем термодинамическое уравнение состояния для внутренней энергии (как функции объема при постоянной температуре).
|
8 вопрос: обратимые и необратимые процессы. Первое начало термодинамики
9 вопрос: теплоемкость. Уравнение Майера.
10 вопрос: изопроцессы: изохорический, изобарический, изотермический, адиабатический процессы в идеальных газах.
11 вопрос: уравнение Клапейрона - Клаузиуса. Реальные газы. Уравнение Ван-дер-Вальса.
12 вопрос: Давление газа с точки зрения МКТ. Уравнение МКТ. Теплоемкость и число степеней свободы молекул газа.
1 вопрос: Электростатика. Электронный заряд. Закон Кулона
2 вопрос: напряженность эл.поля. Потенциал эл.поля.
3 вопрос: Эл.диполь. Диполь в эл. Поле.
4 вопрос: проводник в эл.поле. распределение зарядов в проводнике
5 вопрос: Электроемкость. Конденсатор
6 вопрос: Эл.ток. сила тока и плоскость тока
7 вопрос: законы Ома, правила Кирхгофа. Закон Джоуля-Ленца
8 вопрос: маг.поле. характеристики маг.полч
9 вопрос: движение заряженных частиц в маг.поле
10 вопрос: Магнетики: диа-, пара-, ферромагнетики
11 вопрос: явление электромагнитной индукции. Самоиндукции
12 вопрос: ЭДС источника тока. Сторонние силы. Работа сторонних сил
13 вопрос: колебания. Характеристики
14 вопрос: продольные и поперечные волны. Уравнение волны. Фазовая скорость волны
|
|
|
|
|
Дата добавления: 2014-11-08; Просмотров: 2742; Нарушение авторских прав?; Мы поможем в написании вашей работы!