
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Опыт 5. Электролиз водного раствора сульфата меди (II) с инертными электродами
|
|
|
|
В U-образную трубку налить раствор иодида калия. В оба колена добавить 4-5 капель фенолфталеина, опустить графитовые электроды, присоединить последние к блоку питания. Пропустить ток.
Опыт 4. Электролиз водного раствора иодида калия
Краткая теория.
Лабораторная работа №3
на тему: «Электролиз водных растворов солей»
Цель работы:
- научиться составлять уравнения электролиза водных растворов солей;
- изучить закономерности протекания электролиза водных растворов солей.
Электролиз – это …
Потенциал разложения – это….
Потенциал разложения определяется…
Перенапряжение зависит от…
Поляризация электродов – это
При электролизе водных растворов вода может восстанавливаться на ………………………...в соответствии с уравнениями:
(в кислой среде)
(в нейтральной и щелочной среде)
Окислительно-восстановительный потенциал водородного электрода зависит от…………. и может быть рассчитан по уравнению ……………
При электролизе водных растворов вода может окисляться на ……………………….в соответствии с уравнениями:
(в кислой среде)
(в нейтральной и щелочной среде)
Окислительно-восстановительный потенциал кислородного электрода зависит от………… и может быть рассчитан по уравнению ……………
При электролизе водного раствора соли первым осуществляется процесс, характеризующийся…………………………….значением ………………………………….
На катоде первым ………………………..окислитель с ……………………..значением …
На аноде первым ……………………..восстановитель с ……………………..значением …
При электролизе водного раствора соли Na2SO4 протекают реакции
на катоде:
на аноде:
суммарное уравнение реакции:
При электролизе водного раствора соли NiCl2 протекают реакции
на катоде:
на аноде:
суммарные уравнения реакций
Отметить внешние изменения в растворе около электродов;
- составить уравнение электролитической диссоциации иодида калия в водном растворе:
KI →
- в растворе KI ……………………….среда;
- уравнение электролитической диссоциации воды:
- к отрицательно заряженному электроду перемещаются ионы………………….
- к положительно заряженному электроду перемещаются ионы…………………….
- возможные окислители:
- используя значения окислительно-восстановительных потенциалов, выбрать наиболее сильный окислитель:
 …………
………… 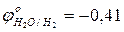 ; (pH=7)
; (pH=7)
- возможные восстановители:
- используя значения окислительно-восстановительных потенциалов, выбрать наиболее сильный восстановитель:
 …………
………… 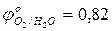 ; (pH=7);
; (pH=7);
- составить уравнение катодного процесса восстановления окислителя,
катодная реакция:
- составить уравнение анодного процесса окисления восстановителя,
анодная реакция:
- составить суммарное уравнение электролиза водного раствора KI, объединив уравнения катодной и анодной реакций с учетом коэффициентов электронного баланса:
 (ионное уравнение);
(ионное уравнение);
 (молекулярное уравнение);
(молекулярное уравнение);
- рассчитать минимальный потенциал разложения (без учета перенапряжения), необходимый для протекания электролиза иодида калия;
- ответить, какие металлы не выделяются на катоде при электролизе водных растворов их солей.
Вывод:
|
|
|
|
|
Дата добавления: 2014-11-18; Просмотров: 1488; Нарушение авторских прав?; Мы поможем в написании вашей работы!