
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Краткая теория. на тему: «Химические свойства металлов IIIA и IVA – подгрупп
|
|
|
|
Лабораторная работа №6
на тему: «Химические свойства металлов IIIA и IVA – подгрупп
(Al, Sn, Pb)»
Цель работы:
- Изучить свойства металлов IIIA и IVA- подгрупп;
- Изучить свойства характеристичных соединений металлов IIIA и IVA- подгрупп;
1. Положение элементов в периодической системе, свойства атомов
Электронные конфигурации атомов, валентные электроны
IIIA- подгруппа:
IVA- подгруппа:
Степени окисления: IIIA- подгруппа ……………..IVA- подгруппа …….
2. Свойства простых веществ – металлов:
- положение в «ряду стандартных окислительно-восстановительных (электродных) потенциалов металлов»
φ(Men+/Me) =
- активность металлов:
Составьте уравнения реакций:
- взаимодействие с кислородом:
а) Al б) Sn
в) Pb
- взаимодействие с галогенами (хлором):
а) Al б) Sn в) Pb
- взаимодействие с серой:
а) Al
- взаимодействие с водными растворами кислот, окисляющими H+ (HF, HCl, HBr, HI, разбавленной H2SO4, H3PO4, RCOOH и другими):
а) Al + HBr → б) Sn + RCOOH →
- Металлы IIIA – подгруппы не взаимодействует с водой, так как …………………………………, но легко вытесняют водород из водного раствора щелочи
Al + NaOH + H2O →
- взаимодействие с концентрированной H2SO4:
а) Sn + H2SO4(конц) → ………….+ S + H2O
- взаимодействие с разбавленной и концентрированной HNO3:
а) Pb + HNO3(разб) → ………….+ NО + H2O
б) Sn + HNO3(конц) → H2SnO3 + NO2 + H2O
3. Свойства оксидов и гидроксидов металлов III A и IV A- подгрупп:
- формулы оксидов металлов IIIA …………и IVA- подгрупп……………….
- формулы гидроксидов металлов IIIA ……………..и IVA- подгрупп……………
- растворимость, взаимодействие с водой оксидов и гидроксидов металлов IIIA и IVA- подгрупп
- диссоциация в водном растворе гидроксидов металлов IIIA и IVA- подгрупп (на примере гидроксида олова (II)):
[Sn(OH)4]2- + 2H+  2 H2O + Sn(OH)2
2 H2O + Sn(OH)2  Sn2+ + 2OH-
Sn2+ + 2OH-
Оксиды и гидроксиды металлов IIIA и IVA- подгрупп проявляют ………………………… свойства
- взаимодействие оксидов и гидроксидов металлов IIIA и IVA- подгрупп с кислотами и кислотными оксидами.
а) Al2О3 + H2SO4 →
б) Pb(OH)2 + H2SO4 →
- взаимодействие оксидов и гидроксидов металлов IIIA и IVA- подгрупп с основаниями при сплавлении происходит с образованием простых солей и воды
PbO + NaOH → Na2PbO2 + H2O
Pb(OH)2 + NaOH → Na2PbO2 + H2O
- взаимодействие оксидов и гидроксидов металлов IIIA и IVA- подгрупп с водными растворами щелочей происходит с образованием комплексных солей
Al2О3 + NaOH + H2O → Na[Al(OH)4]
Al(OH)3 + NaOH → Na[Al(OH)4]
Pb(OH)2 + NaOH →
4. Окислительно-восстановительные свойства соединений металлов IIIA и IVA-подгрупп
Соединения алюминия ……………….окислительно-восстановительных свойств, так как …………
Используя значения ОВП, приведенных на диаграммах Латимера, охарактеризовать окислительно-восстановительные свойства соединений олова.
Диаграммы Латимера:
а) для олова;
-0,118
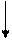
 SnO2
SnO2
+0,154 -0,141

 Sn4+ Sn2+ Sn0
Sn4+ Sn2+ Sn0
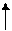 -0,96 -0,79
-0,96 -0,79

 [Sn(OH)6]2- [Sn(OH)6]4-
[Sn(OH)6]2- [Sn(OH)6]4-
Используя значения ОВП, приведенных на диаграммах Латимера, охарактеризовать окислительно-восстановительные свойства соединений свинца.
Диаграммы Латимера:
б) для свинца: -0,956

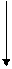 PbS
PbS
1,685 -0,356
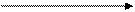

 PbSO4
PbSO4
1,456 - 0,126

 PbO2 Pb2+ Pb0
PbO2 Pb2+ Pb0
 0,305 -0,538
0,305 -0,538
 [Pb(ОН)6]2- [Pb(OH)4]2-
[Pb(ОН)6]2- [Pb(OH)4]2-
ВНИМАНИЕ! Все соединения свинца ядовиты! При работе с ними соблюдать особую осторожность! По окончании опытов с кислотами растворы слить в слив, а не растворившиеся металлы положить в специальную посуду!
Опыт 1. Взаимодействие «амальгамированного» алюминия с водой
В пробирку с 5 мл дистиллированной воды поместить обычную алюминиевую проволоку и оставить для сравнения до окончания опыта. В две пробирки налить по 3-5 мл раствора соли ртути(II) и опустить в каждую металлическую алюминиевую проволоку, выдержать в течение 5 минут. После чего проволочки протереть кусочком фильтровальной бумаги, и одну из них оставить на воздухе, а вторую поместить в пробирку с дистиллированной водой. Наблюдать за изменениями в пробирках и на поверхности проволоки, оставшейся на воздухе, в течение 5-10 минут.
- Отметить, происходят ли изменения в с обычной алюминиевой проволокой в воде
- в обычных условиях алюминий не взаимодействует с водой, потому что…………………
- отметить, как изменилась поверхность алюминиевой проволоки после обработки солью ртути………..
- составить уравнения реакций, протекающих в растворе соли ртути
Hg(NO3)2 + H2O →
- составить уравнения реакций, протекающих в растворе соли ртути на поверхности алюминиевой проволоки:
Al2O3 + HNO3 →
Al + Hg(NO3)2 →
- объяснить, может ли образоваться на поверхности «амальгамированного» алюминия защитная оксидная пленка……….
- отметить, что образуется на поверхности «амальгамированного» алюминия на воздухе…..
- составить уравнение реакции окисления алюминия на воздухе:
Al + O2 →
- отметить, какие изменения происходят в пробирке с «амальгамированной» алюминиевой проволокой в воде
- составить уравнение реакции между «амальгамированным» алюминием и водой:
Al + H2O →
- ответить, пассивирован ли «амальгамированный» алюминий.
|
|
|
|
|
Дата добавления: 2014-11-18; Просмотров: 651; Нарушение авторских прав?; Мы поможем в написании вашей работы!