
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Электрохимия
Электрохимия рассматривает процессы превращения химической энергии реакции в электрическую (например, в гальванических элементах) или процессы обратного превращения энергии (в электролизерах). И те, и другие устройства составлены из электродов.
Виды электродов. В зависимости от природы материала твердого тела, находящегося в контакте с раствором, различают следующие виды электродов:
1. Электроды 1-го рода. Они представляют собой металл M (или неметалл Х), опущенный в раствор его соли. Условно их изображают следующим образом:
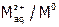 (или
(или 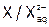 ). Например,
). Например, 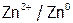 (или
(или 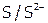 ).
).
Возникающий на электроде потенциал (E) будет тем отрицательнее, чем активнее металл и чем меньше активность катионов этого металла в растворе. Последнее следует из формулы Нернста, по которой рассчитывают ОВП веществ в нестандартных условиях [8]. Например, формула Нернста для цинкового электрода:
 .
.
В случае неметаллов, наоборот: чем больше активность ионов, тем отрицательнее потенциал. В частности, для серы:
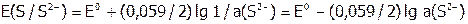 .
.
2. Электроды 2-го рода. Они состоят из металла, покрытого слоем его малорастворимого соединения и погруженного в раствор соли, который содержит анион, являющийся общим с малорастворимым соединением. Это каломельный электрод (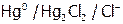 ), хлорсеребряный (
), хлорсеребряный (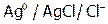 ) и т.п.. Потенциал таких электродов зависит от активности аниона малорастворимого соединения. Например, в случае каломельного электрода:
) и т.п.. Потенциал таких электродов зависит от активности аниона малорастворимого соединения. Например, в случае каломельного электрода:
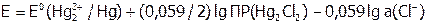 .
.
Электроды 2-го рода хорошо воспроизводимы и устойчивы по значению потенциала, и поэтому часто используются в качестве электродов сравнения в измерительных приборах, в частности, в pH-метрах.
3. Газовые электроды. Это пористые пластинки из благородных металлов, насыщенные газом и находящиеся в контакте с раствором, содержащим соответствующие (газу) ионы. Их потенциал определяется, с одной стороны, давлением, под которым в систему подается газ, а с другой – активностью ионов в растворе. Газовым является, например, водородный электрод [8].
4. Ионообменные электроды. К ним относится, в частности, стеклянный электрод, потенциал которого определяется степенью обмена ионов стекла (например, ионов  ) на ионы раствора (в частности, на ионы водорода; в этом случае потенциал стеклянного электрода линейно зависит от рН раствора, поэтому данный электрод используется в качестве измерительного в pH-метрах).
) на ионы раствора (в частности, на ионы водорода; в этом случае потенциал стеклянного электрода линейно зависит от рН раствора, поэтому данный электрод используется в качестве измерительного в pH-метрах).
Гальванические элементы (ГЭ). Они состоят из двух электродов, имеющих разные ОВП (схема одного из них приведена на рис. 10). Электродвижущая сила (э.д.с.), т.е. 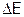 любого гальванического элемента рассчитывается по формуле:
любого гальванического элемента рассчитывается по формуле:
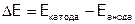 ,
,
причем катодом служит электрод с более положительным ОВП
В случае концентрационного ГЭ электроды различаются только концентрацией (точнее активностью) потенциалопределяющих ионов в водной фазе. В таких ГЭ катодом является электрод с более высокой концентрацией электролита [8], [12].
Электрохимическая коррозия металла. Это разрушение М в результате электрохимического взаимодействия его с компонентами окружающей среды. Такую коррозию вызывают, главным образом, примеси, содержащиеся в М, или неоднородность его структуры. В этом случае при контакте металла с раствором электролита (например, с влагой, поглотившей компоненты окружающей среды) на поверхности М возникает множество микрогальванических элементов.
Причем катодом чаще всего бывают примеси, а анодом, который растворяется, – частицы самого металла как более активного вещества. На катоде в кислой среде может выделяться водород, а в нейтральной – восстанавливаться кислород, растворенный в электролите (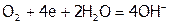 ), стимулируя окисление М («связыванием» его электронов).
), стимулируя окисление М («связыванием» его электронов).
Процесс электрохимической коррозии, очевидно, тем более термодинамически обусловлен (т.е. 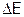 тем выше), чем дальше отстоят друг от друга вещества, образовавшие гальваническую пару (на поверхности металла), в ряду напряжений.
тем выше), чем дальше отстоят друг от друга вещества, образовавшие гальваническую пару (на поверхности металла), в ряду напряжений.
На практике часто защищают металлические (в частности, железные) изделия от коррозии (в том числе и от электрохимической), соединяя их с более активным М. Благодаря постепенному окислению этого металла (в образовавшемся ГЭ) обеспечивается электрохимическая защита самого изделия от коррозии.
Электродные процессы при электролизе. На характер электродных процессов большое влияние оказывает состав электролита. В частности, электролиз расплава и раствора одного и того же вещества часто протекает неодинаково из-за конкурирующего влияния частиц растворителя.
1). Процессы на катоде. При электролизе расплава соли на катоде выделяется металл, а в случае раствора катодный процесс может идти по-разному:
а) в нейтральной среде, если потенциал М более положителен, чем воды (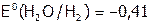 В), выделяется металл, например, медь:
В), выделяется металл, например, медь:
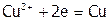 (
(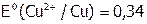 В).
В).
Если потенциал М более отрицателен, чем воды, как в случае натрия (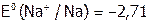 В), то выделяется водород:
В), то выделяется водород: 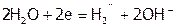 .
.
Если же потенциал металла близок к величине (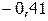 ) В (это М, расположенные в ряду напряжений между Mn и
) В (это М, расположенные в ряду напряжений между Mn и 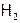 ), то в зависимости от концентрации раствора, его температуры и силы тока возможно как восстановление металла, так и выделение водорода; часто оба процесса идут совместно.
), то в зависимости от концентрации раствора, его температуры и силы тока возможно как восстановление металла, так и выделение водорода; часто оба процесса идут совместно.
б) в кислой среде, из-за возрастания потенциала водородной пары, не только термодинамически более обусловлен процесс выделения водорода (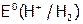 =0,00 B), но и механизм его восстановления становится другим:
=0,00 B), но и механизм его восстановления становится другим:
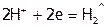 .
.
2). Процессы на аноде. Следует различать электролиз с инертным анодом (например, из графита или платины) и с растворимым анодом:
а) материал растворимого анода легче окисляется (т.е. его ОВП менее положителен), чем анионы раствора. Таким материалом является, например, никель:
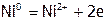 .
.
Используя в качестве растворимого анода металл с примесями, можно его очистить. При этом чистый М выделяется на катоде, а примеси, освобождающиеся при растворении анода, или остаются в растворе, или оседают на дно ячейки.
б) на инертном аноде при электролизе расплавов разряжаются анионы соли:
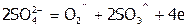 ,
, 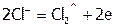 .
.
При электролизе же водных растворов HF и кислородосодержащих кислот (в которых ц.а. имеет высшую ст.ок. а также их солей происходит окисление частиц воды, имеющих менее положительный потенциал [8]. Причем в щелочной среде разряжаются преимущественно гидроксильные ионы: 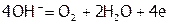 ,
,
а в кислой и нейтральной – молекулы воды: 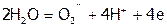 .
.
Напротив, бескислородные анионы ( ,
, 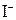 и др.) обычно имеют потенциал окисления менее положительный, чем у воды, и поэтому окисляются на аноде не только при электролизе в расплаве, но и в водном растворе.
и др.) обычно имеют потенциал окисления менее положительный, чем у воды, и поэтому окисляются на аноде не только при электролизе в расплаве, но и в водном растворе.
Перенапряжение. Характер продуктов электролиза часто определяется таким явлением, как перенапряжение. Это дополнительное напряжение по сравнению с расчетным, которое нужно приложить к электродам для окисления или восстановления данных частиц.
Перенапряжение на катоде наблюдается, в частности, при электролитическом выделении водорода, причем его величина сильно зависит от материала катода и убывает в ряду: 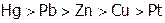 . Поэтому на ртутном катоде при электролизе раствора NaCl выделяется
. Поэтому на ртутном катоде при электролизе раствора NaCl выделяется 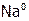 , а не
, а не 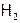 . По этой же причине растворение цинка в кислоте ускоряется, если привести его в контакт с металлической медью, на которой именно из-за меньшего перенапряжения и выделяется водород. Приведение же цинка в контакт со свинцом не влияет на скорость растворения Zn в кислоте, а водород при этом восстанавливается, как и до контакта, на цинке.
. По этой же причине растворение цинка в кислоте ускоряется, если привести его в контакт с металлической медью, на которой именно из-за меньшего перенапряжения и выделяется водород. Приведение же цинка в контакт со свинцом не влияет на скорость растворения Zn в кислоте, а водород при этом восстанавливается, как и до контакта, на цинке.
Перенапряжение на платиновом аноде делает потенциал разряда молекул воды (с выделением О2) более положительным, чем нужно для окисления даже хлоридов (до Cl2), хотя их Е0 без учета перенапряжения 0,82В и 1,36В соответственно.
ЛАБОРАТОРНАЯ РАБОТА
«Электрохимия»
ПРИМЕЧАНИЕ. При оформлении отчета привести уравнения всех полуреакций, протекающих на электродах в проведенных опытах.
1. Ряд напряжений. Перенапряжение
а). Коррозия оцинкованного и луженого железа. Две пробирки наполнить на 1/2 их объема водой и добавить по 2 капли 1М серной кислоты и гексацианоферрата(III) калия (реактив на ионы железа(II)). Две железные проволоки очистить наждачной бумагой, затем одной обмотать кусочек очищенного цинка, а другой – очищенного олова и опустить их в приготовленные растворы. Как объяснить различие в их окраске, проявляющееся через несколько минут? Относятся ли наблюдаемые явления к электрохимической коррозии? Записать схему возникающего ГЭ. Что эффективнее для защиты Fe от коррозии: цинкование или лужение (покрытие оловом)?
б). Перенапряжение выделения водорода. Внести в 2 пробирки по 6 капель 1М серной кислоты и по грануле цинка. Что наблюдается? Коснуться кусочка цинка в одной из пробирок медной проволокой. Изменилась ли скорость образования газа? На каком из металлов он выделяется? Отнять проволоку и вновь отметить наблюдаемый эффект. Добавить в одну пробирку с гранулой цинка 2 капли сульфата меди(II), а в другую – соли свинца(II). Изменилась ли скорость процесса? Почему?
Соответствуют ли результаты опытов «а» и «б» ряду напряжений металлов?
 2. Составление гальванических элементов.
2. Составление гальванических элементов.
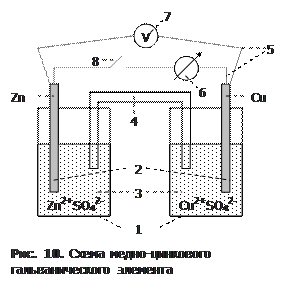
а)Медно-цинковый ГЭ. Собрать установку (рис. 10), используя стаканы на 50 мл (1), металлические пластинки цинка и меди (2), 1М растворы солей этих металлов (3), а в качестве электролитического мостика – стеклянную П-образную трубку (4), заполненную насыщенным раствором хлорида калия в смеси с агар-агаром. Внешнюю часть электроцепи составить из звонковых проводов (5), нуль-гальванометра (6), вольтметра (7) и ключа (8).
Отметить показания вольтметра при разомкнутой внешней цепи, а затем при замкнутой в первый момент работы ГЭ и потом. Объяснить наблюдение.
Рассчитать значения э.д.с. медно-цинкового элемента по величине стандартных ОВП и сравнить с опытными данными. В чем причина возможных расхождений? Изобразить двойной электрический слой на границе раздела «металл ‑ раствор соли» для цинкового и медного электродов. В результате какой ОВР возникает электрический ток в данном ГЭ. Каково направление тока? Какие ионы и куда перемещаются в растворе при замыкании внешней цепи?
б) Концентрационный ГЭ. Использовать ту же установку (рис. 10), но медный электрод заменить цинковым с 0,001М раствором сульфата цинка (последний приготовить из одномолярного последовательным трехкратным разбавлением в 10 раз). Какой электрод является катодом? Что можно сказать о величине отклонения стрелки гальванометра при замыкании внешней цепи по сравнению с опытом «а»? Объяснить результаты.
Рассчитать теоретическое значение э.д.с. составленного концентрационного ГЭ и сравнить с опытными данными. Почему возможны расхождения? Каково направление тока во внешней цепи и направление движения ионов в растворе при работе данного ГЭ? Как и почему меняется величина его э.д.с. в ходе работы?
3. Электролиз
а). Инертные электроды. Собрать установку (рис. 11), в которой электролизером служит V‑образная трубка (1), закрепленная на штативе (2) и заполненная на 1/2 объема раствором  сульфата натрия (с добавлением метилоранжа или лакмуса); а электроды (3) из инертного материала соединены с полюсами батарейки (4) и опущены в указанный раствор соли.
сульфата натрия (с добавлением метилоранжа или лакмуса); а электроды (3) из инертного материала соединены с полюсами батарейки (4) и опущены в указанный раствор соли.
Пропустить через раствор электрический ток. Отметить и объяснить изменение окраски в обоих коленах электролизера.
б). Растворимый анод. Использовать ту же установку, что и в опыте 6, но анодом сделать медную пластинку и заполнить электролизер 0,3М сульфатом меди(II). Через 6 минут электролиза отметить цвет катода. Какой газ выделяется на аноде? Сделать катод анодом, поменяв полюса батарейки, и снова пропустить электрический ток. Что наблюдается? Почему?
в). Электролитическое фрезерование. 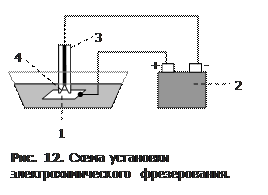 Собрать установку по рис. 12. В чашку налить насыщенный раствор хлорида натрия, опустить в него кусочек алюминиевой фольги (1) и сделать металл анодом, присоединив к положительному полюсу батарейки (2). Катод (3), который представляет собой кусочек карандаша с небольшим углублением (4) в грифеле и выполняет функцию химического сверла, приложить к пластинке.
Собрать установку по рис. 12. В чашку налить насыщенный раствор хлорида натрия, опустить в него кусочек алюминиевой фольги (1) и сделать металл анодом, присоединив к положительному полюсу батарейки (2). Катод (3), который представляет собой кусочек карандаша с небольшим углублением (4) в грифеле и выполняет функцию химического сверла, приложить к пластинке.
Образуется ли через несколько минут отверстие на месте контакта? Какой газ выделяется вокруг карандаша? Какой тип электрода используется в данном опыте в качестве анода?
|
|
Дата добавления: 2014-11-20; Просмотров: 845; Нарушение авторских прав?; Мы поможем в написании вашей работы!