
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Типовые задачи. Задача 1. Рассчитать рН раствора соляной кислоты с молярной концентрацией вещества в растворе С(НСl) = 0,001 моль·дм-3
|
|
|
|
Задача 1. Рассчитать рН раствора соляной кислоты с молярной концентрацией вещества в растворе С(НСl) = 0,001 моль·дм-3.
Дано: Решение:
 С(HCl) = 0,001 моль·дм-3 HCl «H+ + Cl-, т.к. a = 1, то
С(HCl) = 0,001 моль·дм-3 HCl «H+ + Cl-, т.к. a = 1, то
 [H+] = [HCl] = 10-3 моль·дм-3
[H+] = [HCl] = 10-3 моль·дм-3
рН -? pH = -lg [H+]
pH = -lg10-3 = 3
Ответ: pH = 3.
Задача 2. Рассчитать pH раствора гидроксида калия с молярной концентрацией вещества в растворе C(KOH) = 1,5·10-2 моль·дм-3.
Дано: Решение:
 С(KOH) = 1,5·10-2 моль·дм-3 KOH «K+ + OH-, т.к. a = 1, то
С(KOH) = 1,5·10-2 моль·дм-3 KOH «K+ + OH-, т.к. a = 1, то
 [OH-] = [KOH] = 1,5·10-2 моль·дм-3
[OH-] = [KOH] = 1,5·10-2 моль·дм-3
рН -? pOH = –lg[OH-]
pOH = –lg1,5·10-2 = 1,82
pH + pOH = 14 Þ pH = 14 – pOH
pH = 14 – 1,82 = 12,18.
Ответ: pH = 12,18.
Задача 3. pH желудочного сока равен 1,65. Определить концентрации ионов [H+] и [OH-] в желудочном соке.
Дано: Решение:
 pH = 1,65 pH = –lg [H+]
pH = 1,65 pH = –lg [H+]
 lg [H+] = –pH Þ [H+] = 10–pH
lg [H+] = –pH Þ [H+] = 10–pH
[H+] -? [H+] = 10–1,65 = 0,0224 моль·дм–3 = 2,24·10–2 моль·дм–3
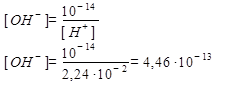 |
[OH-] -? [H+] · [OH-] = 10–14
Ответ: [H+] = 2,24·10–2 мольˑдм–3; [OH–] = 4,46·10–13 мольˑдм–3.
Тестовые задания для самоконтроля
Выберите правильный вариант ответа
01. КОНЦЕНТРАЦИЯ ИОНОВ ОН— (МОЛЬ/ДМ 3) В РАСТВОРЕ ПРИ рН = 2,00 РАВНА ________МОЛЬ/ДМ3
1) 10–10
2) 10–2
3) 10–12
4) 10–4
02. ЗНАЧЕНИЯ С(ОН—) И С(Н+ ) В РАСТВОРЕ ПРИ рН = 5,0 СОСТАВЛЯЮТ______ МОЛЬ/ДМ3
1) 10–5 и 10 –9
2) 10–4 и 10 –10
3) 10–10 и 10 –4
4) 10–9 и 10 –5
03. ЗНАЧЕНИЯ С(ОН—) И С(Н+ ) В РАСТВОРЕ ПРИ рОН = 6,0 СОСТАВЛЯЮТ ______ МОЛЬ/ДМ3
1) 10–8 и 10–6
2) 10–4 и 10–10
3) 10–6 и 10–8
4) 10–7 и 10–7
04. УКАЖИТЕ рН СОЛЯНОЙ КИСЛОТЫ С КОНЦЕНТРАЦИЕЙ 0,1 МОЛЬ/Л И ВОДНОГО РАСТВОРА ГИДРОКСИДА КАЛИЯ С КОНЦЕНТРАЦИЕЙ 1,0 МОЛЬ/Л, СЧИТАЯ, ЧТО УКАЗАННЫЕ ВЕЩЕСТВА ДИССОЦИИРУЮТ ПОЛНОСТЬЮ
1) 1 и 14
2) 7 и 7
3) 14 и 0
4) 2 и 12
05. В РАСТВОРЕ АЗОТНОЙ КИСЛОТЫ С рН = 2 КОНЦЕНТРАЦИЯ ВЕЩЕСТВА ПРИ α = 100% РАВНА _____ МОЛЬ/ДМ3
1) 0,05
2) 0,1
3) 0,01
4) 0,001
06. рН РАСТВОРА ГИДРОКСИДА БАРИЯ РАВЕН 13, КОНЦЕНТРАЦИЯ ОСНОВАНИЯ В НЕМ ПРИ α =100% РАВНА ______ МОЛЬ/ ДМ3
1) 0,005
2) 0,1
3) 0,05
4) 0,001
07. РАСТВОР, В 500 МЛ КОТОРОГО РАСТВОРЕНО 1,825 г HCl, ИМЕЕТ рН, РАВНЫЙ
1) 2
2) 4
3) 5
4) 1
08. УКАЖИТЕ рН 0,003 МОЛЯРНОГО РАСТВОРА СОЛЯНОЙ КИСЛОТЫ
1) 11,5
2) 3
3) 7
4) 2,5
Контрольные задания
09. Рассчитать рН и рОН слюны, если концентрация ионов водорода в ней составляет
1,78·10–7 моль·дм-3.
10. Физиологическое значение рН крови 7,36. Определить концентрацию ионов [H+] и [OH-] в крови.
11. Рассчитать рН раствора соляной кислоты с концентрацией 0,03 моль/дм3 и водного раствора гидроксида калия с концентрацией 0,12 моль/дм3, считая, что указанные вещества диссоциируют полностью.
12. Определите рН кишечного сока, если концентрация гидроксид- анионов ОН- в составе кишечного сока составляет 2,3·10-6 моль·дм-3.
Литература
1. Общая химия. Биофизическая химия. Химия биогенных элементов: Учеб. для вузов / Ю. А. Ершов, В.А. Попков, А.С. Берлянд и др.; Под ред. Ю.А. Ершова. – 5-е изд., стер. – М.: Высш.шк., 2005. – С. 66 – 76, 101 – 107.
2. Практикум по общей химии. Биофизическая химия. Химия биогенных элементов: Учеб. пособие для студентов медицинских спец. вузов / Ю.А. Ершов, А.М. Кононов, С.А. Пузаков и др.; Под ред. Ю.А. Ершова, В.А. Попкова. – М.: Высш. шк., 2008. – С.45-50.
|
|
|
|
|
Дата добавления: 2014-11-20; Просмотров: 10871; Нарушение авторских прав?; Мы поможем в написании вашей работы!