
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Буферные системы
|
|
|
|
Свойством всех живых организмов является постоянство рН биологических жидкостей, тканей и органов. Это постоянство поддерживается их буферными системами и необходимо для обеспечения нормальной деятельности ферментов, регулирования осмотического давления и других показателей.
Знания по теме «Буферные «системы» необходимы для понимания механизма их действия, количественной оценки способности буферных систем связывать посторонние кислоты и щелочи, понимания их взаимосвязи и роли в поддержании кислотно-основного гомеостаза.
Кроме того, важно уметь готовить буферные растворы для последующего использования их в различных медико-биологических, химических и клинических исследованиях.
Буферными называют системы, состоящие из двух сопряженных компонентов, способных до определенного предела противодействовать изменению рН среды при добавлении к ним небольших количеств кислоты и щелочи, а также при разбавлении раствора или концентрировании.
Способность буферных систем сохранять постоянство pH называется буферным действием.
По составу, с точки зрения протонной теории, буферные системы делят на кислые и основные.
Кислые буферные системы состоят из слабой кислоты и сопряженного с ней избытка сильного основания, создаваемого солью этой кислоты.
Например: Ацетатная буферная система – кислая буферная система, состоит из:
 СН3СООН – слабая кислота;
СН3СООН – слабая кислота;
СН3СООNa – растворимая соль (содержит сопряженное сильное основание СН3СОО- ).
Аммиачная буферная система – основная буферная система, состоит из:
 NН4ОН – слабое основание;
NН4ОН – слабое основание;
NН4Сl –растворимая соль (содержит сопряженную сильную кислоту NН4+).
Буферные системы в растворенном состоянии образуют буферные растворы.
Буферные растворы, в отличие от буферных систем, могут быть многокомпонентными.
Кровь относят к буферным растворам.
Водородный показатель среды буферного раствора рассчитывают по уравнению Гендерсона-Гассельбаха:
pH = pKa + lg[соль]/[кислота]
pH - водородный показатель среды буферного раствора,
pKa – показатель константы кислотности слабой кислоты,
[соль]/[кислота]– количества соли и кислоты в момент равновесия; буферное соотношение.
В рабочем виде: 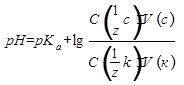
- C (1/z с), C (1/z к) – исходные молярные концентрации эквивалентов соли и кислоты, моль·дм-3;
- V (с), V (к) – объемы растворов соли и кислоты соответственно, см3.
Величину, характеризующую способность буферной системы противодействовать смещению реакции среды при добавлении кислот и щелочей, называют буферной емкостью (B). Буферную ёмкость можно определить по кислоте или по основанию.
Буферная ёмкость показывает сколько моль-эквивалентов сильной кислоты или щелочи следует добавить к 1 дм3 буферного раствора, чтобы изменить его рН на единицу.
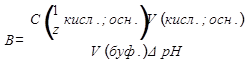 |
B – буферная ёмкость, моль дм-3;
C(1/z кисл.; осн.) – молярная концентрация эквивалента добавляемой кислоты или основания;
V(кисл.; осн.) – объем раствора добавляемой кислоты или основания, см3;
∆pH – изменение pH;
V (буф.)- объем буферного раствора, см3.
Для сохранения оптимальных условий обменных процессов необходимо постоянство pH внутренних сред организма. Постоянство кислотности сред, наряду с физиологическими механизмами поддерживается буферными системами организма.
Контрольные вопросы
1. Буферные системы, их состав, свойства, классификация. Механизм буферного действия. Буферные растворы
2. Уравнение кислых буферных систем Гендерсона-Гассельбаха, его вывод и анализ. Зона буферного действия.
3. Буферная емкость. Факторы, влияющие на величину буферной емкости.
4. Биологическая роль буферных систем. Буферные системы крови: гемоглобиновая, оксигемоглобиновая, белковая, водородкарбонатная, фосфатная, эфиры глюкозы и фосфорной кислоты различной степени замещенности.
5. Роль водородкарбонатной буферной системы в поддержании постоянства рН крови. Ацидоз. Алкалоз. Щелочной резерв крови.
|
|
|
|
|
Дата добавления: 2014-11-20; Просмотров: 2703; Нарушение авторских прав?; Мы поможем в написании вашей работы!