
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Влияние температуры на химическое равновесие. Уравнение изобары химической реакции
|
|
|
|
Для определения зависимости K 0от температуры в дифференциальной форме воспользуемся уравнением Гиббса‑Гельмгольца (III, 41)
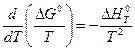
и уравнением (V, 11)
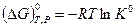
Комбинируя приведенные выше уравнения, получим
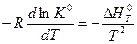 или
или 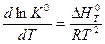 (V, 12)
(V, 12)
Уравнение (V, 12) называется уравнением Вант-Гоффа или уравнением изобары реакции (процесс осуществляется при P = const).
Для небольшого интервала температур T 1 ¸ T 2 тепловой эффект реакции можно принять постоянным. После интегрирования с учетом сделанного допущения уравнение (V, 12) примет вид
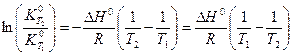 (V, 13)
(V, 13)
Выражение (V, 13) позволяет вычислить константу равновесия при одной из температур, если известны её значение при другой температуре, а также тепловой эффект реакции.
При неопределенном интегрировании уравнения (V, 12) получим
 (V, 14)
(V, 14)
где В — константа интегрирования.
Согласно уравнению (V, 14) зависимость ln K 0 от обратной температуры 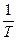 выражается прямой, тангенс угла наклона которой равен
выражается прямой, тангенс угла наклона которой равен 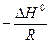 .
.
Этот метод вычисления теплового эффекта обычно используется, если его непосредственное определение (или вычисление по закону Гесса) затруднено, например, в тех случаях, когда реакция осуществляется только при высоких температурах.
Согласно уравнению (V,14), влияние температуры на константу равновесия определяется знаком теплового эффекта.
Если D H 0 > 0 (эндотермический процесс), то в координатах ln K 0 – 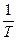 тангенс угла наклона прямой будет иметь отрицательное значение (угол наклона — тупой), следовательно, с повышением температуры константа будет увеличиваться, т. е. химическое равновесие смещается в сторону продуктов реакции (смотри рис.19).
тангенс угла наклона прямой будет иметь отрицательное значение (угол наклона — тупой), следовательно, с повышением температуры константа будет увеличиваться, т. е. химическое равновесие смещается в сторону продуктов реакции (смотри рис.19).
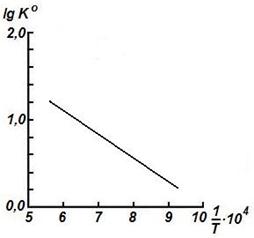
Рис. 19. Зависимость логарифма константы равновесия эндотермической реакции от обратной температуры (D H 0 > 0).
При D H 0 < 0 (экзотермическая реакция) тангенс угла наклона прямой будет иметь положительное значение (угол наклона — острый). С повышением температуры константа равновесия будет уменьшаться и химическое равновесие смещается в сторону исходных веществ (смотри рис.20).
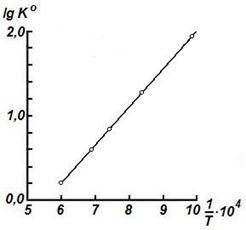
Рис. 20. Зависимость логарифма константы равновесия экзотермической реакции от обратной температуры (D H 0 < 0)
§ 7. Принцип Ле Шателье‑Брауна
Выведенная из состояния равновесия система вновь возвращается к состоянию равновесия. Ле Шателье и Браун высказали простой принцип, которым можно воспользоваться для предсказания того, в каком направлении система отреагирует на возмущение, выводящее ее из состояния равновесия.
Ле Шателье сформулировал этот принцип следующим образом:
«Любая система, находящаяся в равновесии, претерпевает в результате изменения одного из факторов, управляющих равновесием, компенсирующее изменение в таком направлении, что если бы это изменение было единственным, то оно вызвало бы изменение рассматриваемого фактора в противоположном направлении».
В качестве примера рассмотрим равновесие
N 2 + 3 H 2«2 NH 3
В этой реакции при превращении реагентов в продукты число молей уменьшается, что приводит к понижению давления при фиксированной температуре. Если в такой системе, находящейся в состоянии равновесия, внезапно увеличить давление, то система отреагирует на такое возмущение производством большего количества NH 3, отчего давление понизится. Компенсирующее изменение в системе произойдет в направлении, противоположном возмущению. Новое состояние равновесия будет отличаться бóльшим содержанием NH 3. Реакция синтеза аммиака — экзотермическая. Следовательно, если к системе подводится теплота, то равновесие сдвинется в сторону образования исходных веществ, а содержание NH 3 в равновесной смеси уменьшится.
(Заметим, что характер влияния давления и температуры на равновесие мы уже обсуждали ранее (смотри §§4и6, глава V). Закономерности, выявленные Ле Шателье и Брауном, позволили сделать обобщенный вывод относительно всех возможных факторов, оказывающих возмущающие воздействия на равновесную систему, в виде сформулированного ими принципа).
|
|
|
|
|
Дата добавления: 2014-11-29; Просмотров: 1274; Нарушение авторских прав?; Мы поможем в написании вашей работы!