
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
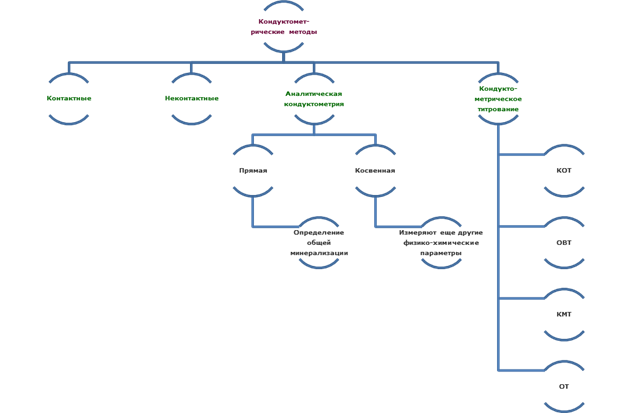
Кондуктометрия
|
|
|
|
Виды потенциометрического титрования
· Кислотно-основное
(рН-селективный электрод).
· Комплексонометрическое
(Ме-селективные электроды).
· Окислительно-восстановительное
(Pt-электрод).
· Осадительное (Ag-электрод; другие ионоселективные электроды).
Основана на измерении удельной электропроводности анализируемого раствора.
Электрическая проводимость – способность веществ пропускать электрический ток под действием внешнего электрического поля. Единица измерения – сименс (См).
Вещества, пропускающие электрический ток (проводники) по механизму переноса электричества делятся на 3 класса:
n проводники первого рода (электронные): Ме, полупроводники, сплавы, С, некоторые твердые соли и оксиды;
n проводники второго рода (ионные): растворы и расплавы электролитов;
n проводники третьего рода (смешанные): растворы щелочных и щелочноземельных Ме в жидком аммиаке, некоторые жидкие сплавы и соли.
Электрическая проводимость – W – величина обратная электрическому сопротивлению – R (W = 1/R).

Удельная электропроводность æ (См/см или Ом-1•см-1) равна электрической проводимости 1 мл раствора, находящегося между параллельными электродами площадью 1см2 при расстоянии между ними 1 см, другими словами, - это электрическая проводимость столба раствора длиной 1 см и площадью поперечного сечения 1 см2. Ее можно измерить, или рассчитать по формуле: æ = 1 / ρ = l / (R • S)
Для измерения удельной электропроводности анализируемого раствора используется электролитическая ячейка с переменным током.

Эквивалентная ионная электропроводность (подвижность) λ (См•см2/моль-экв) – это проводимость раствора, содержащего 1 моль эквивалента вещества и находящегося между двумя параллельными электродами, расстояние между которыми равно 1 см. Ее можно рассчитать по формуле:
λ = (1000 • æ) / СN.

Закон аддитивности электрической проводимости
В соответствии с законом независимого движения ионов Кольрауша эквивалентная электропроводность раствора электролита при бесконечном разбавлении называется предельной эквивалентной электропроводностью (λ¥ или λ0) и может быть представлена суммой предельных электрических проводимостей, или предельных подвижностей ионов: λ¥ = λ0(-) + λ0(+). Подвижности ионов в растворах с конечной концентрацией не являются постоянными и зависят от концентрации раствора: с ростом концентрации раствора подвижность ионов уменьшается: λ = λ0 – а • √СN, где а – константа.
 Молярная электропроводность m (См•см2/моль) – это проводимость раствора, содержащего 1 моль вещества и находящегося между двумя параллельными электродами, расстояние между которыми составляет 1 см. Ее можно рассчитать по формуле:
Молярная электропроводность m (См•см2/моль) – это проводимость раствора, содержащего 1 моль вещества и находящегося между двумя параллельными электродами, расстояние между которыми составляет 1 см. Ее можно рассчитать по формуле:
μ = (1000 • æ) / СM.
Измерение удельной электропроводности используется электролитическая ячейка с переменным током частотой 1000 Гц.
Кондуктометрически можно определять:
физико-химические свойства и характеристики веществ, например:
ü степень диссоциации,
ü константу диссоциации,
ü растворимость малорастворимых соединений и др.
Для их расчета можно использовать формулы:
ü степень диссоциации: α = λ / λ¥;
ü константа диссоциации:
Кд = {λ2 / [λ¥ • (λ¥ - λ)]} • CN;
ü растворимость малорастворимого соединения: S = (1000 • æнас) / λ¥.
|
|
|
|
|
Дата добавления: 2014-11-29; Просмотров: 531; Нарушение авторских прав?; Мы поможем в написании вашей работы!