
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Структурні формули у спрощеному стані
|
|
|
|
Структурні формули
Електронні формула
Вуглеводневі радикали
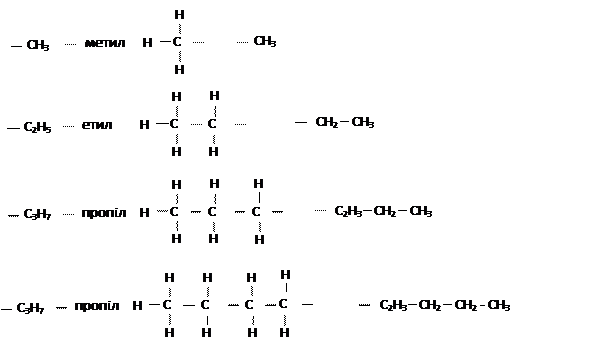 |
4.2.4 Вуглеводні.
Гомологічний ряд метану
Алкани, парафін, насичені вуглеводні
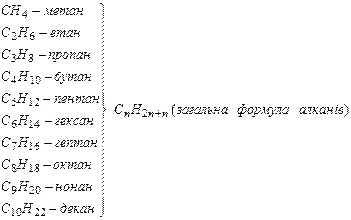
Сполуки, що складаються з Карбону і Гідрогену, в яких усі валентності атомів Карбону, що вільні після утворення зв'язків С - С, насичені атомами Н, називаються насиченими вуглеводнями.
- СН2 - гомологічна різниця.
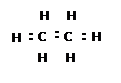 | 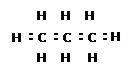 |
етану пропану тощо
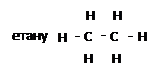 | 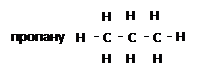 |
СН3 - СН3: СН3 - СН2 - СН3: СН3 - СН2 - СН2 - СН3:
етан пропан бутан
Пояснення різних випадків ізомерії дає теорія будови органічних сполук, створена в шестидесятих роках позаминулого сторіччя Бутлеровим, згідно з якою властивості речовин визначаються не тільки їх якісним і кількісним складом, як вважали раніше, але і внутрішньою будовою молекул, певним порядком з'єднаних між собою атомів, утворюючих молекулу. Цей внутрішній устрій Бутлеров назвав «хімічною будовою».
Особливо важливою була ідея Бутлерова про те, що атоми, з'єднуючись хімічно в певній послідовності відповідно до їх валентності, взаємно впливають один на одного таким чином, що частково змінюється їх власна природа, їх «хімічний зміст». Вчення Бутлерова про хімічну будову молекул складають теоретичну основу органічної хімії.
Класифікація
Сучасна класифікація органічних сполук ґрунтується на наступних положеннях:
Атоми в молекулах сполучені один з одним в певній послідовності. Зміна цієї послідовності приводить до утворення нової речовини з новими властивостями.
Поєднання атомів відбувається відповідно до їх валентності. Валентності всіх атомів в молекулі взаємно насичені. Вільних валентностей у атомів в молекулах не залишається.
Властивості речовин залежать від їх «хімічної будови», тобто від порядку поєднання атомів в молекулах і характеру їх взаємного впливу. Найбільш сильно впливають атоми, безпосередньо пов'язані один з одним. Тому молекули, що мають однакові угрупування атомів, володіють подібними властивостями.
Вуглець — чотиривалентний. Кожен атом вуглецю має чотири одиниці валентності, за рахунок яких він може приєднувати до себе інші атоми або атомні групи.
Атоми вуглецю здатні з'єднуватися один з одним, утворюючи «ланцюги» атомів, або «вуглецевий скелет» молекули.
Відповідно до будови вуглецевого ланцюга всі органічні сполуки підрозділяються на три великі групи.
Сполуки з відкритим ланцюгом атомів вуглецю, звані також ациклічними сполуками або з жирного ряду, оскільки до них відносяться жири і близькі до жирів речовини. Залежно від характеру зв'язків атомів вуглецю в «ланцюгах» ці сполуки ділять на насичені, такі, що містять в молекулах тільки прості зв'язки, і ненасичені, в молекулах яких є подвійні або потрійні зв'язки між атомами вуглецю.
Сполуки із замкнутим ланцюгом атомів вуглецю, або карбоциклічні сполуки. Вони утворюють дві підгрупи:
сполуки ароматичного ряду, кільця, що характеризуються наявністю у складі їх молекули шести атомів вуглецю з особливим чергуванням простих і подвійних зв'язків; таке кільце знаходиться в молекулі бензолу і називається бензольним кільцем;
аліциклічні сполуки — карбоциклічні сполуки, які розрізняють за кількістю атомів вуглецю в циклі і за характером зв'язків між цими атомами.
Гетероциклічні сполуки. Гетероциклічними називають сполуки, кільця яких окрім атомів вуглецю містять також атоми інших елементів (кисню, азоту, сірки тощо).
При класифікації органічних сполук за основні речовини беруться речовини, що відносяться до класу вуглеводнів, тобто сполуки, що складаються тільки з вуглецю і водню. Вся решта сполук розглядається як похідні з вуглеводнів шляхом заміни в їхніх молекулах частини або всіх атомів водню іншими атомами або атомними групами.
Групи атомів, які обумовлюють загальні хімічні властивості речовин, що належать до одного і того ж класу, називаються функціональними групами.
Якщо в молекулі речовини є декілька різних функціональних груп, то така речовина називається сполукою із змішаними функціями.
Насиченими називаються вуглеводні, в молекулах яких є тільки прості (одинарні) зв'язки. Простим представником насичених вуглеводнів є метан СН4.
Ненасиченими називаються вуглеводні, в молекулах яких є подвійні або потрійні зв'язки між атомами вуглецю.
Класифікація за хімічною будовою
За хімічною будовою поділяють на ациклічні і циклічні.
Ациклічні — це вуглеводні з відкритим ланцюгом атомів (аліфатичні, або сполуки жирного ряду). В свою чергу вони поділяються на насичені і ненасичені. Насичені — це вуглеводні із загальною формулою СпН2n+2 (парафіни, або алкани). Атоми вуглецю в цих сполуках пов'язані між собою і з атомами водню простими (одинарними) зв'язками: С-С і С-Н. Ненасичені — це вуглеводні із загальною формулою СпН2n (олефіни); СпН2n-2 (ацетиленові або дієнові), СпН2n-4, СпН2n-6 і т. д. Олефінові вуглеводні містять подвійний (олефіновий) зв'язок С=С, ацетиленові — потрійний зв'язок С ≡ С, дієнові — два подвійних зв'язки.
Циклічні — це сполуки із замкненим (кільцевим, або циклічним) ланцюгом атомів. Вони поділяються на ізоциклічні і гетероциклічні. Ізоциклічні — це вуглеводні із замкненим ланцюгом атомів вуглецю. До них належать:
аліциклічні, або поліметиленові (циклопарафіни і їх похідні);
ароматичні сполуки (бензол, нафталін і їх похідні). В циклічну систему гетероциклічних сполук, крім атомів вуглецю, входять атоми інших елементів (напр., кисню, азоту, сірки).
Вуглеводні СnН2n+2, СnН2n, СnН2n-2 і т. д. утворюють гомологічні ряди, в яких кожний подальший член ряду відрізняється від попереднього на групу СН2 (гомологічна різниця). При заміщенні в гомологічних рядах вуглеводнів одного або декількох атомів водню функціональними групами: Х (будь-який галоген), ОН, NH2, NO2, СООН і т. д. відповідно утворюються гомологічні ряди галогенопохідних RX, спиртів RОН, амінів RNH2, нітросполук RNO2, кислот RСООН і т. д., де R -радикал (СnН2n+2, СnН2n, СnН2n-2 і т. д.).
До найважливіших класів похідних вуглеводнів належать: галогенопохідні, спирти, ефіри, альдегіди та кетони, органічні кислоти, сірчисті сполуки (тіоспирти, тіоефіри, сульфокислоти), аміни та їх аналоги — фосфини, арсини, стибіни, бісмутини, металорганічні сполуки.
4.2.5 Номенклатурні системи назв органічних речовин
Для найменування окремих органічних сполук користуються різними номенклатурними системами. Широко застосовуються льєжські правила і номенклатура IUPAC. Поширені тривіальна, раціональна і женевська системи номенклатури.
За найбільш старою, тривіальною номенклатурою назви органічних сполук носять випадковий характер, наприклад: болотяний газ, мурашиний спирт, бурштинова кислота і т. д. Такі назви не дають уявлення про будову сполук, і тому тривіальна система не задовольняє вимог теорії і практики органічної хімії. Раціональна і женевська номенклатури основані на принципах наукової систематики органічних сполук: назва речовини дається відповідно до її хімічної будови.
За раціональною номенклатурою в основу найменувань органічних речовин покладені назви найпростіших (перших) сполук того або іншого гомологічного ряду. Більш складні сполуки розглядаються як похідні найпростіших, в яких атоми водню заміщені радикалами.
Згідно з женевською номенклатурою основою найменування є назва нормального вуглеводню, що містить те ж число атомів вуглецю, що і найдовший (або найскладніший) безперервний ланцюг вуглецевих атомів в даній сполуці. Початок нумерації головного ланцюга визначається передусім вуглеводневими радикалами, назви яких ставлять перед коренем слова. У разі однакового положення двох радикалів перевага віддається радикалу з меншим числом атомів вуглеводню. Кратні зв'язки, що позначаються закінченням -ен або суфіксом -ен- (подвійний зв'язок) або -ин(ін) (потрійний зв'язок) замість -ан у насиченого вуглеводню, займають друге місце при визначенні порядку нумерації, причому перевага надається потрійному зв'язку. Наступні місця належать функціональним кисневим або сірчаним групам і азотним групам, позначення яких відповідно ставляться в кінці слова і перед назвою вуглеводневих радикалів. Останнє за значенням місце при визначенні початку нумерації належить нефункціональним замісникам (галогенам, нітрозо-, нітро-, азидогрупам), позначення яких ставлять на самому початку назви органічної сполуки. Порядок розташування назв нефункціональних замісників зворотний до їх старшинства при визначенні нумерації. Цифрами позначають положення бічних ланцюгів, груп або кратних зв'язків в головному вуглеводневому ланцюгу; грецькими (іноді латинськими) числівниками — число однакових замінних груп або кратних зв'язків. Приклади: При найменуванні сполук із замкненим ланцюгом атомів загальні принципи женевської номенклатури залишаються незмінними, але є ряд особливостей.
Контрольні запитання:
1. Вуглеводні
2. Класифікація вуглеводнів
3. насичені вуглеводні (алкани)
4. Ізомерія
5. Номенклатура
Лекція 13 (заняття 19)
Тема 4.3 Вуглеводні: алкани, алкени, алкіни, алкадієни, арени та їх застосування
План:
4.3.1Алкани
4.3.2 Алкени
4.3.3 Алкіни
4.3.4 Алкадієни
4.3.5 Арени
4.3.1 Алкани
Алкани, парафін, насичені вуглеводні
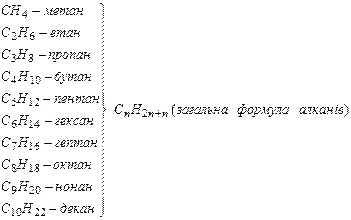
Сполуки, що складаються з Карбону і Гідрогену, в яких усі валентності атомів Карбону, що вільні після утворення зв'язків С - С, насичені атомами Н, називаються насиченими вуглеводнями.
Алкани, насичені вуглеводні (рос. алканы; англ. alkanes; нім. Alkane), насичені ациклічні вуглеводні, що мають загальну формулу CnH2n+2, їх також називають парафінами. Більшість їх хімічних реакцій з різними реагентами починається з розриву зв'язку С-Н, тоді як їх розпад при високих температурах йде передовсім по зв'язках С-С. Алкани складають значну частину вуглеводнів нафт і природних горючих газів. Із нафти і горючих газів виділено всі алкани нормальної будови, від метану до тритриаконтану (С33Н68) включно. Оскільки алкани містять максимально можливу кількість водню в молекулі, то вони характеризуються найбільшою масовою теплотою згоряння (енергоємністю), а з ростом кількості атомів масова теплота згоряння алканів зменшується (в метану 50207 кДж/кг). Внаслідок низької густини об'ємна теплота згоряння алканів менша, ніж вуглеводнів іншої будови з такою ж кількістю вуглецевих атомів у молекулі. За агрегатним складом алкани діляться на газоподібні (С1-С4), рідкі (С5-С15) і тверді (починаючи з С16), що кристалізуються при 200oС.
4.3.2 Алкени
Ненасичені вуглеводні (алкени, олефіни, алкіни)
Вуглеводні, що містять кратні зв'язки
подвійні (>С = С<) зв'язки
потрійні (- С ≡ С -) зв'язки
|
|
|
|
|
Дата добавления: 2014-11-29; Просмотров: 3929; Нарушение авторских прав?; Мы поможем в написании вашей работы!