
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Галогенопроизводные непредельных углеводородов
|
|
|
|
Галогенопроизводные непредельных углеводородов делят на две группы: первая включает в себя соединения, у которых галоген отделен от атома углерода с двойной связью одним или более атомами углерода CH2=CH–(CH2)n–Cl.
Эти соединения имеют такую же реакционную способность, как и галогенопроизводные предельных углеводородов. Однако в соединениях, где между атомами галогена и углерода при двойной связи стоит только одна группа -СН2 , например:
CH2 = CH – CH2Cl (хлористый аллил), галоген наиболее подвижен. Этот галоген замещается в более мягких условиях, чем в случае галогенопроизводных предельных углеводородов. Такую активность галогена связывают с большой устойчивостью карбкатиона, заряд которого компенсирован π - электронами двойной связи:

Мезомерный карбкатион
Мезомерный карбкатион имеет плоское строение; атака его нуклеофилом возможна с двух сторон плоскости, поэтому реакция нуклеофильного замещения у хлористого аллила протекают по механизму SN1, т.е. значительно легче, чем для третичных и вторичных алкилгалогенидов. Протекание реакции по механизму SN2 в данном случае затруднено, так как π - электронное облако двойной связи мешает молекуле нуклеофила образовать с хлористым аллилом переходное состояние.
Вторая группа объединяет соединения, в которых галоген непосредственно связан с атомом углерода, имеющим двойную связь. Например, CH2= CHClхлористый винил, хлорбензол  .
.
В таких соединениях галоген очень малоподвижен. Это объясняется взаимным влиянием двойной связи и атома галогена друг на друга. В случае винилхлорида происходит взаимодействие π - электронной системы двойной связи со свободными электронными парами атома галогена, которые смещаются при этом в сторону двойной связи (+ М -эффект сопряжения):
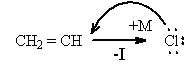
В то же время атом галогена за счет индуктивного эффекта (-I) оттягивает на себя π - электроны соседней связи. Эти два эффекта действуют в противоположных направлениях, и общее распределение электронной плотности в молекуле хлористого винила отражается мезомерной формулой:

При этом связь между углеродом и галогеном приобретает в известной степени характер двойной связи, ее длина укорачивается (от 1,78 до 1,72 А° ). Все это приводит к повышению энергии связи С-Х, уменьшению ее поляризации и понижению реакционной способности атома галогена. Образование карбкатиона затруднено и реакции по механизму SN1, проходить не могут. Реакции, протекающие по механизму SN2, также затруднены, так как затруднен подход нуклеофила к атому углерода в молекуле.
|
|
|
|
|
Дата добавления: 2014-12-26; Просмотров: 2730; Нарушение авторских прав?; Мы поможем в написании вашей работы!