
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Свойства ферментов
|
|
|
|
Ферменты отличаются от обычных катализаторов рядом свойств.
Термолабильность, или чувствительность к повышению температуры (рис. 22).
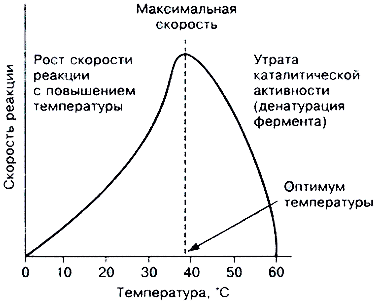
Рис. 22. Зависимость скорости ферментативной реакции от температуры
При температуре, не превышающей 45–50 °С, скорость большинства биохимических реакций повышается в 2 раза при повышении температуры на 10 °С согласно правилу Вант-Гоффа. При температуре выше 50 °С на скорость реакции влияниет тепловая денатурация белка-фермента, постепенно приводящая к его полной дезактивации.
Температура, при которой каталитическая активность фермента максимальна, называется его температурным оптимумом. Температурный оптимум для большинства ферментов млекопитающих лежит в пределах 37-40 °С. При низких температурах (0 °С и ниже) ферменты, как правило, не разрушаются, хотя активность их падает почти до нуля.
Зависимость активности фермента от значения рН среды (рис. 23).
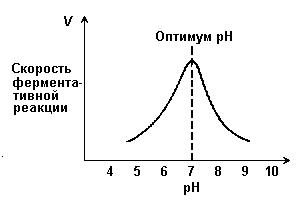
Для каждого фермента существует оптимальное значение рН среды, при котором он проявляет максимальную активность. рН-оптимум действия ферментов животных тканей лежит в пределах узкой зоны концентрации водородных ионов, соответствующей выработанным в процессе эволюции физиологическим значениям рН среды 6,0-8,0. Исключения составляют пепсин – 1,5-2,5; аргиназа – 9,5-10.
|
| Рис. 23. Зависимость скорости ферментативной реакции от рН среды |
Влияние изменений рН среды на молекулу фермента заключается в воздействии на степень ионизации его активных групп, а, следовательно, на третичную структуру белка и состояние активного центра. рН меняет также ионизацию кофакторов, субстратов, фермент-субстратных комплексов и продуктов реакции.
Специфичность. Высокая специфичность действия ферментов обусловлена конформационной и электростатической комплементарностью между молекулами субстрата и фермента и уникальной структурной организацией активного центра, обеспечивающими избирательность протекания реакции.
Абсолютная специфичность – способностьфермента катализировать единственную реакцию. Например, уреаза катализирует реакцию гидролиза мочевины до NH3 и СО2, аргиназа – гидролиз аргинина.
Относительная (групповая) специфичность – способность фермента катализировать группу реакций определенного типа. Относительной специфичностью, например, обладают гидролитические ферменты пептидазы, гидролизующие пептидные связи в молекулах белков и пептидов, липаза, гидролизующая сложноэфирные связи в молекулах жиров.
Стереохимической специфичностью обладают ферменты, катализирующие превращения только одного из пространственных изомеров. Фермент фумараза катализирует превращение транс-изомера бутендиовой кислоты - фумаровой кислоты в яблочную, и не действует на цис-изомер - малеиновую кислоту.
Высокая специфичность действия ферментов обеспечивает протекание лишь определенных химических реакций из всех возможных превращений.
|
|
|
|
|
Дата добавления: 2015-03-31; Просмотров: 482; Нарушение авторских прав?; Мы поможем в написании вашей работы!