
- Р Р‡.МессенРТвЂВВВВВВВВжер
- ВКонтакте
- РћРТвЂВВВВВВВВнокласснРСвЂВВВВВВВВРєРСвЂВВВВВВВВ
- РњРѕР№ Р В Р’В Р РЋРЎв„ўР В Р’В Р РЋРІР‚ВВВВВВВВРЎР‚
- LiveJournal
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Влияние на ферменты активаторов и ингибиторов
|
|
|
|
Контроль количества фермента.
РЕГУЛЯЦИЯ АКТИВНОСТИ ФЕРМЕНТОВ
Активность фермента определяют по скорости реакции, катализируемой ферментом, при стандартных условиях измерения (оптимальных условиях температуры, рН среды и полном насыщении фермента субстратом). О скорости ферментативной реакции судят или по скорости убыли субстрата, или по скорости образования продукта реакции.
Одна стандартная единица активности фермента (Е или U) - такое количество фермента, которое катализирует превращение 1 мкмоль вещества за 1 мин.
В связи с введением Международной системы единиц (СИ) предложено выражение активности фермента в каталах (кат, kat): 1 кат - каталитическая активность, способная осуществлять реакцию со скоростью, равной
1 моль/с. 1 U (международная единица) фермента составляет 16,67 нкат.
Удельная активность фермента - число единиц ферментативной активности на 1 мг белка (или число каталов на 1 кг активного белка).
Молярная активность равна числу единиц активности фермента, деленному на количество фермента, выраженное в микромоль. Она показывает, сколько молекул субстрата превращается одной молекулой фермента за
1 мин.
Существует два основных способа контроля скорости ферментативных реакций.
Количество фермента в клетке определяется соотношением скоростей его синтеза и распада. На скорость синтеза фермента влияют присутствие субстрата и продуктов реакции. В клетках имеются конститутивные ферменты - постоянно присутствующие в клетках - в отличие от индуцируемых ферментов, синтезирующихся в определенных условиях. Этот способ регуляции скорости ферментативной реакции является достаточно медленным процессом и проявляется спустя несколько часов.
2. Контроль активности фермента. В результате данного способа регуляции активность ферментов меняется очень быстро.
Активаторами ферментов являются катионы многих металлов, например, ионы кальция активируют липазу. Некоторые анионы также способны активировать ферменты: a-амилаза слюны активируется ионами хлора.
Активаторами ферментов могут быть разнообразные органические вещества (желчные кислоты повышают активность панкреатической липазы).
Ингибиторы тормозят действие ферментов.
По характеру своего действия ингибиторы подразделяются на обратимые и необратимые. В основе такого деления лежит прочность соединения ингибитора с ферментом.
Обратимые ингибиторы - соединения, которые нековалентно взаимодействуют с ферментом и могут отделяться от фермента.
Обратимое ингибирование может быть конкурентным. Конкурентный ингибитор имеет структуру, похожую на структуру субстрата, но несколько от нее отличающуюся. Он конкурирует с субстратом за связывание в субстратсвязывающем участке активного центра. Конкурентный ингибитор увеличивает Кm.
Пример: фермент сукцинатдегидрогеназа дегидрирует сукцинат, превращая его в фумарат. Малонат,структурно сходный с сукцинатом, связывается в активном центре фермента, но не может дегидрироваться (рис. 24).
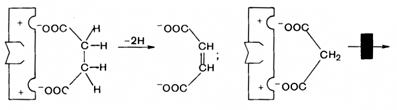
Рис. 24. Схема конкурентного ингибирования
Степень торможения будет определяться соотношением концентраций малоната и сукцината. При высокой концентрации субстрата последний может полностью вытеснять ингибитор из активного центра, поэтому umax не изменяется.
Метод конкурентного торможения широко применяется в медицинской практике. Сульфаниламиды – препараты, используемые для лечения инфекционных болезней, – структурные аналоги парааминобензойной кислоты, участвующей в метаболизме бактерий. Сульфаниламид вытесняет пара-аминобензойную кислоту из комплекса с ферментом, что приводит к гибели микроорганизмов.
При обратимом неконкурентном ингибировании субстрат и ингибитор связываются с разными центрами. Увеличение концентрации субстрата не препятствует связыванию ингибитора. Неконкурентный ингибитор уменьшает umax, а Кm не меняется.
Известно бесконкурентное ингибирование: ингибитор связывается с ферментом не в каталитическом центре только с ES-комплексом в виде тройного комплекса. Бесконкурентный ингибитор увеличивает Кm и уменьшает umax.
Необратимые ингибиторы - соединения, которые могут специфически связывать функционально важные группы активного центра, образуя ковалентные прочные связи с ферментом.
Любые агенты, вызывающие денатурацию белка, приводят к необратимой инактивации фермента, но она не связана с механизмом действия ферментов.
Неконкурентное необратимое ингибирование вызывается тяжелыми металлами (ртуть, свинец и др. присоединяются к HS-группам полипептидной цепи), солями синильной кислоты, оксидом углерода (II) и др.
При конкурентном необратимом торможении ингибитор, обладающий структурным сходством с субстратом, соединяется с ферментом, подменяя собой субстрат.
Диизопропилфторфосфат структурно близок к нейромедиатору ацетилхолину и присоединяется вместо него к ферменту ацетилхолинэстеразе. Он блокирует активный центр фермента, и в результате утрачивается способность нейронов проводить нервные импульсы.
|
|
|
Дата добавления: 2015-03-31; Просмотров: 761; Нарушение авторских прав?; Мы поможем в написании вашей работы!