
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Скорость химических реакций
|
|
|
|
Откуда
Следовательно, для данной реакции
Рассчитать изменение стандартных энтальпии и энтропии химической реакции
УРОВЕНЬ В
ЭНЕРГЕТИКА ХИМИЧЕСКИХ РЕАКЦИЙ
4HCl(г) + O2(г) = 2Н2О(г) + 2Сl2(г)
| Дано: Уравнения химической реакции | Решение Изменение стандартных энтальпии и энтропии химической реакции рассчитываем на основании первого следствия из закона Гесса: | |||
| D r Ho(298 K) –? D rS o(298 K) –? | ||||
D rH o(298 K) = [2D f Ho(298 K, Н2О(г)) + 2D f Ho(298 K, Cl2(г))] –
– [4D fH o(298 K, НCl(г)) + D fH o(298 K, О2(г))];
D rS o(298 K) = [2 S o(298 K, Н2О(г)) + 2 S o(298 K, Cl2(г))] –
– [4 S o(298 K, НCl(г)) + S o(298 K, О2(г))],
где D rH o(298 K, В) и S o(298 K, В) – стандартные энтальпии образования и энтропии веществ, которые находим из таблицы:
| 4HCl(г) | + О2(г) | = 2Н2О(г) | + 2Сl2(г) | |
| D rH o(298K) кДж/моль | 4(-92,3) | 2(-241,84) | ||
| S o(298 K), Дж/(мольК) | 4(186,8) | 2(188,7) | 2(222,9), |
тогда:
D rH o(298 K) = 2(–241,84) – 4(–92,3) = –114,48 кДж;
∆ rS o(298 K) = (2·188,7 + 2·222,9) – (4·186,8 + 205) = –129 Дж/К.
Ответ: D rH o(298 K) = –114,48 кДж, D rS o(298 K) = –129 Дж/К.
2. Стандартная энтальпия сгорания этилена (С2Н4) равна
–1410,8 кДж/моль. Написать термохимическое уравнение сгорания этилена и вычислить стандартную энтальпию его образования.
| Дано: D flH o(298 K, C2H4(г)) = = –1410,8 кДж/моль | Решение Составляем реакцию сгорания 1 моль этилена: |
| D fH o(298 K, C2H4(г)) –? |
1C2H4(г) + 3О2(г) = 2СО2(г) + 2Н2О(ж);
D flH o(298 K) = – 1410,8 кДж/моль.
Стандартной энтальпией сгорания вещества называется тепловой эффект реакции полного сгорания 1 моль органического вещества до СО2(г) и Н2О(ж) при стандартных условиях.
D flH o(298 K) = D rH o(298 K) = –1410,8 кДж.
Для определения D fH o(298 K, C2H4(г)) используем первое следствие из закона Гесса для этой же реакции:
D rH o(298 K) = 2D fH o(298 K, СО2(г)) + 2D fH o(298K, Н2О(ж)) –
– D fH o(298 K, С2Н4(г)) – 3D fH o(298 K, О2(г)).
D fH o(298 K, С2Н4(г)) = 2D fH o(298 K, СО2(г)) +
+ 2D fH o(298K, Н2О(ж)) – D rH o(298K) – 3D fH o(298K, О2(г)).
Значения стандартных энтальпий образования (Н2О(ж) и СО2(г)) берем из таблицы:
D fH o(298 K, С2Н4(г)) = 2(–393,5) +
+ 2(–285,8) – (–1410,8) = 52,2 кДж/моль.
Ответ: D fH o(298 K, С2Н4(г)) = 52,2 кДж/моль.
3. По заданным термохимическим уравнениям рассчитать стандартную энтальпию образования Fe2O3(к) из простых веществ:
Fe(к) +1/2O2(г) = FeO(к), D rH o(298 K, 1) = – 264,8 кДж. (4.1)
4FeO(к) + O2(г) = 2Fe2O3(к), D rH o(298 K, 2) = – 585,2 кДж. (4.2)
| Дано: Термохимические уравнения двух реакций | Решение Стандартная энтальпия образования вещества есть тепловой эффект реакции образования 1 моль Fe2O3(к)из простых веществ при стандартныхусловиях. Запишем |
| D rH o(298 K) искомой реакции |
термохимическое уравнение реакции образования Fe2O3(к) из простых веществ Fe(к) и O2(г):
2Fe(к) + 3/2O2(г) = Fe2O3(к). (4.3)
Из двух реакций (4.1) и (4.2) необходимо получить реакцию (4.3). Для этого складываем термохимические уравнения (4.1) и (4.2), предварительно умножив на 2 стехиометрические коэффициенты реакции (4.1) и разделив на 2 стехиометрические коэффициенты реакции (4.2):
2Fe(к) + O2(г) + 2FeO(к) + ½O2(г) = 2FeO(к) + Fe2O3(к).
После сокращения получаем уравнение реакции (4.3):
2Fe(к) + 3/2O2(г) = Fe2O3(к).
Для определения изменения стандартной энтальпии реакции (4.3) аналогичные математические действия осуществляем с тепловыми эффектами приведенных реакций (4.1) и (4.2):
D rH o(298 K, 3) = 2D rH o(298 K, 1) + ½D rH o(298 K, 2) =
= 2(-264,8) + ½(-585,2) = – 822,2 кДж.
Так как реакция (4.3) соответствует образованию 1 моль Fe2O3 из простых веществ, то
D fH o(298 K, Fe2O3) = – 822,2 кДж/моль.
Ответ: D fH o(298 K, Fe2O3) = – 822,2 кДж/моль.
Дано:
Е ак = 60 кДж/моль а) Т 1 = 320 К,
Т 2 = 360 К б) Т = 298 К,
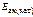 = 48кДж/моль = 48кДж/моль
| Решение
а) Из уравнения Аррениуса получаем
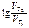 = = 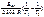 ; ;
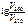 = = 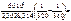 1,09,
где 103 – коэффициент пересчета килоджоулей в
джоули, тогда 1,09,
где 103 – коэффициент пересчета килоджоулей в
джоули, тогда
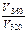 =101,09 = 12,3 раза. =101,09 = 12,3 раза.
|
а) 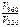 –?
б) –?
б) 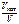 –? –?
|
| Дано: Уравнение реакции, Кр = 1 | Решение
CO2(г) + C(к) <=> 2CO(г), 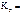 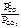 . .
|
| Т –? |
|
|
|
|
|
Дата добавления: 2015-03-31; Просмотров: 361; Нарушение авторских прав?; Мы поможем в написании вашей работы!