
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Внутрішня енергія реального газу
|
|
|
|
Внутрішня енергія реального газу U складається з кінетичної енергії теплового руху його молекул (визначає внутрішню енергію ідеального газу, що дорівнює U к = CVT для одного моля) і потенціальної енергії міжмолекулярної взаємодії U n. Потенціальна енергія реального газу зумовлена лише силами притягання між молекулами, які приводять до виникнення внутрішнього тиску на газ 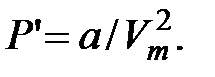 Робота, яка витрачається для подолання сил притягання, що діють між молекулами газу, іде на збільшення потенціальної енергії системи, тобто
Робота, яка витрачається для подолання сил притягання, що діють між молекулами газу, іде на збільшення потенціальної енергії системи, тобто 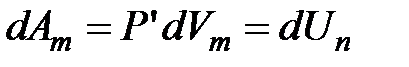 або
або 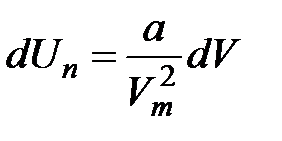 . Звідси знаходимо потенціальну енергію одного моля реального газу:
. Звідси знаходимо потенціальну енергію одного моля реального газу: 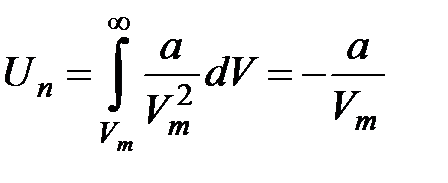 . Знак "-" означає, що молекулярні сили, які створюють внутрішній тиск, є силами притягання. Тоді повна внутрішня енергія одного моля реального газу дорівнює
. Знак "-" означає, що молекулярні сили, які створюють внутрішній тиск, є силами притягання. Тоді повна внутрішня енергія одного моля реального газу дорівнює 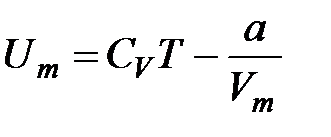 .
.
Вона зростає зі збільшенням температури й об’єму газу.Якщо газ розширюється без теплообміну з навколишнім середовищем і не виконує роботу, то на підставі першого закону термодинаміки одержимо, що 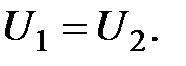 Отже, при адіабатичному розширенні без здійснення зовнішньої роботи внутрішня енергія газу не змінюється. Для ідеального газу це означає, що при адіабатному розширенні у вакуум (тобто без виконання роботи) його температура не змінюється Т 1 = Т 2. Для реального газу, з огляду на те, що для одного моля газу
Отже, при адіабатичному розширенні без здійснення зовнішньої роботи внутрішня енергія газу не змінюється. Для ідеального газу це означає, що при адіабатному розширенні у вакуум (тобто без виконання роботи) його температура не змінюється Т 1 = Т 2. Для реального газу, з огляду на те, що для одного моля газу 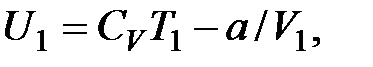
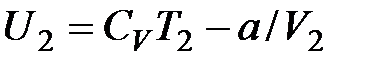 , одержуємо
, одержуємо 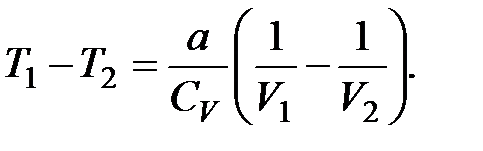 Оскільки V2 > V1,то T1 >T2, тобто реальний газ при адіабатному розширенні у вакуум охолоджується.
Оскільки V2 > V1,то T1 >T2, тобто реальний газ при адіабатному розширенні у вакуум охолоджується.
|
|
|
|
|
Дата добавления: 2015-05-23; Просмотров: 2335; Нарушение авторских прав?; Мы поможем в написании вашей работы!