
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Рівняння Ван-дер-Вальса.Вирази до поправок р і б
|
|
|
|
Врахуємо для реального газу власний об’єм молекул і дію сил притягання. Наявність сил відштовхування, які не дозволяють проникнути іншим молекулам у зайнятий молекулою об’єм, зводиться до того, що фактичний вільний об’єм, у якому можуть рухатися молекули реального газу, буде меншим, ніж об’єм ідеального газу: Vm® Vm - b, де Vm - b – об’єм одного моля реального газу; b – об’єм, що "заборонений" для руху молекул.
| Рис. 2.27 |
| V o |
NA – число Авогадро (кількість молекул в одному молі речовини).
Дія сил притягання між молекулами реального газу приводить до появи додаткового тиску, що називається внутрішнім тиском: Р ® Р + Р'. Тут 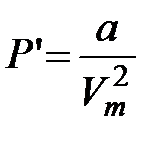 – додатковий тиск, який, згідно з розрахунками Ван-дер-Ваальса, обернено пропорційний квадрату молярного об’єму газу, а – стала Ван-дер-Ваальса, яка характеризує сили міжмолекулярного притягання. Щоб отримати рівняння стану реального газу, уведемо у рівняння Менделєєва–Клапейрона поправки, що враховують власний об’єм молекул і сили притягання молекул. Тоді рівняння стану (для одного моля) набуває вигляду:
– додатковий тиск, який, згідно з розрахунками Ван-дер-Ваальса, обернено пропорційний квадрату молярного об’єму газу, а – стала Ван-дер-Ваальса, яка характеризує сили міжмолекулярного притягання. Щоб отримати рівняння стану реального газу, уведемо у рівняння Менделєєва–Клапейрона поправки, що враховують власний об’єм молекул і сили притягання молекул. Тоді рівняння стану (для одного моля) набуває вигляду:
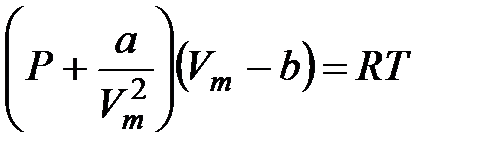 . Це рівняння називається рівнянням Ван-дер-Ваальса.
. Це рівняння називається рівнянням Ван-дер-Ваальса.
Враховуючи, що V=nVm (n = m/M – кількість молів), отримаємо рівняння для довільної кількості речовини:
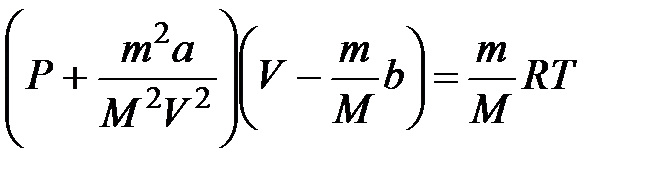 . a i b – сталі Ван-дер-Ваальса, постійні для кожного газу величини, що визначаються дослідним шляхом.
. a i b – сталі Ван-дер-Ваальса, постійні для кожного газу величини, що визначаються дослідним шляхом.
|
|
|
|
|
Дата добавления: 2015-05-23; Просмотров: 757; Нарушение авторских прав?; Мы поможем в написании вашей работы!