
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Методи одержання і будова ліофобних колоїдних розчинів
|
|
|
|
Ліофобні і ліофільні (молекулярні) колоїди
За характером взаємодії між частинками дисперсної фази і дисперсійного середовища колоїди поділяють на ліофільні (від грецького lyo – розчиняю, phіlia – люблю) і ліофобні (phobia – страх, нелюбов).
Ліофільні колоїди характеризуються інтенсивною взаємодією частинок дисперсної фази з дисперсійним середовищем.
В ліофобних системах майже повністю відсутня взаємодія між молекулами середовища і частинками дисперсної фази.
Дослідженнями В.Каргіна, С.Ліпатова та інших було доведено, що системи, які раніше називали ліофільними золями, являють собою істинні розчини високомолекулярних сполук (ВМС).
Визнано доцільним замінити термін „ліофільні колоїди” або терміном „розчини ВМС”, або “молекулярні колоїди”.
До ліофобних колоїдів належать колоїдні розчини металів, їх оксидів, гідроксидів, сульфідів та інших солей.
Прикладом ліофільних (молекулярних) колоїдів можуть слугувати золі білків, полісахаридів тощо.
Ліофобні колоїдні розчини одержують двома методами: дисперсійним і конденсаційним.
Дисперсійний метод полягає в подрібненні грубих частинок дисперсної фази до розмірів колоїдних шляхом механічного розтирання їх з рідиною або в спеціальних колоїдних млинах.
Конденсаційний метод – це об’єднання атомних і молекулярних частинок в значно більші агрегати, яке відбувається при перебігу хімічних реакцій за певних умов. Завдяки дослідженням А.Думанського, Н.Пєскова, С.Ліпатова, А.Фрумкіна, а також Веймарна, Паулі, Фаянса, Кройта була створена так звана міцелярна теорія будови колоїдних частинок. Уявлення про міцелярну будову колоїдних частинок поширювалась спочатку на всі системи, однак подальші дослідження показали, що розчини ВМС мають іншу будову. В наш час міцелярна теорія будови колоїдних частинок зберігає своє значення тільки для ліофобних золів.
Ліофобний колоїдний розчин складається з двох частин: міцел і інтерміцелярної рідини. Міцели – це окремі частинки, які утворюють дисперсну фазу золя, а інтерміцелярна рідина – це дисперсійне середовище золя, яке містить розчинник і всі інші розчинені в ньому речовини. Наприклад, якщо в киплячу воду вливати при помішуванні розчин ферум(ІІІ) хлориду, то утворюється колоїдний розчин ферум(ІІІ) гідроксиду Fe(OH)3 внаслідок реакції гідролізу:
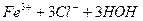 L
L 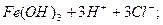
 L
L 
Молекули Fe(OH)3 утворюють ядро колоїдної частинки [Fe(OH)3]m, де m = 400-500 молекул. Ядро може адсорбувати з розчину йони, близькі за природою до його складу, в даному випадку йони Fe3+. (Адсорбція – це явище поглинання і концентрування на поверхні поділу фаз молекул або йонів з навколишнього середовища).
Йони, адсорбовані ядром, називають потенціалвизначаючими, тому що вони визначають заряд колоїдних частинок.
Ядро колоїдної частинки з адсорбованими потенціал- визначаючими йонами притягає до себе з середовища йони протилежного заряду (Cl-). Ці йони утворюють адсорбційний шар протийонів. Потенціалвизначаючі йони і протийони – гідратовані, і тому разом з ними приходить вода, молекули якої утворюють гідратну оболонку. Весь цей комплекс переміщується в розчині як єдине ціле і його називають колоїдною частинкою. До складу колоїдної частинки входить тільки частина протийонів. Їх називають зв’язаними. Інша частина протийонів залишається в дисперсійному середовищі (в рідкій фазі). Ці протийони утворюють дифузний шар, і їх називають вільними. Вони надають заряд дисперсійному середовищу. Колоїдну частинку з гідратованими протийонами дифузного шару називають міцелою, яка вважається структурною одиницею ліофобного колоїдного розчину.
В колоїдному розчині ферум(ІІІ) гідроксиду колоїдна частинка і міцела мають такий склад:
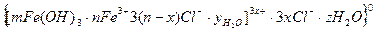
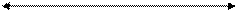
колоїдна частинка

 міцела
міцела
Будова міцели ферум(ІІІ) гідроксиду може бути представлена схемою (рис.26).
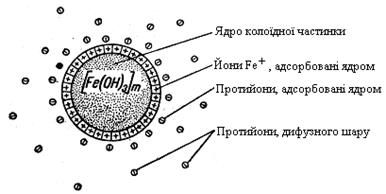
Рис. 26. Схема будови міцели ферум(ІІІ) гідроксиду
Кислі речовини (силікатна кислота, сульфіди металів, кислі барвники тощо) в водному розчині мають від’ємний заряд. Склад колоїдної частинки і міцели силікатної кислоти можна представити так:

колоїдна частинка

 міцела
міцела
Ферум, кадмій, алюміній, хром гідроксиди, основні барвники мають додатний заряд.
Різниця потенціалів між рухомою (дифузною) і нерухомою (адсорбційною) частиною подвійного електричного шару називається електрокінетичним потенціалом. Він позначається буквою ξ - дзета (рис.27).

Рис. 27. Схема подвійного електричного шару
Величина ξ - потенціала пов’язана з товщиною дифузного шару протийонів. Чим більше розмитий цей шар, тим більша величина потенціала.
Знак ξ - потенціала залежить від хімічної природи твердої фази.
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 3464; Нарушение авторских прав?; Мы поможем в написании вашей работы!